コノトキシンの鎮痛機序|MVIIAとジコノチド
コノトキシンの鎮痛機序|MVIIAとジコノチド
海の捕食者であるイモガイは、数百種規模に広がる系統のなかで、多様な小型ペプチド毒コノトキシンを磨き上げてきました。その到達点のひとつが、ω-コノトキシンMVIIAの作用をもとに生まれ、2005年にFDA承認へ至ったジコノチドです。
海の捕食者であるイモガイは、数百種規模に広がる系統のなかで、多様な小型ペプチド毒コノトキシンを磨き上げてきました。
その到達点のひとつが、ω-コノトキシンMVIIAの作用をもとに生まれ、2005年にFDA承認へ至ったジコノチドです。
ただし、毒がそのまま“夢の鎮痛薬”になるわけではありません。
CaV2.2を狙い撃ちする高い選択性は強みですが、ペプチド薬ゆえに血液脳関門と投与経路の壁があり、臨床では髄腔内投与に加えて、少量から週単位でじわじわ増やす設計が背骨になります。
毒性学と薬理の実務で、治療域の狭い薬ほどこの漸増設計が成否を分ける場面を見てきた立場から言えば、ここを飛ばしてジコノチドは語れません。
この記事では、イモガイの捕食戦略から分子機構、承認薬の利点と限界、さらにCVIDやRgIA系、徐放製剤、AI設計までを一気通貫でたどります。
難治性疼痛の新しい選択肢を知りたい人にも、毒が薬へ反転する条件を分子レベルで理解したい人にも、全体像がつかめる構成です。
イモガイの毒とは何か――コノトキシンの基礎

イモガイの捕食戦略と毒器官
イモガイは巻貝の仲間ですが、餌の取り方は「おとなしい貝」の印象から大きく外れます。
イモガイはすべて肉食性で、魚を狙う種、ゴカイ類を狙う種、ほかの貝を狙う種へと食性が分かれ、獲物に応じて毒の設計図を作り分けてきました。
捕食の中核にあるのが、銛のように改変された歯舌(ラドゥラ)と毒腺です。
歯舌は単なる「歯」ではなく、発射される器具として機能し、そこから獲物の体内へ毒が注入されます。
動かない殻の中から、神経系を狙って獲物の運動を止める。
イモガイの毒は、この捕食戦略のために磨かれてきた分子群です。
この構造を知ると、イモガイ毒がなぜ薬理学で注目されるのかも見えてきます。
獲物を短時間で無力化するには、筋肉や神経のスイッチを担う分子を正確に叩く必要があります。
実際、コノトキシンの多くはイオンチャネルや受容体を標的にします。
神経細胞の興奮、シナプスでの伝達、筋収縮の引き金といった「電気信号の要所」に作用するため、基礎研究のツールとしても、創薬の種としても価値が高いのです。
一方で、危険性の理解には言い回しの整理が欠かせません。
一般向けには「1個体で約30人分の致死量」といった刺激的な表現が流通していますが、こうした定型句は一次根拠が追いにくく、俗説として広がった面が濃い記述です。
イモガイ、とくに魚食性の大型種が人にとって危険な毒を持つこと自体は事実ですが、致死量を人口換算で断言する書き方は、この段階では避けたほうが科学的です。
本記事の軸は、毒を「どう扱うか」の実用情報ではなく、「なぜそんな分子が生まれ、どこが薬になるのか」の理解にあります。
そのため、毒の抽出、製造、具体的な取扱い手順には触れません。
ここで見るべきなのは、海の捕食者が進化の中で作り上げた分子標的性そのものです。
コノトキシン=多様なペプチド群という前提
まず押さえたいのは、コノトキシンは単一の化学物質名ではないという点です。
これはイモガイが作る毒の中に含まれる、小型ペプチド群の総称です。
長さはおおむね10〜30残基ほどで、短い配列の中に複数のシステイン残基を持ち、ジスルフィド結合で立体構造を固定したものが多く見られます。
記事全体の主役であるMVIIAもその一つで、25アミノ酸残基、6個のシステイン、3本のジスルフィド結合という、いかにも「小さいのに仕事が鋭い」ペプチドです。
このとき似た語として出てくるのが「コノペプチド」です。
広い文脈ではコノトキシンとほぼ同義に扱われますが、学術的には少し丁寧な使い分けがあります。
毒として機能することが明確なものをコノトキシン、イモガイ由来ペプチドをより広く指すときにコノペプチドと呼ぶ、という整理です。
ただ、実際の文献でも厳密な統一はなく、読者向けの本記事では混乱を避けるためコノトキシンで統一します。
研究現場でこの分野に触れると、最初に修正される思い込みがあります。
「この種の毒はこういう成分でできている」と一枚岩で捉えてしまう見方です。
生物毒は、実務感覚ではむしろ“混ざっていて当たり前”です。
同じ種名がついていても、個体が違えば毒の中身は揃いません。
餌の違い、成長段階、地域集団の差で、目立つ成分も比率もずれます。
毒性学の仕事では、この「同じ名前でも中身は一様ではない」という前提を外すと、議論がすぐに雑になります。
イモガイ毒はその典型で、1種につき1毒素ではなく、1個体が多数のペプチドを組み合わせた毒カクテルを持つと考えるほうが実態に近いです。
だからこそ、研究や創薬では個々のペプチド名だけでなく、「どの群に属するか」が重視されます。
たとえば α-コノトキシンはニコチン性アセチルコリン受容体、μ-コノトキシンは電位依存性Naチャネル、ω-コノトキシンは電位依存性Caチャネルを主標的とする代表的な作用群として整理されます。
ここでいう“群”は、読者にとっては「どの神経スイッチを狙うか」の地図です。
MVIIAが属する ω-コノトキシン群は、その中でも N型電位依存性カルシウムチャネル、すなわちCaV2.2への作用で知られ、ここからジコノチドという承認薬へつながりました。
ただし、作用群と遺伝子スーパーファミリーは同じ分類軸ではありません。
一般解説ではこの二つが混ざりがちですが、片方は「何に効くか」、もう片方は「どんな配列系統か」の整理です。
コノトキシンは数が多いぶん、分類も階層的になります。
創薬の話題で迷子にならないためには、名称より先に「これは単独分子ではなく、多数のペプチドからなる世界だ」と理解しておくと、後のMVIIAやジコノチドの位置づけが見通しやすくなります。
種数と命名・分類の揺らぎ
イモガイの全体像をつかみにくくしている理由の一つが、種数と分類の揺らぎです。
一般向けには約500種と書かれることが多い一方、研究文脈では500〜700種以上、あるいは分類体系によってはそれを上回る数え方も出てきます。
ここで起きているのは、単純な数え間違いではありません。
どこまでをConus属に含めるか、近縁群をどう切り分けるか、シノニムをどこまで整理したかで、見かけの種数が動くのです。
したがって、現時点ではイモガイは分類体系により種数表記が変わる、数百種規模の巨大グループと捉えるのが最も安全です。
命名の揺れは、毒素名でも起こります。
MVIIAのような著名なコノトキシンは比較的追いやすいのですが、文献をまたぐと旧称、別表記、前駆体由来の呼び方が交差します。
しかも、同じ標的に作用しても別の種から別名のペプチドが見つかるため、初学者には「名前が違うだけで何が同じなのか」が見えにくい構造になっています。
こうした混線をほどくために、ConoServerのような学術データベースが整備され、配列、構造、遺伝子情報を紐づけて管理する基盤が育ってきました。
2022年時点の文献では、122種から8,134件のコノペプチドが蓄積されたと整理されており、この数字だけでも「コノトキシン」を単数形の感覚で捉えるのが無理だとわかります。
表記統一もこの分野では地味に効きます。
本記事では、毒の総称をコノトキシン、動物群をイモガイ、代表ペプチドをMVIIA、医薬品名をジコノチドで通します。
こうしておかないと、同じ対象を別名で追いかけるだけで認知負荷が上がるからです。
分類が揺れる分野ほど、記事内のラベルは固定したほうが、読者は作用機序そのものに集中できます。
この命名の複雑さは、裏を返せば資源の豊かさでもあります。
数百種規模の捕食者が、それぞれ異なる獲物に合わせて、短いペプチドを無数に作り分けてきた。
その結果、神経系の分子を精密に叩くライブラリが自然界に蓄積されたわけです。
次の段階で見るMVIIAとジコノチドは、その膨大なライブラリから実際に医薬品へ届いた、きわめて稀で具体的な成功例として位置づけられます。
なぜ神経を止めるのか――コノトキシンの作用機序
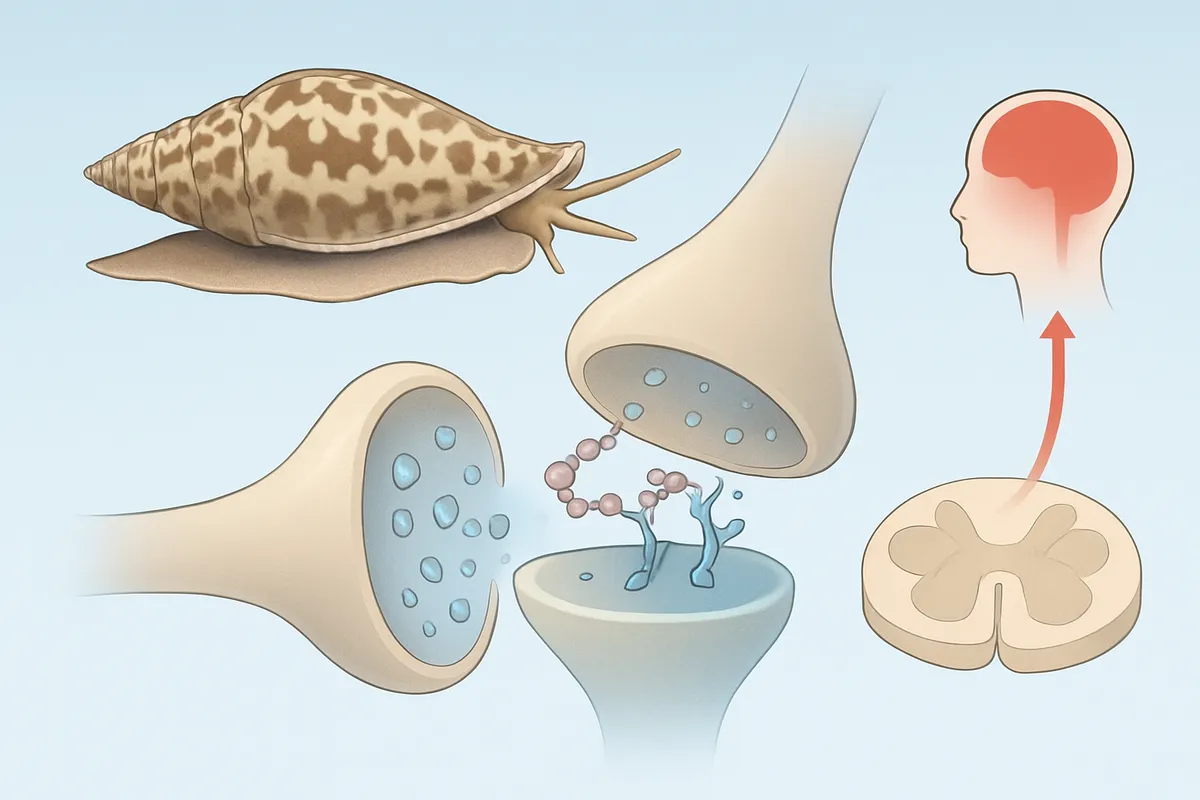
コノトキシンが「神経を止める」理由は、神経系のど真ん中にある分子を、鍵穴を選ぶような精度で狙うからです。
神経細胞の興奮は、Naチャネル、Caチャネル、Kチャネルといったイオンチャネルが開閉し、さらに受容体が化学シグナルを受け取ることで成り立っています。
コノトキシンはその要所のどれかに結合して、活動電位の発生、軸索での伝導、シナプス終末での神経伝達物質放出、筋収縮の引き金といった流れを途中で遮断します。
獲物から見れば「急に動けない」「反応できない」という現象ですが、分子レベルでは神経回路の特定のスイッチが切られているわけです。
ここで面白いのは、イモガイの毒が雑に神経を壊すのではなく、獲物の生理に合わせて標的を切り分けてきた点です。
魚を素早く止める必要がある種では、興奮伝導や神経筋接合部を落とす分子が選ばれやすい。
逆に、別の獲物を狙う系統では別の標的セットが磨かれる。
この「食性に応じた分子標的の最適化」が、コノトキシン群の驚くほど細かい選択性につながっています。
自然選択が積み上げた標的特異性が、そのまま薬理学の道具箱になっている、と考えると全体像がつかみやすくなります。
毒性学やイオンチャネル薬理の現場では、この選択性が実験設計を左右します。
たとえば、ある化合物でシナプス伝達が落ちたとき、それがNaチャネル抑制による伝導停止なのか、CaV2.2遮断による放出抑制なのかで、解釈はまったく変わります。
選択性の低い阻害剤だと、見えている現象が一次作用なのか二次作用なのか判別しにくくなります。
逆に、標的が鋭く切り分けられたコノトキシンを使うと、「どの段で神経回路が止まったか」を明瞭に読めます。
研究現場でデータを読むとき、効いたかどうか以上に、どこにだけ効いたかが価値になります。
コノトキシンはその条件を満たしやすい稀有な分子群です。
代表的ファミリーと標的の対応
一般向けによく出てくる α、μ、δ、κ、ω という呼び分けは、まず「何を主に標的にするか」を整理するための薬理学的なラベルです。
代表例として、α-コノトキシンはニコチン性アセチルコリン受容体、μ-コノトキシンは電位依存性Naチャネル、ω-コノトキシンは電位依存性Caチャネルを狙います。
δ や κ はさらに幅があり、サブタイプによって作用点が分かれます。
δ はNaチャネルの不活性化に影響する群として知られ、κ はKチャネルに作用する群として整理されることが多いものの、コノトキシン全体では例外や細分化も少なくありません。
その中でも、本記事の軸になるのは ω-コノトキシンです。
神経終末ではCaチャネルが開くことでカルシウムが流入し、その流入が神経伝達物質放出の引き金になります。
MVIIAはこの流れの中で、N型電位依存性カルシウムチャネルCaV2.2を遮断します。
すると、脊髄後角での痛覚伝達に関与する神経終末から伝達物質が放出されにくくなり、鎮痛につながります。
毒の文脈では「神経伝達を止める分子」ですが、医薬の文脈では「過剰な痛みシグナルを抑える分子」に反転するわけです。
一方、α-コノトキシンは神経筋接合部や神経系のニコチン性アセチルコリン受容体を切り分けるのに向いています。
受容体サブタイプごとの差が大きい分野なので、どの nAChR を見ているのかを整理するうえで強力です。
μ-コノトキシンはNaチャネルを抑えて興奮伝導の成立そのものを崩します。
活動電位の立ち上がりに関わるので、神経や筋の興奮性を読む実験で意味が明快です。
こうした違いを並べると、コノトキシンの毒性は「強いから怖い」のではなく、「狙う場所が具体的だから怖い」と言ったほうが実態に近いとわかります。
比較すると位置づけが見えやすいので、主要な3群を表にまとめます。
| 項目 | α-コノトキシン | μ-コノトキシン | ω-コノトキシン |
|---|---|---|---|
| 主標的 | ニコチン性アセチルコリン受容体 | 電位依存性Naチャネル | N型などの電位依存性Caチャネル |
| 主な用途文脈 | 神経受容体研究 | 興奮伝導研究 | 鎮痛薬開発・神経伝達研究 |
| 代表例 | ImI, GI | G3B, PIIIA | GVIA, MVIIA, CVID |
| 医薬品化実績 | 承認薬の確認なし | 承認薬の確認なし | MVIIA由来ジコノチドがFDA承認 |
この表で見えてくるのは、ω 群だけが特別というより、研究資産としてはどの群も濃いことです。
ただ、医薬品にまで到達した成功例としてはMVIIA由来のジコノチドが抜けています。
GVIAは研究ツールとして著名で、CVIDは次世代候補として検討されてきましたが、承認薬という意味ではジコノチドが今も象徴的な存在です。
神経科学の研究ツールとしての価値
コノトキシンの価値は、毒としての強さより、分子プローブとしての切れ味にあります。
神経科学では、ある現象を説明するときに「どのチャネルが効いているのか」「どの受容体サブタイプが主役なのか」を分ける必要があります。
そこに高選択的なコノトキシンを入れると、回路のどの部品が寄与しているかを一段ずつ切り分けられます。
GVIAやMVIIAがCaV2.2研究で重用されてきたのはそのためです。
Ca流入を止めたときに伝達物質放出がどう変わるかを見れば、シナプス終末で何が起きているかを直接読めます。
この種の分子は、単に「阻害剤がひとつ増える」という話ではありません。
選択性が高いと、実験結果の解像度が上がります。
研究実務では、ひとつの化合物で現象が止まっても、それだけでは安心できません。
標的外作用が広い薬だと、期待したチャネル以外も同時に叩いてしまい、きれいなストーリーに見える結果ほど危ういことがあります。
コノトキシンのように標的が絞られた分子は、その曖昧さを削ってくれます。
とくに電気生理やシナプス研究では、選択性の高さがそのまま解釈の信頼性になります。
創薬シードとしても同じ構図があります。
病態に関わる標的へ鋭く届く分子は、作用機序の実証に向いています。
ジコノチドはその代表例で、25アミノ酸残基からなるMVIIAをもとにした合成ペプチドです。
脊髄レベルでCaV2.2を遮断し、痛覚伝達物質の放出を抑えるという機序が明快です。
重症慢性疼痛に対する非オピオイド髄腔内鎮痛薬として2005年にFDA承認へ到達した事実は、コノトキシン研究にとって大きな節目です。
もっとも、研究ツールとして優秀なことと、薬として扱いやすいことは別です。
ジコノチドは髄腔内投与が前提で、副作用も軽くありません。
実臨床では少量から慎重に刻む必要があり、投与設計はマイクログラム単位になります。
こういう薬を見ていると、ペプチド薬の世界では「量が少ない=簡単」ではないと痛感します。
むしろ微量だからこそ、設定の荒さがそのまま作用のブレになります。
研究でも臨床でも、標的が鋭い分子ほど、扱う側にも精密さが要求されます。
近年は、こうした資産をConoServerのようなデータベースで集積し、機械学習やバイオインフォマティクスで機能予測につなげる流れも太くなっています。
122種から8,134件のコノペプチドが蓄積されたという規模感は、もはや「珍しい海洋毒を個別に眺める」段階を超えています。
自然界が作った膨大なペプチドライブラリから、どの配列がどの標的へ向かいそうかを先回りして読む時代に入ったということです。
💡 Tip
コノトキシン研究が神経科学で重宝されるのは、神経を止めるからではなく、どの分子を止めた結果なのかを切り分けやすいからです。毒性と研究価値が同じ根を持っている、というのがこの分野の面白さです。
“薬理群”と“遺伝子スーパーファミリー”の違い
コノトキシンを調べ始めた人がつまずきやすいのが、α や ω といった名前と、遺伝子スーパーファミリーの名前が同じ階層に見えてしまう点です。
ここは切り分けておくと理解が急に楽になります。
α、μ、ω などは、基本的には薬理群です。
つまり「何に作用するか」でまとめた呼び方です。
いっぽうで遺伝子スーパーファミリーは、前駆体配列のシグナル配列や配列系統の近さでまとめた分類です。
こちらは「どの家系に属するか」を示します。
同じ薬理群の中に、異なる遺伝子スーパーファミリー由来のペプチドが入ることがありますし、逆に同じスーパーファミリーの中でも作用が枝分かれすることがあります。
つまり、「ωだからこの配列系統」とは限りませんし、「このスーパーファミリーだから必ず同じ標的」とも言えません。
薬理群は機能の地図、スーパーファミリーは進化と配列の地図です。
重なりはありますが、同じものではありません。
この区別が必要になるのは、毒の多様性をどう読むかに関わるからです。
生態学的には、イモガイが獲物ごとに有利な標的を選んで進化してきた結果として、薬理群の多様性が生まれました。
一方で、その材料になったのは遺伝子重複や配列変化を重ねた前駆体遺伝子群です。
進化の履歴を見るならスーパーファミリーが効き、神経回路への作用を見るなら薬理群が効く。
読みたい問いによって使う分類軸が変わるわけです。
研究者同士の会話でも、この二つを混ぜると話が噛み合わなくなります。
標的選択性の議論をしているのに系統名で返すと、機能の話なのか配列の話なのかがぼやける。
逆に、配列進化を議論している場面で薬理群だけを見ていると、なぜ似た作用が別系統から何度も現れるのかを見落とします。
コノトキシンの世界が広く見えるのは、毒だからではなく、機能と進化の二つの分類軸が同時に走っているからです。
ここを押さえると、MVIIAのような個別分子も、単独のスターではなく、進化が作った巨大な分子群の一員として立体的に見えてきます。
鎮痛薬になったのはω-コノトキシンMVIIA

MVIIAの構造とジスルフィド結合
鎮痛薬へつながった主役分子は、Conus magusに由来するω-コノトキシンMVIIAです。
医薬品名で知られるジコノチドは、このMVIIAをそのまま合成した同一配列体で、天然毒素を手本にしたというより、活性本体そのものを医薬品に持ち込んだ例として見るのが正確です。
MVIIAの骨格は、25アミノ酸残基からなる小型ペプチドです。
その中に6個のシステイン残基が組み込まれ、3本のジスルフィド結合を作ることで、立体構造がきれいに固定されます。
コノトキシン全体を見渡すと短いペプチドは珍しくありませんが、MVIIAは「短いのに崩れにくい」代表格です。
配列長だけを見ると小さな分子ですが、システイン配置と架橋の入り方が、標的チャネルに食い込むための形を実質的に規定しています。
ペプチド薬の開発文献を読む際は、まず配列そのものよりも、どのシステインがどこと橋をかけているかに目を向ける。
この構造的な安定化モチーフは、薬としての扱いにも直結します。
分子量はおよそ2.6 kDaと、低分子医薬よりは大きく、ペプチドとしては小ぶりです。
それでも作用量はマイクログラム単位に収まり、連続投与では1日あたりの必要量がナノモル近傍に入る水準です。
ここでは「小さいから単純」ではなく、「小さいが、三次元構造がきっちり決まっているから効く」と捉えたほうが実態に近いです。
CaV2.2遮断と疼痛伝達の抑制
MVIIAが狙うのは、N型電位依存性カルシウムチャネルCaV2.2です。
痛みの情報が脊髄へ入ってくると、一次求心性ニューロンの終末では脱分極に続いてCaV2.2が開き、カルシウムが流入します。
このCa流入が引き金になって、小胞から神経伝達物質が放出されます。
MVIIAはこの入口をふさぐことで、痛み信号の中継そのものを細らせます。
作用部位としてとくに重要なのが脊髄後角です。
一次求心性線維の終末では、CaV2.2依存的にグルタミン酸やサブスタンスPなどが放出され、次のニューロンへ痛覚情報が渡されます。
MVIIAがCaV2.2を選択的に遮断すると、この放出が抑えられ、結果として疼痛伝達が減弱します。
オピオイド受容体を介して回路全体の興奮性を調節する薬と違い、ジコノチドはシナプス前終末のカルシウム流入という、もっと物理的な入口に手をかけるイメージです。
この機序が明快なぶん、投与経路の制約もまた明快です。
MVIIAはペプチド薬なので、血液脳関門を越えて中枢標的へ届かせるには不利です。
全身投与で脊髄後角のCaV2.2を狙う設計には壁があり、そこで臨床では髄腔内投与という形に収れんしました。
作用点まで薬を直接近づける発想です。
ジコノチドが非オピオイド鎮痛薬として独特の位置にあるのは、標的選択性の高さだけでなく、この投与経路まで含めて作用機序に合わせ込まれているからでもあります。
臨床の用量設計を眺めると、この分子の鋭さがよく見えます。
髄腔内持続投与の開始量は0.5〜1.2 μg/day、増量幅は0.5 μg/day以下で、頻度は週1回以下が基本です。
なお、規制文書やレビューでは用量の提示単位がμg/day と μg/h で表記に差があるため、換算例(0.1 μg/h = 2.4 μg/day)を付記しておくと参照が容易です。
こうした数字を追うと、ジコノチドは「効く場所と量の窓が細い薬」であり、投与設計の精密さが重要になります。
ℹ️ Note
臨床用量の表示は文献や規制文書で単位(μg/day と μg/h)が異なることがあるため、本文で示した開始量(0.5–1.2 μg/day)や増量幅は主に臨床レビューおよび規制ラベルを参照した提示です。規制ラベル(FDA)や欧州の SmPC などの一次ソースを確認すると、表示単位や換算の解釈が明確になります(例:FDA ラベル:
GVIA・MVIIA・CVIDの比較表
同じω-コノトキシンでも、GVIAMVIIACVIDは位置づけが異なります。
研究現場でよく名が出るのはGVIA、医薬品へ到達したのがMVIIA、その次を狙う候補として注目されたのがCVIDという並びです。
比較すると、単に「どれもN型Caチャネル阻害剤」では片づかない差が見えてきます。
とくに創薬文献では、選択性と可逆性が、そのまま臨床応用可能性の読み筋になります。
| 項目 | GVIA | MVIIA | CVID |
|---|---|---|---|
| 系統 | ω-コノトキシン | ω-コノトキシン | ω-コノトキシン |
| 由来 | Conus geographus | Conus magus | Conus catus |
| 主標的 | N型Caチャネル | N型Caチャネル(CaV2.2) | 高いN型選択性が注目 |
| 選択性の位置づけ | N型Caチャネル研究の基準分子として著名 | CaV2.2を標的とする医薬品化分子 | 改良候補として選択性の面から注目 |
| 可逆性の位置づけ | 研究ツールとしての使い勝手が中心 | 臨床投与を前提に評価が進んだ | 臨床候補として可逆性改善の文脈で検討 |
| 位置づけ | 研究ツールとして著名 | ジコノチドとして医薬品化 | 次世代候補として検討 |
| 臨床文脈 | 主に研究用途 | 承認薬あり | 開発候補・改良候補 |
この3者を並べると、MVIIAが薬になった理由は一段はっきりします。
GVIAは神経科学の道具としての価値が際立ち、CVIDは改良候補として魅力を持ちながら、最初に承認薬へ届いたのはMVIIAでした。
つまり、創薬では単純な活性の強さだけでなく、選択性、可逆性、投与経路、製剤化の見通しが一体で評価されます。
MVIIAはその総合点で前に出た分子です。
ジコノチドがFDA承認に到達したのは2005年です。
慢性非悪性疼痛のランダム化比較試験では、VASPI低下率が31.2%で、プラセボの6.0%を上回りました。
研究ツールとして育った分子群の中から、特定の配列と立体構造を持つひとつが臨床効果まで証明したわけです。
もっとも、その道筋は「毒の活性をそのまま強みとして押し切った」ものではありません。
ペプチドである以上、血液脳関門と全身投与の壁が残り、そこを髄腔内投与で越える設計が不可欠でした。
次のセクションで扱う投与法と副作用の話は、この構造と機序の延長線上にあります。
2005年、毒が薬になる――ジコノチド承認の意味
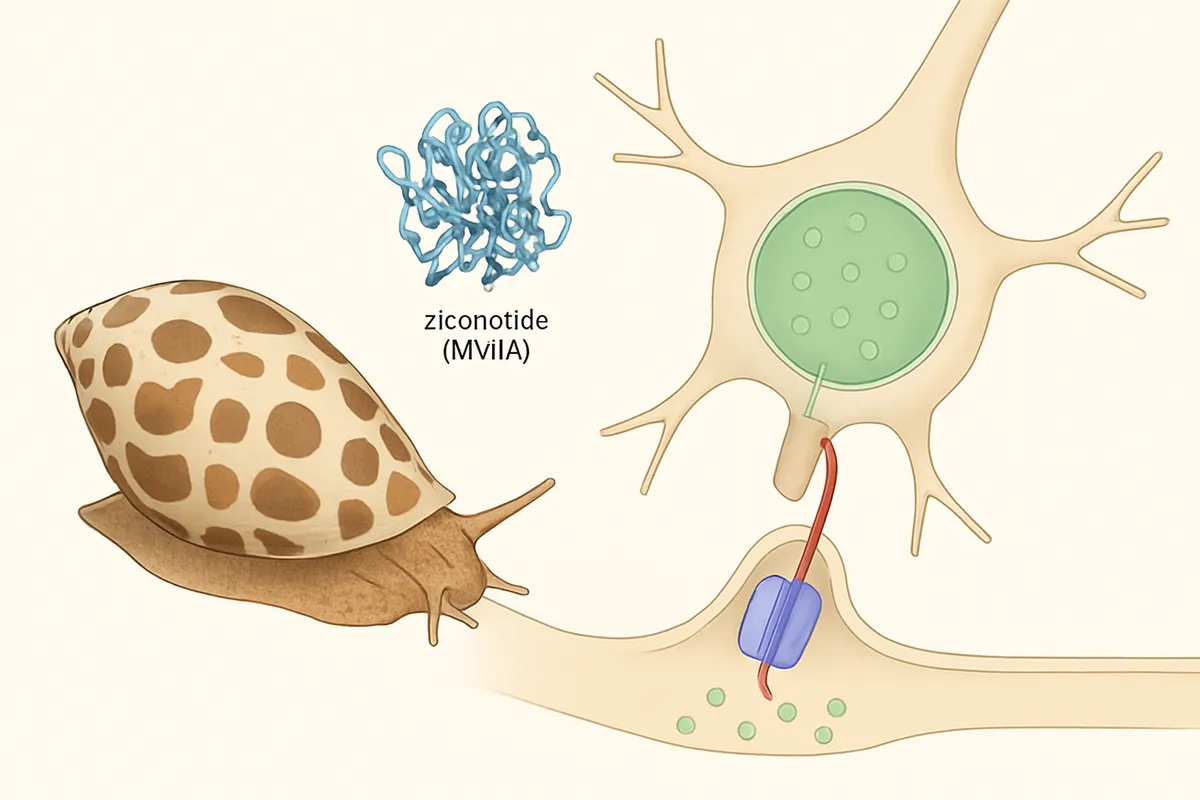
FDA承認(2005年)と適応の整理
ジコノチドが医学史に刻まれたのは、2005年にFDAが承認した時点です。
製品名はPrialt。
適応は、ほかの治療で十分な効果が得られない、あるいは忍容できない重症の慢性疼痛患者に対する髄腔内投与です。
ここでのポイントは、「強い鎮痛薬が一つ増えた」という話ではなく、海産毒ペプチドを起点とする分子が、厳密な投与経路の設計とともに正式な医薬品へ到達したことにあります。
この承認の読みどころは、薬効そのものと同じくらい適応の切り方にあります。
Prialtは経口薬や静注薬の延長として置かれたのではなく、既存治療に抵抗性または不耐の患者に向けた、選択肢の狭い領域で位置づけられました。
実際、開発事例を見ていると、“毒から薬へ”の転換で評価されるのは毒性の弱体化だけではありません。
標的選択性が十分に高いこと、全身曝露を避ける剤形に落とし込めること、そして作用点に届く投与経路が確立できることがそろって、ようやく承認の現実味が出てきます。
ジコノチドはその3点がきれいにかみ合った例です。
このケースを創薬レビューの題材として読むと、承認は分子単体の勝利ではなく標的・製剤・デリバリーの三位一体の設計であると理解できる。
非オピオイド鎮痛薬としての位置づけ
Prialtのもう一つの意義は、非オピオイド鎮痛薬として承認された点です。
従来の強力な鎮痛薬としてまず連想されるのはモルヒネのようなオピオイドですが、ジコノチドの標的はオピオイド受容体ではありません。
狙っているのはN型電位依存性カルシウムチャネルCaV2.2で、脊髄後角のシナプス前終末における神経伝達物質放出を抑えることで痛みの伝達を減らします。
この差は、単なる教科書的な分類以上の意味を持ちます。
オピオイドは受容体作動薬として鎮痛を得る一方、依存や耐性が臨床上の中心課題になります。
ジコノチドでは問題設定がそこからずれます。
依存・耐性の議論をオピオイドと同じ軸で抱え込まない代わりに、髄腔内投与という侵襲的な管理と、神経精神系を含む副作用への別種の注意が前面に出ます。
つまり、非オピオイドであることは「副作用がない」という意味ではなく、ベネフィットとリスクの座標軸が異なるということです。
NSAIDsとも立ち位置は大きく異なります。
NSAIDsはCOX阻害を通じて炎症性疼痛に広く使われますが、難治性の神経障害性疼痛や重症慢性疼痛では限界がある場面があります。
ジコノチドはその延長線上の汎用薬ではなく、既存鎮痛薬で届かなかった痛み回路に、別の分子機序で切り込む薬として現れました。
非オピオイド鎮痛戦略という言葉が抽象論で終わらず、承認薬の形で実装されたという点で、2005年は一つの節目だったと言えます。
⚠️ Warning
ジコノチドの価値は、「オピオイドではない」こと自体よりも、オピオイド受容体を使わずに強力な鎮痛を組み立てたところにあります。依存や耐性の問題を回避しうる設計思想を、実際の承認薬として示した点が新しかったのです。
合成ペプチドとしての医薬品化
科学史の観点でとくに見逃せないのが、ジコノチドがConus magus由来のω-コノトキシンMVIIAの“合成体(同一配列)”として医薬品化されたことです。
イモガイから薬剤を直接採ってきたわけではありません。
天然毒素MVIIAで見いだされた配列と活性を基盤に、同じアミノ酸配列を持つ合成ペプチドとして製造・品質管理できる形にしたのがジコノチドです。
由来は自然毒、製品は合成医薬品。
この関係を正確に押さえると、自然物創薬としての本質が見えてきます。
もともとコノトキシンは短いペプチド群で、MVIIAも25アミノ酸残基からなり、6つのシステイン残基と3本のジスルフィド結合で立体構造を固定しています。
こうした小さなペプチドが、標的チャネルに対して高い選択性を示す。
創薬の目線で見ると、ここに“毒から薬へ”の転換点があります。
乱暴に細胞機能を壊す毒ではなく、特定の分子標的に深く食い込む精密なリガンドだからこそ、投与経路を限定し、用量を細かく刻むことで薬として成立しました。
しかも、ジコノチドはマイクログラム単位で調整される薬です。
こういう製剤を眺めると、ペプチド薬は「大きい分子で扱いにくい」という一般論だけでは語れないと実感します。
分子量は低分子医薬より大きい一方で、薬理作用はきわめて微量で立ち上がるため、臨床ではμg/mLレベルの濃度管理と微細な流量設定がものを言います。
毒素の精密さが、そのまま製剤学と投与設計の精密さへ接続しているわけです。
自然毒ペプチドが、その本体配列を保ったまま承認薬に至る例は多くありません。
その意味でPrialtは、単なる珍しい薬ではなく、天然毒素研究、神経薬理学、ペプチド創薬、難治性疼痛治療が一点で交わった到達点です。
毒を無毒化して薬にしたというより、毒が持っていた標的認識能を、臨床が扱える形へ翻訳した。
この翻訳の成功が、ジコノチド承認の本当の意味です。
強力だが使いやすくはない――臨床使用の現状と限界
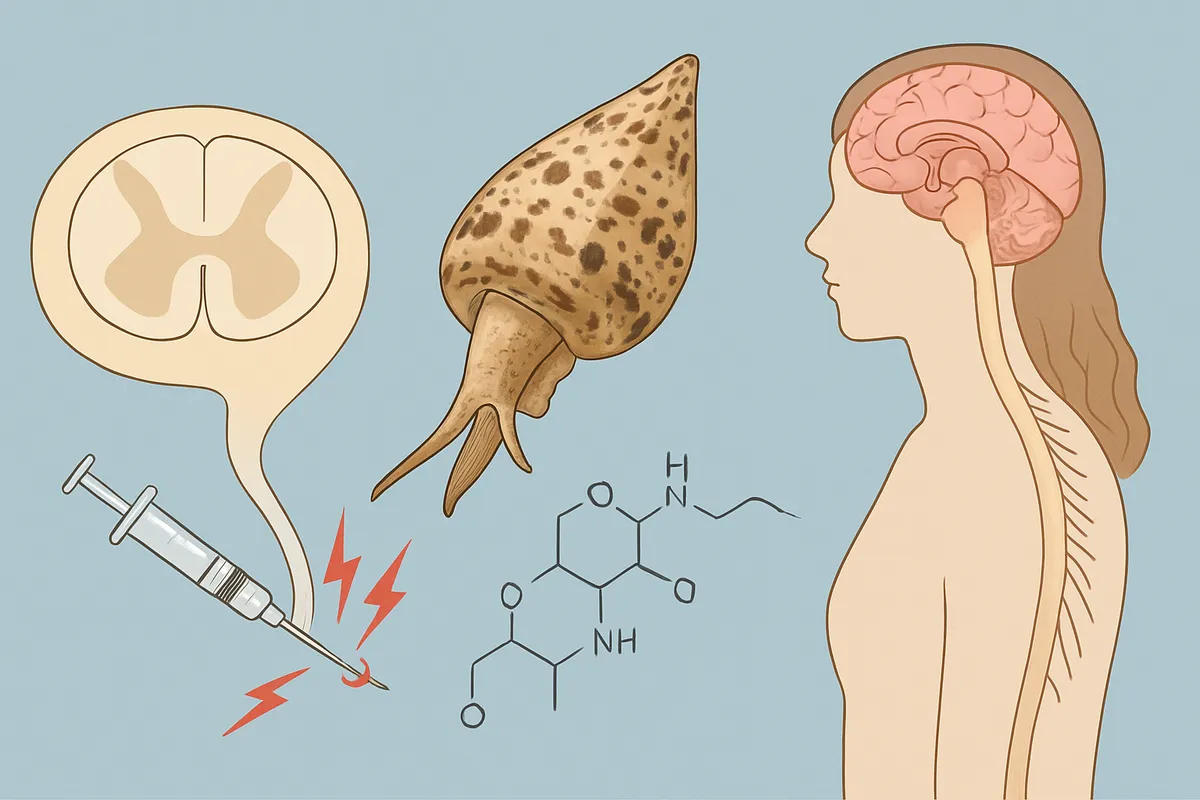
髄腔内投与が選ばれる必然
ジコノチドが強力な鎮痛薬として語られるとき、つい「効く薬なら全身投与で広く使えればよかったのに」と考えたくなります。
ですが、この薬はもともとペプチドであり、しかも標的は脊髄後角にあるCaV2.2です。
血液脳関門を越えにくい分子を、痛み伝達の中枢回路へ届かせたい。
そう考えると、髄腔内投与で標的部位に直接近づける設計は、回り道ではなくむしろ本筋です。
薬の開発経緯を追うと、“強力”と“扱える”は別問題だとわかる。
この合理性はそのまま臨床上の負担にもつながります。
髄腔内投与は、経口薬や一般的な注射薬の延長線上にはありません。
Prialtは髄腔内ポンプによる持続投与を前提に運用され、導入後も細かな流量調整と経過観察が欠かせません。
分子の標的適合性は高くても、運用のハードルが低い薬ではないのです。
ここに、ジコノチドが「切れ味のある薬」でありながら、適応患者が限られやすい現状の理由があります。
有効性エビデンス
有効性は難治性疼痛領域で臨床的意義が示されています。
慢性非悪性疼痛を対象としたランダム化比較試験では、VASPI平均低下率がジコノチド31.2%に対しプラセボ6.0%と報告されています(PubMed 掲載の RCT)。
本記事で示した用量・増量設計の根拠は、FDA の製剤ラベルおよび臨床レビューに基づきます:
副作用プロファイルと“ゆっくり増やす”原則
ジコノチドの副作用プロファイルは中枢神経系・自律神経系にまたがる有害事象が中心で、代表例としてめまい、歩行異常、錯乱、尿閉などが臨床試験や市販後報告で挙げられます。
慢性非悪性疼痛を対象としたランダム化比較試験の結果(VASPI 31.2% vs プラセボ 6.0%)や、用量・増量設計の根拠は一次報告・PubMed 掲載の RCT および FDA 製剤ラベルに記載されています。
用量設計で最も印象的なのは、強い分子を大胆に使う発想ではなく、強いからこそ観察窓を広く取り、増量を遅くするという設計論理である。
💡 Tip
この節で述べているのは、Prialtの承認情報、臨床レビュー、リファレンスに基づく投与設計と安全性の整理です。個別症例への医療判断を示すものではなく、臨床現場での実際の適用は施設運用と規制文書に沿って組み立てられます。
実際、髄腔内ポンプの管理を前提に、少量から時間をかけて漸増し、神経精神症状も含めて追うとなると、誰にでも同じように導入できる治療ではありません。
ジコノチドは、毒由来創薬の成功例として象徴的である一方、鋭い分子を臨床へ翻訳した代償として、運用側に高い精度を要求する薬でもあります。
その意味で、この薬の価値は「万能の強鎮痛薬」ではなく、条件がそろった場面でこそ力を発揮する、きわめて専門性の高い選択肢にあります。
次世代コノトキシン創薬はどこへ向かうか
新規ペプチドと標的の多様化
次世代コノトキシン創薬の焦点は、単にMVIIAの後継を探すことではありません。
どの標的を、どの程度の強さと可逆性で抑え、どの投与設計なら臨床で扱えるかという、設計条件そのものが広がっています。
創薬実務の目線で整理すると、ここは標的選択性×投与設計×製剤の三位一体で見ないと全体像を外します。
標的だけが美しくても、届かず、持続せず、安全域も確保できなければ候補化は進みません。
逆に、分子単体の“切れ味”が少し落ちても、投与経路と製剤で臨床価値が立ち上がることがあります。
その文脈でよく名前が挙がるのが、ω-コノトキシン系のCVIDです。
CVIDはN型カルシウムチャネルに対する高い選択性が注目されてきた分子で、GVIAMVIIAに続く改良候補として位置づけられています。
狙いは明快で、CaV2.2を中心に抑えつつ、余計な標的への作用を減らし、薬効と副作用の距離を少しでも広げることです。
コノトキシン創薬では、この「どれだけ強く効くか」より「どこにどれだけ外さず当てるか」のほうが、むしろ後半戦の勝負になります。
次世代候補はω系だけではありません。
α-コノトキシン由来のRgIA系、なかでもRgIA4は、ヒトα9α10ニコチン性アセチルコリン受容体を高選択的に狙う設計として存在感があります。
ここが面白いのは、鎮痛をCaV2.2遮断一辺倒で考えない流れが強まっていることです。
神経障害性疼痛や化学療法誘発性ニューロパチーのように、疼痛回路の入力点が一様ではない領域では、受容体サブタイプの違いを踏まえた別ルートの介入に意味が出てきます。
RgIA4は前臨床段階ながら、標的の選び方そのものを更新した候補と言えます。
ここで明記しておきたいのは、コノトキシン候補を語るときに見かける「モルヒネの100〜1000倍」といった単純比較は採りません、という立場です。
投与経路も薬力学も到達部位も異なる薬を、数字だけで横並びにすると、薬効の実像より誤解のほうが大きくなります。
次世代創薬で問われているのは、派手な倍率ではなく、標的に対する選択性、作用の可逆性、そして臨床運用へ落とし込める設計かどうかです。
投与経路と製剤設計
ジコノチドが示したのは、優れたペプチドでも投与経路の壁は別問題だという事実でした。
次世代候補でも、最大の障害のひとつはやはり血液脳関門(BBB)です。
ペプチドは全身投与で中枢へ届きにくく、届かせようとすると今度は全身側の安全性が問題になります。
そのため開発は二つの方向に分かれます。
ひとつは中枢へ届けるための送達技術を磨く方向、もうひとつは末梢標的化によって、そもそもBBB通過を必須条件にしない方向です。
このとき分子設計で外せないのが、可逆性と選択性の最適化です。
標的に強く張り付くことは魅力ですが、臨床では“切れ味が鋭い”だけでは足りません。
効きすぎたときに引き返せるか、意図しない標的を巻き込まないか、全身投与に拡張したとき安全域を保てるかが問われます。
私自身、候補分子を評価するときは、活性値だけではなく、作用部位への到達性、オフターゲットの幅、製剤化したときの投与再現性まで並べて見ます。
コノトキシンは小型ペプチドで、全体としてはおおむね10〜30残基の設計空間にありますが、この短い配列のなかで標的親和性、安定性、可逆性を同時に詰め込まなければならない。
ここに難しさと面白さが同居しています。
候補分子の評価では、活性値だけではなく、作用部位への到達性、オフターゲットの幅、製剤化したときの投与再現性まで並べて検討する。
製剤学の側面でも、日本では動きが見えています。
2021年度から2025年度にかけて、科研費で「ω-コノトキシンを用いた新しい鎮痛徐放製剤の開発」が進められました。
これは、コノトキシン創薬のボトルネックが分子発見だけではなく、どう放出を制御し、どう局所濃度を保ち、どう投与負担を下げるかに移っていることをよく示しています。
創薬の現場では、分子の発見が前半、製剤設計が後半というきれいな分業にはなりません。
候補選定の時点から、「この分子はどの剤形なら生きるか」を一緒に考える必要があります。
ℹ️ Note
次世代コノトキシンの評価軸は、標的適合性だけで決まりません。選択性で標的を絞り、投与設計で届け方を定め、製剤で放出と安全域を整える。この三層が噛み合って初めて、毒由来分子は“研究上の有望株”から“開発候補”へ進みます。
中枢移行を無理に追わず、末梢の痛覚回路や炎症関連シグナルに焦点を当てる発想も、今後の重要な流れです。
BBBを越えること自体が開発難度を押し上げる以上、末梢で意味のある標的を選べるなら、全身投与の設計自由度は上がります。
ここでもRgIA4のような非CaV2.2系の候補は、単なる標的の“横展開”ではなく、投与法の選択肢まで広げる存在になっています。
AIとバイオインフォマティクスが拓く設計空間
次の変化は、探索のやり方そのものです。
コノトキシンは配列が短く、しかもジスルフィド結合や翻訳後修飾の影響が大きいため、昔は一つひとつ実験的に当たりをつける色合いが濃い領域でした。
いまはその前段で、配列から機能を予測し、標的候補や改変方針を絞り込む流れが強まっています。
2024年から2025年にかけてのレビューでは、機械学習とバイオインフォマティクスを使って、コノペプチドの分類、活性予測、標的推定、最適化候補の抽出までを一続きの設計工程として扱う考え方が前面に出ています。
この潮流を支えているのが、ConoServerのような学術データベースです。
コノペプチドの配列、遺伝子情報、立体構造、注釈を束ねた基盤があることで、未知配列を既知ファミリーに照らし、どのシステイン配置がどの標的に結びつきやすいかを比較できます。
2022年時点で、ここには122種由来の8,134件のコノペプチドが蓄積されているという整理があり、探索母集団はすでに人手で直感的に眺められる範囲を超えています。
ここまで候補が広がると、AIは“流行の飾り”ではなく、探索空間を現実的なサイズに圧縮する道具になります。
しかも、AIが役立つのは新規配列探索だけではありません。
既知分子のどの残基を置換すれば選択性が上がるか、どこを変えると可逆性や安定性に影響するか、製剤化を見据えた改変でどの程度薬理を保てるかという、開発後半の問いにも向いています。
MVIIAが医薬品になったあとに必要なのは、同じ分子を称賛し続けることではなく、どの設計原理が次の候補にも転用できるかを抽出することです。
CVIDやRgIA4が象徴しているのは、自然毒をそのまま借りる段階から、自然毒を設計テンプレートとして使う段階への移行です。
日本の研究動向を見ても、この変化は分子探索だけに閉じていません。
徐放製剤のような製剤学、配列情報を扱う情報科学、標的薬理を詰める神経科学が少しずつ接続されつつあります。
コノトキシン創薬の次章は、海洋天然物を“珍しい毒”として掘り出す競争ではなく、配列データ、標的選択性、送達技術を一体で最適化する総合設計の競争になるはずです。
そこで勝つ候補は、最も強い毒ではなく、最もよく設計されたペプチドです。
毒と薬の境界をどう見るか

毒性学の文脈で「紙一重」という表現を用いる場合は、量の差だけでなく、標的の絞り込みとドラッグデリバリーの工夫まで含めて考える必要がある。
MVIIAからジコノチドへ至る流れは、その現実を端的に示しました。
強い作用を持つことと、治療として扱えることは同義ではないということです。
むしろ創薬の本質は、強力な分子を見つけることより、その力をCaV2.2という標的選択性に結びつけ、さらに髄腔内投与という経路設計で成立させた点にあります。
毒を薄めて薬にしたのではなく、狙いを絞り、届く場所を設計し、はじめて薬理作用を治療へ翻訳したわけです。
この視点で読むと、海の毒の物語は珍しい天然物の逸話では終わりません。
次に注目したいのは、別の毒由来医薬品が何を標的に選び、どう届け方を工夫して臨床へ橋を架けたのか、あるいは神経毒がどの回路をどう遮断して症状を変えるのかという設計の比較です。
毒と薬は紙一重ですが、その一線は偶然ではなく、分子標的の選択性と投与経路設計によって引き直されています。
薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
毒から薬へ|毒性のある物質が医薬品になる条件
毒はなぜ薬になりうるのか。この問いに答える鍵は、毒=悪、薬=善という単純な線引きではなく、用量・投与経路・標的選択性・規制という4つの条件にあります。非臨床安全性研究で用量反応曲線を組むとき、初期毒性兆候をどこで拾い、どの投与量をNOAELやLOAELとして切るかを詰める作業そのものが、
ボツリヌス毒素からボトックスへ|最強の毒が美容医療を変えた
ボツリヌス毒素は「最強の毒」とだけ語ると、本質を見失います。毒性学の実務でまず見るのは、何mgかではなく、どこに、どれだけ、どの経路で入るかという三つで、全身に回る中毒と、医師が局所へごく微量を打つ医療は、同じ物質でも意味がまるで変わります。 ボツリヌス毒素は毒と薬という二面性を持つ分子です。
トリカブトと漢方の附子|毒が薬になるまで
山菜と見分けを誤れば命に関わるトリカブトは、塊根を加工し、規格の中で管理すると、生薬附子(ブシ)として医療の現場に入ってきます。この記事は、毒草としての植物が、どうやって処方に組み込まれる医薬の素材へ変わるのかを知りたい人に向けて、その道筋を一本の線でたどるものです。
ジギタリスの物語|毒から薬、そして再評価
花壇では優美に見えるジギタリスは、ひとたび体内に入れば心臓に触れる毒でもあります。その危うい植物が、18世紀の観察医学から現代の薬理学へどう橋を架け、心不全治療の景色をどう変えたのかを追うのが本稿です。