神経毒の仕組み|シナプス遮断の分子機構
神経毒の仕組み|シナプス遮断の分子機構
大学の薬理の実習や授業で何度も見る、あの「正常なシナプス伝達の一枚図」を思い浮かべると、神経毒の整理は一気に進みます。この記事ではその基本図を土台に、どこで信号が止まるのかを軸索伝導、シナプス前、シナプス後の3か所に分け、代表毒素の差分を重ねる形で図示しながら追っていきます。
大学の薬理の実習や授業で何度も見る、あの「正常なシナプス伝達の一枚図」を思い浮かべると、神経毒の整理は一気に進みます。
この記事ではその基本図を土台に、どこで信号が止まるのかを軸索伝導、シナプス前、シナプス後の3か所に分け、代表毒素の差分を重ねる形で図示しながら追っていきます。
同じ「神経毒」でも、TTXはNa+チャネルを塞いで活動電位そのものを止め、BoNTはSNAREを切って放出を止め、α-ブンガロトキシンはnAChRを塞いで受容を止めます。
さらにTeNTは同じSNARE切断でも抑制性介在ニューロンを狙うため、回路の出力は正反対に振れます。
神経毒の面白さは、毒性の強さだけではありません。
チャネル生理学、シナプス小胞融合、受容体薬理学、さらにはボトックスに代表される治療応用まで、神経科学の核心はしばしば毒素によって輪郭を与えられてきました。
読み終えるころには、作用点と分子標的を対応づけて、自分の言葉で言い切れるところまで整理できます。
神経毒はどこで神経伝達を止めるのか

作用点の三分法
神経毒が神経伝達をどこで止めるのかを見分けるには、まず正常な流れを一本の線として置くと座標が定まります。
活動電位が軸索を伝わって神経終末に到達し、そこで電位依存性Ca2+チャネルが開き、流入したCa2+を合図にSNAREタンパク質群が小胞融合を進め、放出された神経伝達物質がシナプス間隙を拡散し、シナプス後膜の受容体を活性化する。
この流れのどこを断つかで、神経毒は大きく三つに分けられます。
第一は軸索伝導遮断です。
ここでは活動電位そのものが先へ進めなくなります。
代表例はTTXで、電位依存性Na+チャネルを選択的に塞ぎ、興奮の発生と伝導を止めます。
つまり、シナプスに着く前の段階で電気信号が途切れる型です。
第二はシナプス前遮断です。
活動電位は終末まで来ているのに、伝達物質を外へ出せません。
BoNTはこの典型で、神経終末に取り込まれた後、軽鎖が細胞質へ移ってSNAREタンパク質を切断し、小胞融合を止めます。
TeNTも同じくSNAREの一種であるVAMP/シナプトブレビンを切断しますが、到達する回路が異なります。
BoNTが末梢のコリン作動性終末でアセチルコリン放出を落とすのに対し、TeNTは神経筋接合部から取り込まれて逆行輸送され、脊髄の抑制性介在ニューロンで抑制性伝達を止めます。
この回路差が、弛緩と痙性という対照的な病像を生みます。
補助例としてω-コノトキシンGVIAもここに入ります。
こちらはSNAREを切るのではなく、神経終末のN型Ca2+チャネルを阻害して、放出の引き金になるCa2+流入を断ちます。
第三はシナプス後遮断です。
伝達物質が放出されても、受け手が応答できません。
α-ブンガロトキシンは神経筋接合部のニコチン性アセチルコリン受容体に強く結合し、アセチルコリンが受容体を活性化できない状態をつくります。
電気信号は届き、放出も起きているのに、受容の扉だけが閉じているわけです。
この三分法の利点は、症状の違いを分子標的から逆算できる点にあります。
軸索で止まれば信号そのものが届かず、シナプス前で止まれば放出が消え、シナプス後で止まれば受容だけが失われる。
同じ「麻痺」という言葉でくくられがちな現象でも、止まっている場所は一致しません。
20 nmのシナプス間隙と分子イベント
神経伝達を実感としてつかむとき、私が授業や解説でよく使う物差しが約20 nmのシナプス間隙です。
電子顕微鏡像で神経終末とシナプス後膜のあいだに見える、あの細いすき間です。
図では広く描かれがちですが、実寸は分子が数個並ぶだけで景色が変わるほどのスケールしかありません。
この幅を頭に入れると、神経毒が止めているのは「ふわっとした神経の働き」ではなく、膜表面で起こるきわめて具体的な分子イベントだと見えてきます。
活動電位が終末に到達すると、膜電位の変化に応じて電位依存性Ca2+チャネルが開きます。
ここで入ってきたCa2+が引き金となり、シナプス小胞はSNARE複合体を介して終末膜と融合し、内部の神経伝達物質を放出します。
放出された分子は20 nmの間隙を横切って拡散し、向かい側の受容体に結合して、シナプス後細胞のイオン透過や膜電位を変えます。
教科書では数段階に分けて描かれる一連の過程ですが、現場ではこの距離の中で連続的に進んでいます。
ここに毒素を重ねると、標的の位置関係が立体的になります。
TTXはこの20 nmの手前、軸索膜のNa+チャネルを塞いで活動電位を終末まで到達させません。
ω-コノトキシンGVIAは終末膜のCa2+チャネルに作用し、放出の引き金を失わせます。
BoNTとTeNTはさらに一歩内側に入り込み、SNAREという融合装置そのものを切断します。
α-ブンガロトキシンは20 nmを渡って届いたアセチルコリンの行き先、すなわちシナプス後膜の受容体を占拠します。
この見方をすると、毒素は「神経を止める一括ボタン」ではありません。
チャネルを閉じるもの、融合装置を切るもの、受容体を塞ぐものがあり、止まる瞬間も場所も異なります。
電子顕微鏡像で見える終末、小胞、間隙、後膜の配置を頭に置いたまま読むと、各毒素の説明が図から浮き上がってきます。
ℹ️ Note
シナプス間隙の約20 nmを基準にすると、軸索膜、終末膜、小胞、受容体という配置が一枚の模式図に収まり、TTXBoNTTeNTα-ブンガロトキシンの違いを位置情報として記憶できます。
なお、神経筋接合部のようなシナプス後遮断では、受容体を少し塞いだだけで直ちに伝達が消えるわけではありません(いわゆる受容体予備能)。
受容体予備能の程度はシナプス種や阻害様式によって変動し、一部のレビューでは競合的遮断で約80%の遮断が必要になるとされる場合があるものの、これは概算にすぎません。
本記事の読み方と比較フレーム
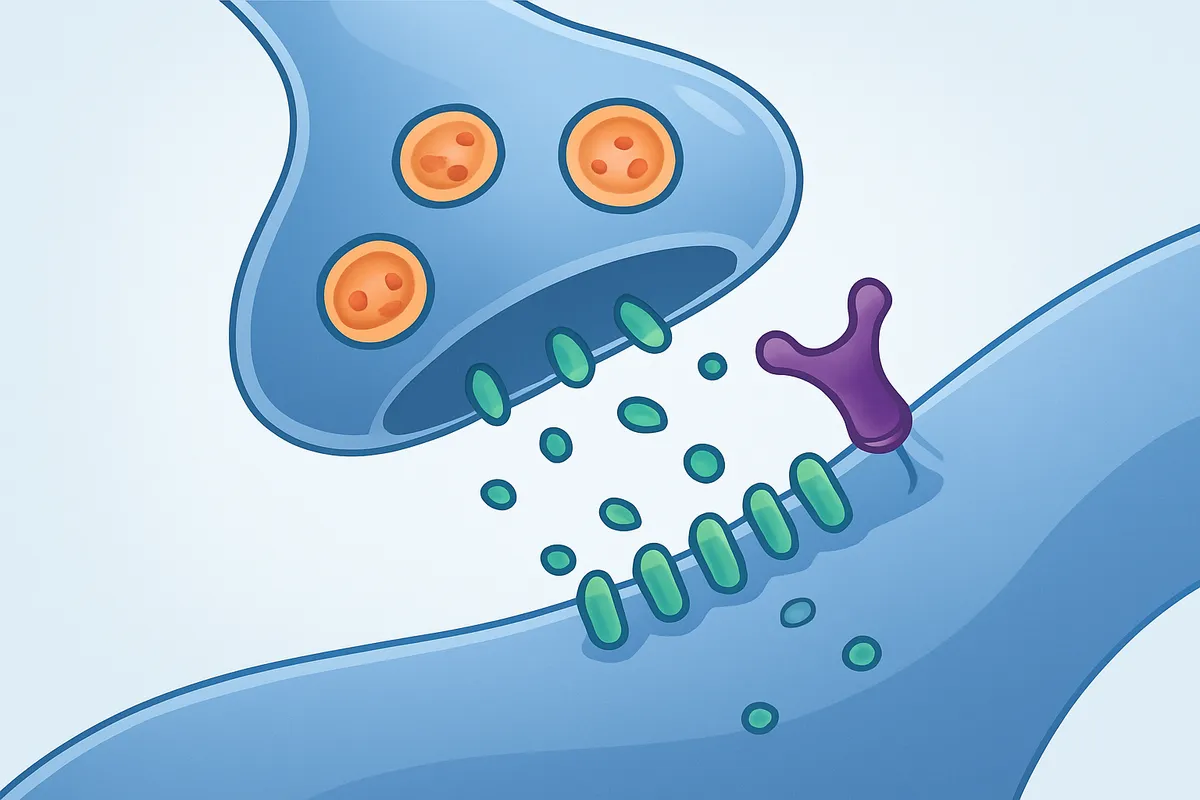
ここから先は、この三分法を比較フレームとして使います。
まずTTXを読むときは、軸索伝導が止まることで活動電位がシナプスまで届かない、という一点に集中すると整理できます。
次にBoNTでは、終末には到達しているのにSNARE切断で放出できない、というシナプス前遮断として読みます。
TeNTでは、同じSNARE切断でも標的回路が抑制性介在ニューロンへ切り替わることで、出力が弛緩ではなく痙性に反転するところが焦点になります。
α-ブンガロトキシンでは、放出までは保たれていて受容だけが止まる、というシナプス後遮断として捉えると混線しません。
この記事のゴールは、毒素ごとの名前を暗記することではなく、作用点、分子標的、回路効果、症状を一列に並べて説明できる状態に持っていくことです。
順番としては、三分法で全体地図をつくり、各代表毒素の分子機構を追い、その後で弛緩性麻痺と痙性麻痺の差を回路レベルで読み解き、そこから研究史や医療応用へ進むと流れが途切れません。
比較の軸を先に固定しておくと、個別の事実も置き場所が定まります。
たとえばTTXは化学式が C11H17N3O8、分子量が319.27の小分子で、Na+チャネル研究の古典的なケミカルツールとして位置づけられます。
一方のBoNTは重鎖約100 kDa、軽鎖約50 kDaからなる約150 kDaの大型タンパク質で、膜融合研究と治療応用の両方にまたがる存在です。
α-ブンガロトキシンは74アミノ酸残基、分子量7983のペプチドで、受容体の標識や解析にも使われてきました。
大きさも化学的な顔つきも異なるのに、どれも神経伝達のどこか一点を精密に止めるという共通項でつながっています。
読み進めるときは、「どこで止めるのか」「何を切る・塞ぐのか」「その結果として回路は静かになるのか、抑制が外れて暴走するのか」の三段で追うと、症状の違いが自然に腑に落ちます。
神経毒の話は怖さだけで語ると輪郭がぼやけますが、20 nmの現場にまで縮尺を下げると、むしろ神経科学の設計図そのものが見えてきます。
シナプス伝達の基礎:電気信号が化学信号に変わる瞬間
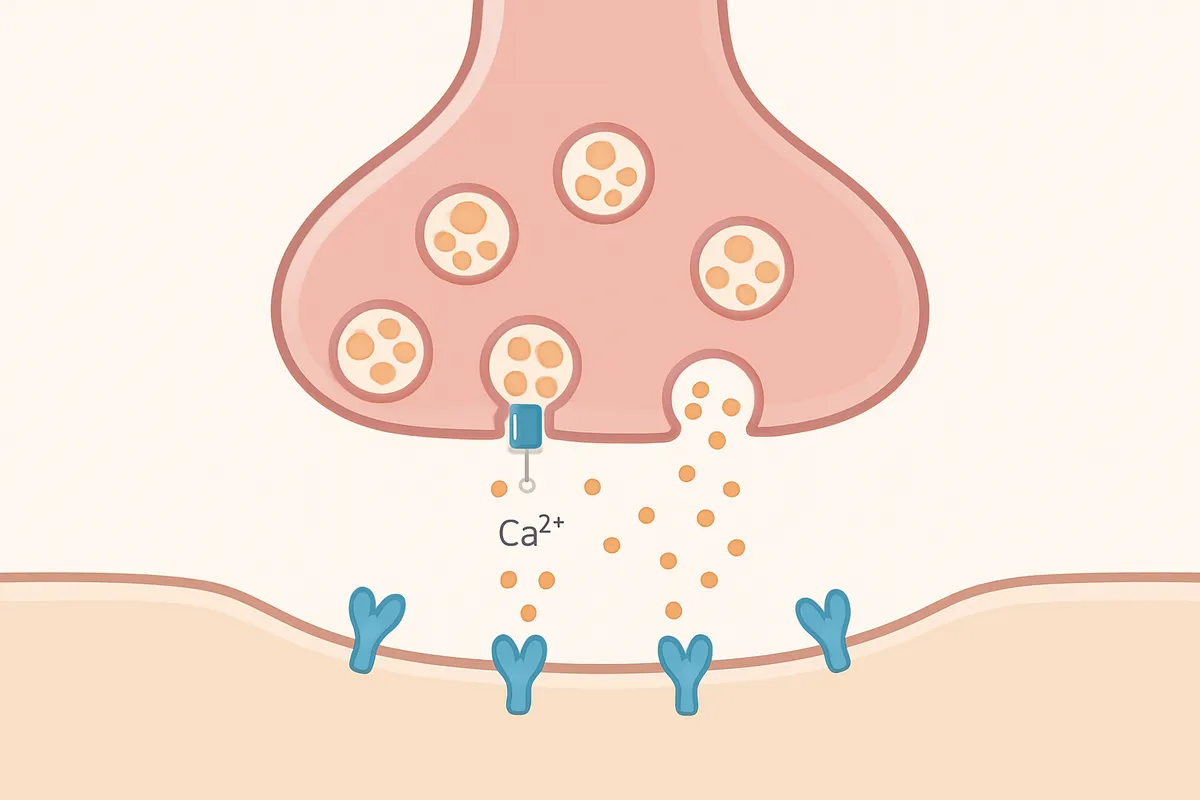
活動電位とCa2+流入
化学シナプスの話は、まず活動電位を一本の電気現象として押さえると見通しが立ちます。
軸索膜では電位依存性Na+チャネルが開いてNa+が流入し、膜電位が急速に立ち上がります。
その後はK+の流出が進んで再分極に向かい、この電位変化が軸索を伝導して神経終末まで届きます。
神経毒を読むときにここが土台になるのは、毒がこの電気信号そのものを止めるのか、終末到達後の放出過程を止めるのかで、病態の意味が変わるからです。
活動電位が神経終末に到達すると、終末膜にある電位依存性Ca2+チャネルが開きます。
神経伝達物質の放出に中心的なのはN型、P/Q型、R型で、終末のごく近い場所にCa2+の高濃度領域が生まれます。
この局所的なCa2+上昇が、小胞融合を引き起こす引き金です。
軸索で走ってきた電気信号が、終末ではCa2+流入という化学放出の合図に翻訳されるわけです。
後で出てくるω-コノトキシンGVIAのような毒は、この翻訳点を狙って放出そのものを弱めます。
小胞とSNARE
神経終末には神経伝達物質を詰めたシナプス小胞が並び、放出の順番待ちをしています。
活動電位だけでは放出は起きず、小胞が膜融合できる状態に組み上がっている必要があります。
その中心がSNARE複合体です。
主要な三者は、終末膜側のシンタキシンとSNAP-25、小胞膜側のVAMP、別名シナプトブレビンです。
これらが噛み合うことで、小胞膜と細胞膜が密着し、融合に向かう力が生まれます。
Ca2+センサーとして働くのがシナプトタグミンです。
終末内にCa2+が流入すると、シナプトタグミンがその変化を拾ってSNARE機構に結びつけ、小胞融合が実行段階に入ります。
授業で模式図を見ると一瞬で終わる出来事に見えますが、実際には「電気信号が来た」だけでは足りず、「融合装置が組まれている」「Ca2+を感知する部品が動く」という二段構えになっています。
だからこそボツリヌス毒素や破傷風毒素のようにSNAREを切断する毒は、活動電位が終末まで到達していても伝達物質を出せなくします。
止まっている場所は電気の発生ではなく、膜融合の実行部です。
受容体とEPSP/IPSP
放出された神経伝達物質は、約20 nmのシナプス間隙を拡散してシナプス後膜の受容体に結合します。
受容体が開くイオンチャネルの向きによって、シナプス後細胞の膜電位は脱分極したり、過分極したりします。
前者が興奮性シナプス後電位、つまりEPSPで、後者が抑制性シナプス後電位、IPSPです。
神経回路はこの足し算と引き算で動いています。
神経筋接合部を例にすると、伝達物質はアセチルコリンで、受容体はニコチン性アセチルコリン受容体です。
ここで生じる電位変化は一般的なニューロン同士のEPSPと同じく脱分極性ですが、筋終板で記録されるので終板電位、EPPと呼びます。
用語は似ていますが、EPSPは広い意味での興奮性シナプス後電位、EPPは神経筋接合部に特化した呼び名です。
この区別を先に入れておくと、後段で受容体毒と放出毒の波形差を読むときに混線しません。
私自身、神経筋接合部の記録例を図にするときは、EPPだけでなくミニチュア終板電流も並べて描くことが多いです。
単発刺激で出る大きな応答と、自発的に1小胞ずつ放出されたときの小さなイベントを同じ座標に置くと、どの毒が「頻度」を落とし、どの毒が「1回あたりの大きさ」を削るのかがひと目で分かれます。
後でBoNTとα-ブンガロトキシンを重ねると、前者は放出側、後者は受容側という差が波形の崩れ方として見えてきます。
神経筋接合部というモデル

神経筋接合部は、シナプス伝達を一連の因果として追うのにもっとも扱いやすいモデルです。
運動ニューロンの活動電位が終末に到達すると、終末膜の電位依存性Ca2+チャネルが開いてCa2+が流入し、それを合図にシナプス小胞がSNARE機構を介して融合し、アセチルコリンが放出されます。
アセチルコリンはシナプス間隙を渡って筋終板のニコチン性アセチルコリン受容体を活性化し、終板電位を生じさせ、筋線維側で活動電位が発生すると収縮へつながります。
刺激から収縮までを一本の鎖として見られるので、Na+チャネル毒、Ca2+チャネル毒、SNARE毒、受容体毒の違いを同じ座標上で比較できます。
生理的前抑制と毒性前遮断の違い
ここで区別しておきたいのが、生理的なシナプス前抑制と、毒によるシナプス前遮断です。
名前は似ていますが、中身は別物です。
生理的前抑制では、たとえばGABA_B受容体を介した調節によって終末のCa2+流入が減り、伝達物質放出の確率が下がります。
これは回路の中で使われる調節機構で、放出をゼロにするというより、利得を絞る働きです。
一方で毒性前遮断は、外因性の分子が放出装置そのものを壊したり、放出に必須の入り口を塞いだりして、病的に伝達を断ちます。
ボツリヌス毒素はSNAREを切断して小胞融合を不能にし、ω-コノトキシンGVIAはN型Ca2+チャネルを阻害して引き金となるCa2+流入を断ちます。
生理的前抑制は神経回路の調律で、毒性前遮断は回路の配線を切る操作に近い、という整理を置いておくと混同しません。
後段でTeNTを読むときも、この区別が効きます。
同じくSNARE切断でも、抑制性介在ニューロンで起きれば、局所の「抑制」が失われた結果として回路全体はむしろ過興奮へ傾くからです。
軸索伝導を止める毒:テトロドトキシンとNa+チャネル遮断

TTXのデータと注意書き
テトロドトキシン(Tetrodotoxin, TTX)は、軸索膜の電位依存性Na+チャネルを標的にして、活動電位の発生と伝導を止める代表的な神経毒です。
化学式は C11H17N3O8、分子量は 319.27 です。
毒性の目安としてマウスのLD50は文献により約8–9 μg/kg(投与経路依存)と報告されることが多く、ヒトの致死量は種差・投与経路・評価法により幅があります(経口で1–2 mgとする推定値が引用される場合もあります)が、これらはあくまで参考値です。
数値を比較する際は必ず「動物種」と「投与経路」を明示してください。
それでもTTXの桁外れの毒性は、分子の小ささを考えると実感しやすくなります。
分子量319.27の化合物で1 mgという量は、分子数に直すと約 1.9×10^18個 に相当します。
質量としては微量でも、分子の数で見れば天文学的な数がNa+チャネルに出会う機会を持つわけです。
毒性学では「少ない重さ」と「少ない分子数」はまったく同義ではない、という感覚がここでよく見えます。
症状の出方も、作用点を知ると腑に落ちます。
TTXはシナプス後受容体を壊すのではなく、末梢神経での伝導を止めるため、知覚異常やしびれが先に出るのが典型です。
運動麻痺は末梢から徐々に進行します。
信号線が順番に沈黙していくイメージ。
この「外から栓をする」という像を持つと、TTXの効果は波形で一気に腑に落ちます。
教育実験で典型的な記録を図にすると、TTXを加えた直後からスパイクが消え、刺激に対して残るのは抑うつした膜電位応答だけになります。
私も授業用の図ではこのトレースをよく示します。
活動電位という鋭い頂点だけがすっと消え、受動的な電位変化の輪郭だけが残るので、「チャネルが一つの部品として抜けた」ことが目で理解できます。
膜そのものが壊れたのではなく、Na+チャネル依存の再生的な立ち上がりだけが失われた、という点がとても鮮明です。
ここで止まるのはシナプス放出の工程ではありません。
軸索を走るはずの電気信号が途中で途絶えるので、神経終末には活動電位が届かず、結果としてCa2+流入も小胞放出も起きません。
見かけ上は「伝達物質が出ない」現象になりますが、故障箇所は終末の放出装置ではなく、その上流の伝導路です。
シナプス前終末を直接壊すBoNTとは、同じ麻痺でも止まっている場所が違います。
単離と構造決定の歴史
TTXの研究史は、神経毒研究と天然物化学の両方で節目になっています。
1909年に田原良純が単離し、テトロドトキシンと命名しました。
フグ毒の本体を一つの化学物質として切り出したこの仕事は、複雑な生物毒の実体を分子として扱う流れを切り開いた出来事でした。
その後、構造の決着には時間がかかります。
1964年に平田義正ら、津田恭介ら、そしてWoodwardらの独立した3グループが構造を決定し、TTXが特異な多官能性骨格を持つ低分子であることが明瞭になりました。
毒性の強烈さに比べると分子量は319.27と小さく、この小さな分子がNa+チャネルを選択的に見分けて強く結合するという事実は、当時の薬理学・有機化学の双方に強い印象を残しました。
この歴史を振り返ると、TTXは「危険な天然毒」であるだけでなく、「作用点が明瞭で、化学としても同定された分子」へと早い時期に移行したことが分かります。
だからこそ、後の生理学で道具として使える土台が整いました。
チャネル生理学への貢献
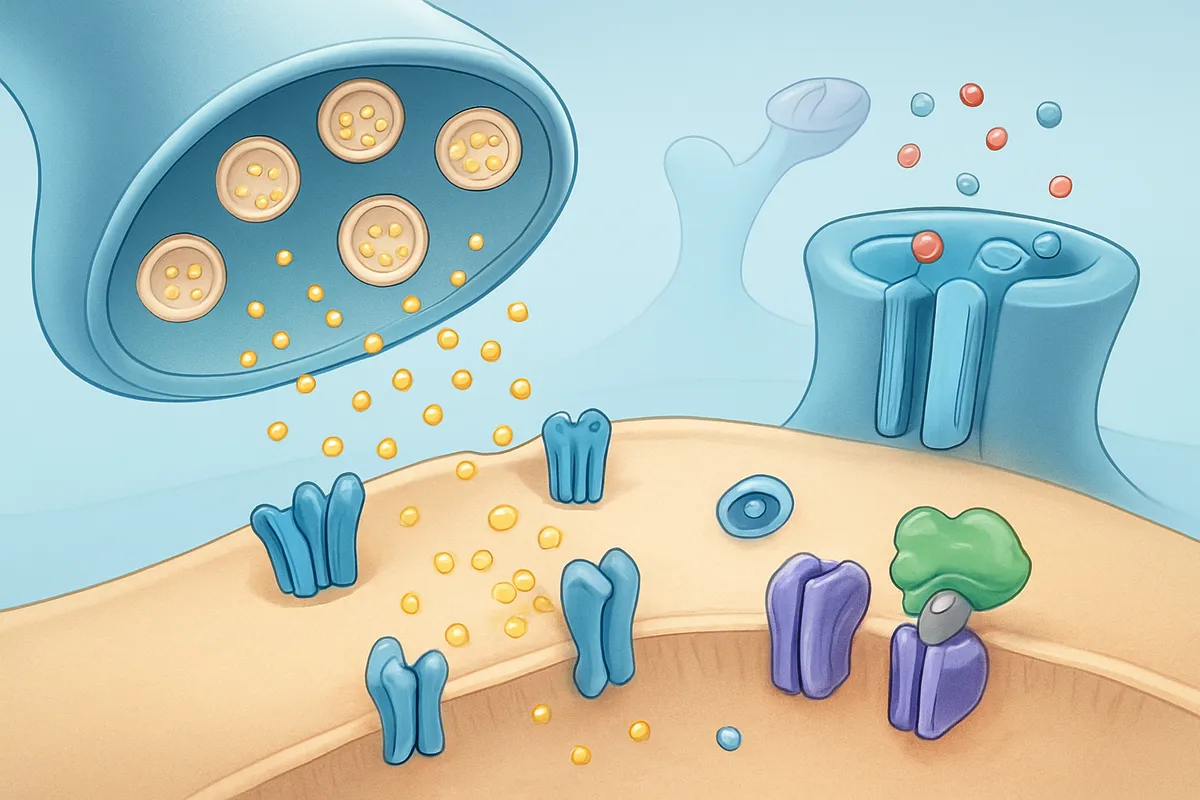
TTXの歴史的価値は、Na+チャネル生理学のchemical toolとして抜群に優れていた点にあります。
神経や筋の電気現象を見ていると、膜電位の変化にはNa+、K+、Ca2+など複数の電流が重なります。
そこでTTXを使うと、Na+チャネル依存成分だけを選択的に引き算できます。
活動電位が消え、残る応答から他の電流や受動特性を読めるようになる。
この切り分けが、電気生理の解像度を一段上げました。
研究の現場では、「TTX感受性か、TTX抵抗性か」という整理そのものがチャネル同定の座標軸になりました。
神経ごと、組織ごとにNaVサブタイプの違いを追う発想も、TTXという選択的遮断薬があったから育った面があります。
単に毒を知る話ではなく、イオンチャネルを実体ある分子として扱う学問の進展に直結していたわけです。
教育面でもTTXは強い力を持っています。
学生に神経毒の違いを説明するとき、私はまず「活動電位が出ない世界」をTTXで見せ、その次に「活動電位は来るのに放出できない世界」をBoNTで示し、「放出はされるのに受け取れない世界」をα-ブンガロトキシンで対比します。
TTXはその最初の座標を与えてくれます。
信号の旅路のどこで切れているのかを、波形と症候の両方でつなげて理解させるうえで、これほど教科書的な分子は多くありません。
シナプス前を止める毒:ボツリヌス毒素と破傷風毒素
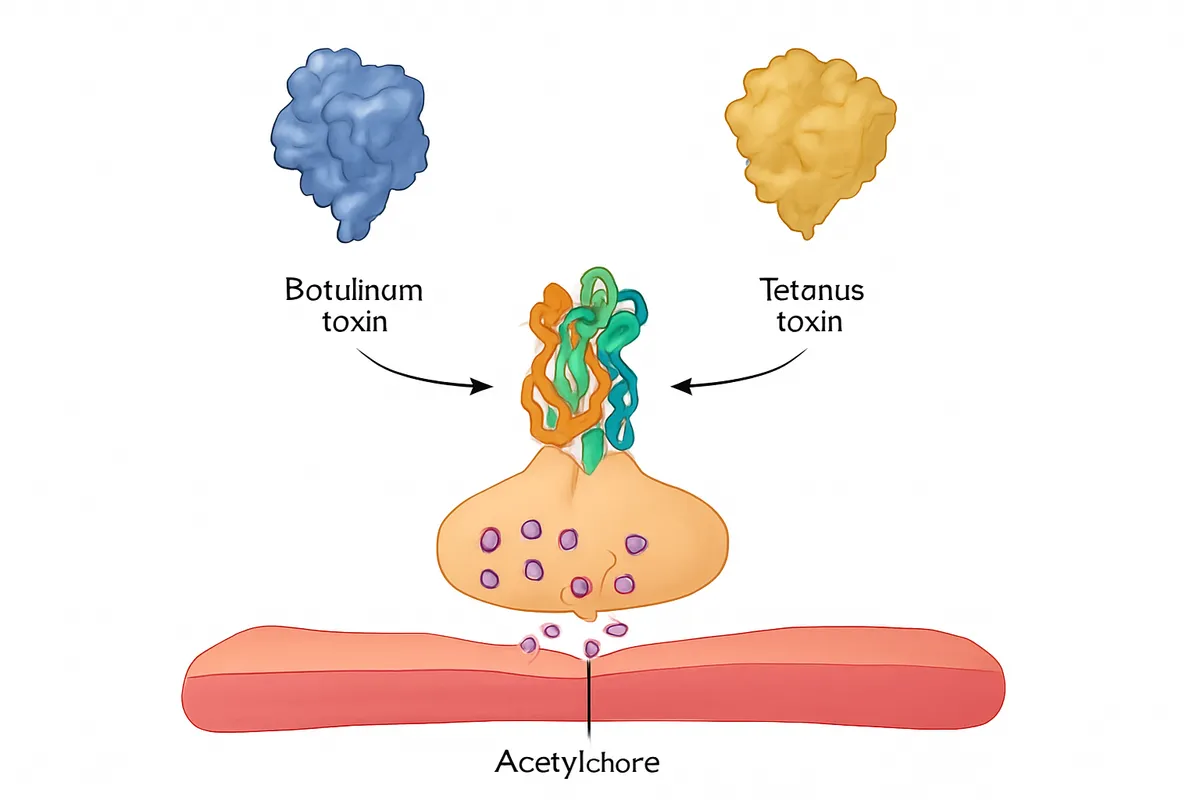
BoNT/TeNTの共通フレーム
ボツリヌス毒素と破傷風毒素は、臨床像だけ見ると正反対です。
前者は筋の力が抜け、後者は筋が張りつめます。
ところが分子レベルまで降りると、両者は驚くほど近縁です。
どちらも神経終末に入り込み、最終的にはSNAREタンパク質を切断して小胞放出を止めるという骨格を共有します。
症状の差は「何を切るか」だけでなく、「どの回路のどの終末に届くか」で決まります。
BoNTは約150 kDaのAB型毒素で、約100 kDaの重鎖と約50 kDaの軽鎖からなります。
重鎖は標的終末への結合と膜移行を担い、軽鎖は細胞質に入ったあとに働く酵素部分です。
軽鎖の本体はZn2+依存性メタロプロテアーゼで、神経伝達物質放出に必要なSNARE群を切断します。
TeNTもこの基本設計と作用原理を共有し、同じ系譜の神経毒として理解すると全体像がつながります。
作用の流れは5段階に整理すると明瞭。
- まず神経終末の膜上で受容体に結合しますよ。
- ついで小胞再取り込みの経路に乗ってエンドサイトーシスされると考えられます。
- 小胞内が酸性化すると、重鎖が膜移行を進め、軽鎖が細胞質側へ出る準備が整いますね。
- その後、重鎖と軽鎖をつないでいたジスルフィド結合が還元され、軽鎖が遊離することになります。
- 遊離した軽鎖がZn2+メタロプロテアーゼとしてSNAREを切断し、小胞融合を止めると考えられます。
この5段階を頭に置くと、「毒がシナプス前終末を止める」とは、膜そのものを破壊することではなく、放出装置の可動部を分解することだと分かります。
活動電位が終末まで到達してCa2+が入ってきても、小胞が膜融合できなければ伝達物質は出ません。
前のセクションで見たTTXが信号線の上流を止める毒だとすれば、BoNTとTeNTは終着点の放出機構を内側から壊す毒です。
BoNT:末梢コリン作動性終末での放出阻害
BoNTの主戦場は、末梢のコリン作動性神経終末です。
とくに神経筋接合部では、運動ニューロン終末からのアセチルコリン放出が落ちることで筋収縮が起きなくなり、弛緩性麻痺が生じます。
活動電位は軸索を伝わって終末まで来ているのに、最後の一押しである小胞融合が成立しないため、筋は命令を受け取れません。
臨床でボトックス製剤が使われる場面を思い浮かべると、この機序はとても具体的です。
眼瞼痙攣の患者さんで、過剰に入っていた筋緊張がほどけ、まぶたの閉じる力の暴走が静まる所見は、まさに末梢コリン作動性終末でACh放出が絞られた結果です。
私はこの所見を説明するとき、回路図を単純化して「運動ニューロン終末から筋へ向かう最後の矢印が細くなる」と表現します。
筋そのものが壊れたわけでも、受容体が消えたわけでもないのに、出力だけが弱まる。
そのため、見た目としては“力が入らない”方向に症状が動きます。
分子機構はSNARE切断で説明できます。
神経終末では、シナプス小胞のVAMP(シナプトブレビン)と、細胞膜側のSNAP-25、シンタキシンが組み合わさって小胞を膜へ引き寄せ、融合直前の状態を作ります。
BoNTの軽鎖はこの複合体の部品を切断し、融合装置を途中で分解します。
Ca2+流入という引き金があっても、機械の歯車が欠けていれば放出は走りません。
ここで見えてくるのは、同じ「麻痺」でも病変の位置で中身が違うということです。
BoNTでは抑制回路が外れるのではなく、筋へ向かう末梢の出力が落ちます。
だから臨床像は、眼輪筋でも頸部筋でも、過緊張していた筋が静まり、表現型としては筋弛緩に寄ります。
分子の仕事はSNARE切断という一点ですが、回路図に置く位置が末梢の最終出力線なので、症候は素直に“出力低下”として現れます。
TeNT:逆行輸送と抑制性介在ニューロン標的
TeNTも末梢神経終末から取り込まれる点ではBoNTと同じです。
違いは、その後の移動経路にあります。
TeNTは末梢で取り込まれたあと、軸索内を逆行輸送され、中枢側へ戻っていきます。
到達先は脊髄などの抑制性介在ニューロン終末で、ここでVAMPを切断し、抑制性伝達物質の放出を止めます。
この一点が、BoNTとの臨床差を決定します。
抑制性介在ニューロンは、運動ニューロンの暴走を抑えるブレーキ役です。
その終末で小胞放出が止まると、GABAやグリシンによる抑制が入らなくなります。
すると運動系は相対的に興奮優位になり、筋は収縮方向へ引っ張られ続けます。
結果として現れるのが痙性麻痺です。
破傷風でみられる閉口や痙笑は、この回路の外し方を知ると一枚の模式図でつながります。
末梢筋そのものが毒で直接縮むわけではありません。
抑制の線が切れ、運動ニューロンにかかっていたブレーキが外れるため、筋への出力が上がり続けるのです。
私はこの対比を説明するとき、ボトックスで見える筋弛緩の所見と、破傷風での顔面筋・咀嚼筋の張りつめた表情を並べて示します。
前者は末梢終末でアクセルが弱くなった像、後者は脊髄回路でブレーキが抜けた像です。
分子レベルではどちらもSNARE切断なのに、回路図のどこに毒が届くかで、体の見え方がここまで反転します。
TeNTの理解では、「同じ放出阻害でも、抑制ニューロンで起きると全身の運動出力は上がる」という回路論が欠かせません。
BoNTとTeNTは分子機構だけ見れば親戚ですが、到達経路と標的ニューロン種が違うため、症候は鏡像のように分かれます。
血清型別のSNARE基質差
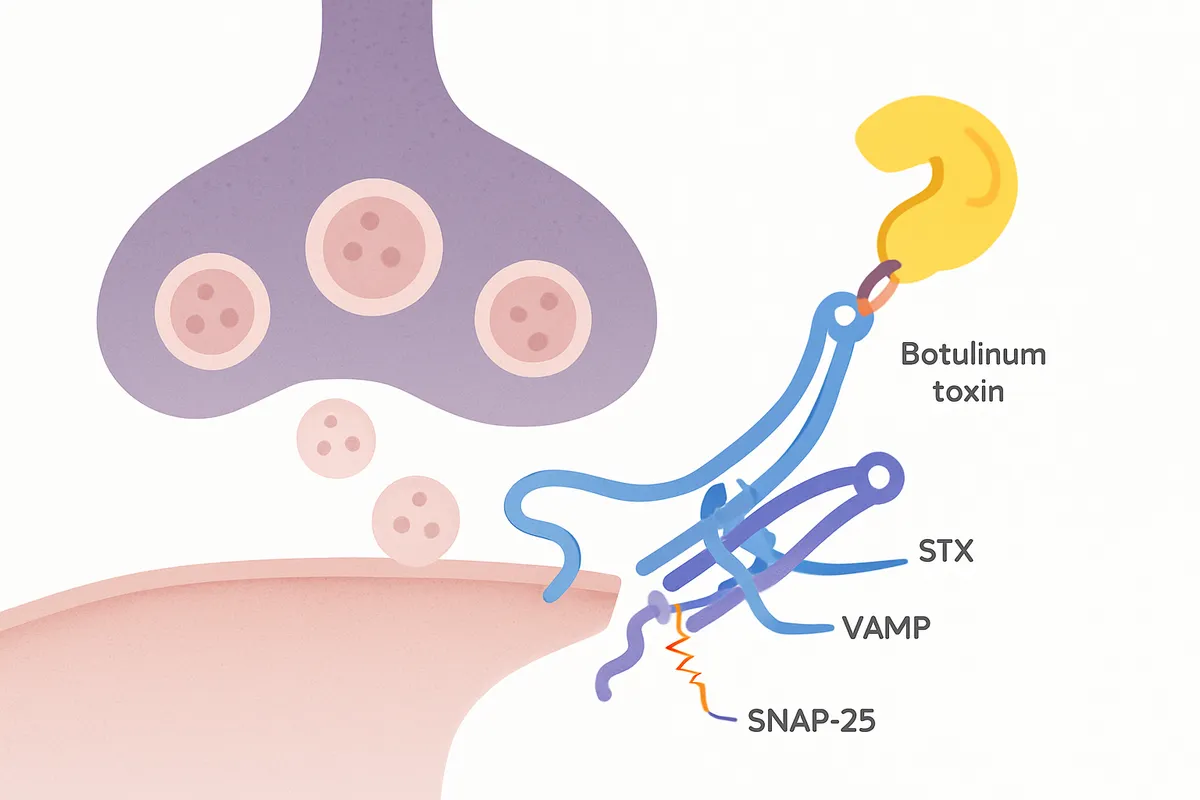
BoNTの血清型は、どのSNAREを切るかで整理できます。
放出阻害という帰結は共通でも、切断標的が異なるため、SNARE研究では血清型そのものが分子解剖の道具になってきました。
整理すると次の通りです。
| 血清型 | 主なSNARE基質 |
|---|---|
| A型 | SNAP-25 |
| E型 | SNAP-25 |
| B型 | VAMP(シナプトブレビン) |
| D型 | VAMP(シナプトブレビン) |
| F型 | VAMP(シナプトブレビン) |
| G型 | VAMP(シナプトブレビン) |
| C型 | SNAP-25 とシンタキシン |
A型とE型はSNAP-25を切断し、B型、D型、F型、G型はVAMPを標的にします。
C型は少し特異で、SNAP-25に加えてシンタキシンも切断します。
つまり、SNARE複合体を構成する三者のうち、どの部品に刃を入れるかが型ごとに違います。
けれども出口は同じで、小胞融合が進まず、神経伝達物質の放出が止まります。
TeNTはこの表でいえばVAMPを切るグループに属する理解でよく、分子の刃先だけ取り出せばBoNTの一部血清型と重なります。
それでも病像が異なるのは、繰り返しになりますが、基質差だけでは症状を説明しきれないからです。
共通項はSNARE切断であり、相違点は到達する回路と標的ニューロンの種類です。
筋を直接動かす末梢コリン作動性終末で放出を止めれば弛緩に向かい、抑制性介在ニューロンで放出を止めれば脱抑制によって痙性に向かう。
BoNTとTeNTは、その回路構造の違いを教科書より鮮やかに見せてくれる分子だと言えます。
シナプス後を止める毒:α-ブンガロトキシンと受容体遮断
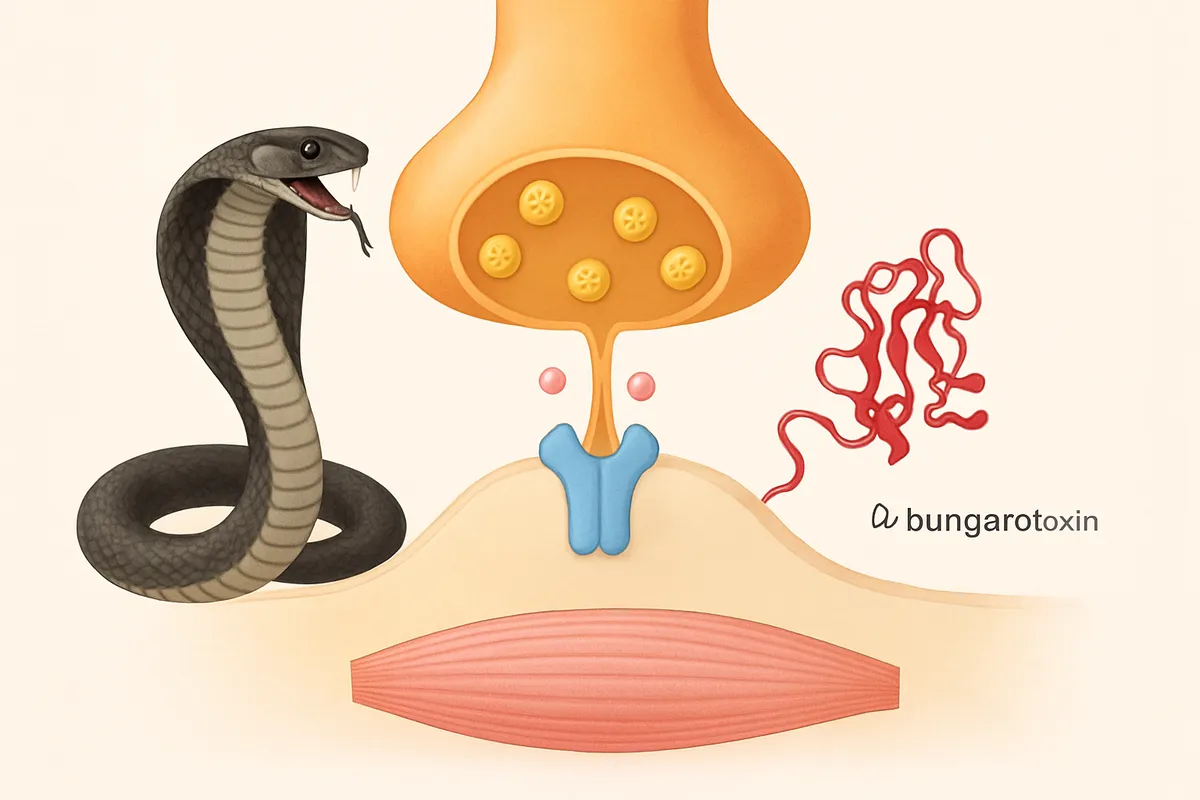
nAChRへの高親和結合
α-ブンガロトキシン(α-BTX)は、74アミノ酸残基からなる分子量7,983のポリペプチド毒で、神経筋接合部のニコチン性アセチルコリン受容体(nAChR)に強固に結合します。
ここで起きていることは、前のセクションで見たBoNTのような「AChが出ない」状態とは別です。
神経終末から伝達物質が放出されていても、受け手側の受容体が塞がれていれば、終板電位は立ち上がれません。
つまり、信号は放たれているのに、受信機のスイッチが押せない状態です。
この位置づけは、古典的にはクラーレ様のシナプス後遮断として整理されます。
クラーレ系薬物と同じく、障害部位は神経筋接合部のシナプス後膜です。
軸索の活動電位伝導が止まるわけでも、シナプス前終末の小胞放出が止まるわけでもありません。
止まるのは、AChがnAChRを活性化して筋線維膜に脱分極を起こす最後の受け渡しです。
私は教育用実習や古典的文献の図を使ってこの点を説明するとき、正常な終板電流の波形の上に、α-BTX投与後の振幅がすっと削られていくイメージを重ねます。
刺激は入っているのに、応答の山だけが細っていく図は、シナプス後遮断を一目で伝えてくれます。
前側の放出装置ではなく、後ろ側の受容体が黙らされているという直感が、その波形にはよく表れます。
神経刺激と筋直接刺激の対照
α-BTXの作用点を実験的に見分けるとき、いちばん鮮やかな対照になるのが、神経刺激では収縮が消えるのに、筋直接刺激では反応が残るという所見です。
運動神経を刺激して筋を動かすには、神経終末からAChが放出され、それが終板のnAChRを開ける必要があります。
ところが受容体がα-BTXで占拠されると、この橋渡しが成立しません。
そのため、神経経由の収縮は途絶えます。
一方で、筋線維そのものを電気刺激すれば、神経筋接合部を迂回して筋膜を直接脱分極できます。
筋の興奮収縮連関が保たれている限り、筋はまだ反応します。
この対照は、病変が筋そのものではなく、神経筋接合部のシナプス後膜にあることを示す診断的な特徴です。
ここは学生実習でも印象に残る場面です。
神経刺激ではぴたりと反応が落ちた標本が、刺激電極を筋側に置き換えると再び収縮を返す。
その切り替わりを見ると、「毒で筋肉が壊れた」のではなく、「神経から筋への受け渡しだけが断たれた」という整理が腑に落ちます。
回路図でいえば、筋はまだ動けるのに、終板という受信部だけが塞がれているわけです。
💡 Tip
神経刺激で反応が消え、筋直接刺激で反応が残る所見は、α-BTXをシナプス後遮断として捉えるうえでの要点です。前シナプス毒との違いは、この切り分けで見えます。
受容体予備能と機能低下のしきい値
神経筋接合部では、受容体が少し塞がれただけで直ちに筋力が落ちるわけではありません。
ここで効いてくるのが受容体予備能(receptor reserve)の考え方です。
終板には、通常の伝達を成立させるのに必要な量を上回る受容体機能が用意されており、ある程度までの遮断なら見かけの伝達は保たれます。
そのため、競合的な受容体遮断では、しきい値が相対的に高い場合があり、文献によっては約80%の遮断が指摘されることもありますが、シナプスの種類や阻害機構に依存して数値は変化するため、あくまで概算として扱うべきです。
この話をするとき、私は「受容体は予備タイヤを一つ積んでいるどころではなく、複数本の余力を抱えた状態で走っている」と表現します。
だから、α-BTXのような遮断薬を加えても、初期には見た目の反応が案外しぶとく残ります。
ところが遮断が進むと、あるところで終板電位が筋線維の活動電位発生に届かなくなり、収縮は急に途切れたように見えます。
教育用の波形でも、なだらかな低下というより、しきい値を割った瞬間に失敗が目立ち始める感じがよく伝わります。
実験ツールとしてのα-BTX
α-BTXは毒であると同時に、nAChR研究を支えてきた実験ツールでもあります。
受容体に高親和で結合する性質のおかげで、神経筋接合部や電気器官のnAChRを同定し、標識し、局在を可視化する道具として長く使われてきました。
放射標識α-BTXは受容体量の評価に、蛍光標識α-BTXは終板の形態観察や受容体クラスターの可視化に向いています。
この用途では、単に「結合する毒」ではなく、「どこに受容体があるかを浮かび上がらせるプローブ」としての価値が際立ちます。
nAChR研究の歴史をたどると、受容体という見えにくい存在を、α-BTXが輪郭のある対象へ変えてきたことがわかります。
薬理学で毒が道具へ反転する典型例の一つです。
私自身、終板を蛍光像として眺める説明では、α-BTXはただ伝達を止める分子ではなく、神経筋接合部の設計図を読ませてくれる分子だと感じます。
TTXが軸索膜のNa+チャネル研究を押し進め、BoNTが小胞融合機構の理解を切り開いたのと同じように、α-BTXはシナプス後膜の受容体生物学を具体像として見せてきました。
毒の本質は遮断ですが、研究の現場ではその選択性こそが武器になります。
同じ麻痺でもなぜ違うのか:弛緩性と痙性を分ける回路
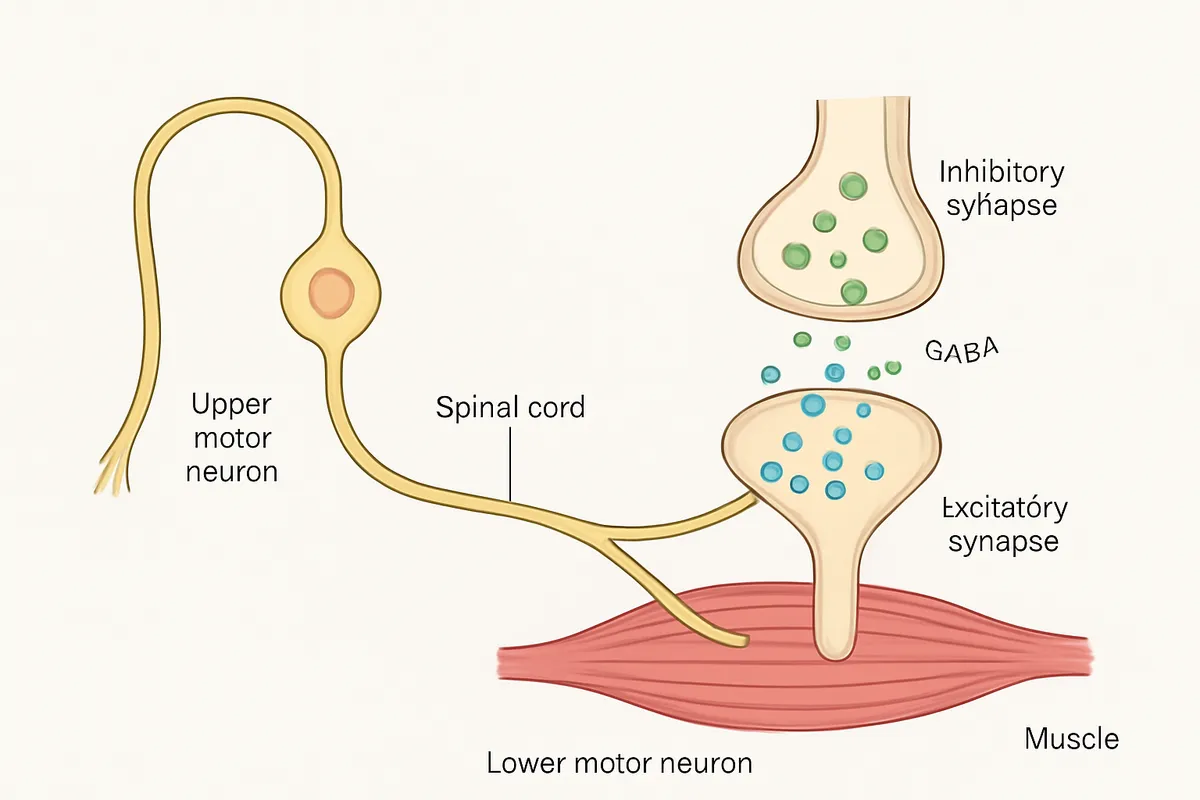
弛緩性麻痺と痙性麻痺の回路理解
同じ「麻痺」という言葉でも、回路のどこが切られたかで身体所見は別物になります。
ここを一枚の回路図として並べると、暗記項目だった毒素の違いが一気につながります。
運動ニューロンが筋へ命令を渡す末梢の神経筋接合部でアセチルコリン放出が止まれば、筋は指令そのものを受け取れず、筋トーンは落ち、腱反射も弱くなる方向へ傾きます。
これがBoNTで見る弛緩性麻痺です。
障害部位は末梢コリン作動性終末で、運動出力の最後の一押しが消えている状態です。
一方のTeNTは、同じSNARE切断毒素でも回路上の意味が逆転します。
破傷風毒素は末梢から取り込まれたあと逆行輸送され、脊髄の抑制性介在ニューロンで伝達を止めます。
すると本来は運動ニューロンにかかっていたブレーキが外れ、運動ニューロンが興奮側へ傾きます。
筋へ行く最終出力は残るどころか抑えが利かなくなるので、筋トーン上昇、反射亢進、こわばりや有痛性けいれんを伴う痙性麻痺の像になります。
BoNTとTeNTは分子レベルでは近縁でも、どのニューロンを黙らせるかで臨床像が反転するわけです。
TTXはさらに別系統です。
これは電位依存性Na+チャネルを塞ぎ、活動電位の発生と伝導そのものを遮断します。
つまり「放出装置」や「受容体の門」より前で、配線に流れる電気信号自体が途切れます。
筋への運動出力も落ちますが、感覚・自律系を含む伝導全般が巻き込まれる点がBoNTやTeNTと異なります。
回路の比喩でいえば、BoNTは終末の放出レバーを固定し、α-BTXは受容体側のドアノブを塞ぎ、TTXは配線に電流が流れないようにする毒です。
この整理を講義や執筆で示すとき、私は臨床教科書に出てくる腱反射と筋トーンの典型像を小さな図表にして、機序と一対一で並べます。
末梢の出力断では反射弓の最後が弱るので腱反射は落ち、抑制の脱落では脊髄回路のゲインが上がるので反射が跳ね上がる、という対応を横に置くと、弛緩と痙性がただの見た目の違いではなく、どの回路素子が沈黙したかの読影になるからです。
症状と作用点の相関
症状から作用点を逆算するときは、「どこで信号が止まったか」だけでなく、「どの回路の抑制と興奮の釣り合いが崩れたか」を見ると整理が進みます。
BoNTでは、神経終末まで活動電位は到達していても、SNARE切断のため小胞融合が起こらず、終板にアセチルコリンが出ません。
筋線維は受け皿も興奮収縮連関も保っているのに、入力だけが途切れるので、像としては力が入らない、筋が柔らかい、反射が鈍いという弛緩性に寄ります。
α-BTXは同じく弛緩性の見え方を取りますが、止めている場所はシナプス後膜です。
神経終末からの放出は残っていても、ニコチン性アセチルコリン受容体が塞がれるため終板電位が立ちません。
つまり神経から筋へのリンクが受容体側で断たれています。
前節で触れた神経刺激と筋直接刺激の対照は、まさにこの切り分けを可視化するものです。
前シナプス毒と後シナプス毒はどちらも弛緩性の顔を見せますが、片方は「送れない」、もう片方は「受け取れない」です。
TeNTでは事情が異なります。
抑制性介在ニューロンが沈黙すると、運動ニューロンは興奮性入力に対してむき出しになります。
筋へ行く命令が消えるのではなく、抑制制御が失われて過剰に出るので、同じ麻痺でも「動けない」の中身が、力が出ないのではなく、力が入り過ぎて思うように制御できない状態へ変わります。
痙性で腱反射が亢進するのは、反射回路の抑制ゲートが壊れているからです。
TTXはこの両者の外側に位置します。
活動電位の伝導自体を止めるため、運動回路の出力も感覚入力も一段上流で落ちます。
症候の表面だけ見ると筋力低下や麻痺として現れますが、本質は「シナプス前」でも「シナプス後」でもなく、配線に信号が走らないことです。
化学式が C11H17N3O8、分子量が 319.27 の小分子でありながら、人体では 1〜2 mg が致死量の目安になるという事実は、軸索伝導がどれほど中枢的なボトルネックかを示しています。
分子数に置き換えると 1 mg でも約1.9×10^18 個に達し、回路全体の通電停止という帰結の重さが数字の上でも見えてきます。
ここで補助線として役立つのがω-コノトキシンGVIAです。
これはN型Ca2+チャネルを塞ぎ、神経終末へのCa2+流入を減らして放出確率を下げます。
SNAREを切るBoNTとは違い、小胞融合装置そのものではなく、その引き金を弱めるシナプス前遮断です。
同じ「出ない」でも、放出機械が壊れたのか、放出を起こすCa2+シグナルが入らないのかで、分子標的の層が一段異なります。
回路図の上にこの違いを書き足すと、シナプス前遮断の内部にも複数の型があることが見えてきます。
💡 Tip
弛緩性か痙性かを見分ける近道は、筋そのものを見るより、回路のどこで抑制が残り、どこで出力が切れたかをたどることです。末梢の神経筋接合部が途絶えれば弛緩へ、抑制性介在ニューロンが途絶えれば痙性へ傾きます。
比較表:代表神経毒5種
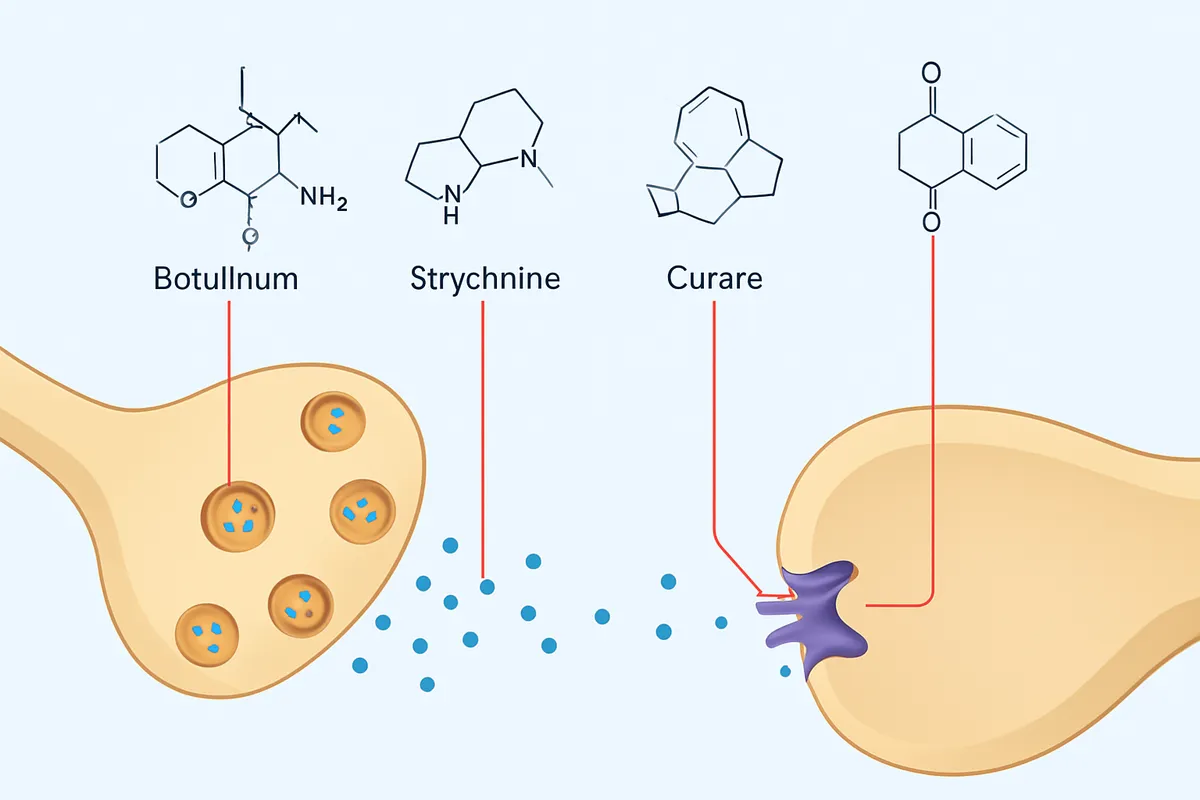
回路の違いを一覧にすると、同じ麻痺でも意味が違うことがさらに明瞭になります。
研究史の観点も横に置くと、毒が単なる病原因子ではなく、神経生理の地図を描いてきた道具でもあったことが見えてきます。
| 毒素 | 作用点 | 分子標的 | 典型的な症状・回路効果 | 歴史的意義 |
|---|---|---|---|---|
| TTX | 軸索膜 | 電位依存性Na+チャネル | 活動電位の発生・伝導停止による出力低下。伝導全般が遮断される | Na+チャネル研究のchemical toolとして神経興奮の理解を押し進めた |
| BoNT | 末梢のコリン作動性神経終末 | SNAP-25、シナプトブレビン、シンタキシン | ACh放出停止による弛緩性麻痺 | SNAREと膜融合機構の解明、治療応用の基盤を作った |
| TeNT | 脊髄の抑制性介在ニューロン | VAMP(シナプトブレビン) | 抑制性伝達低下による運動ニューロン過興奮。痙性麻痺 | 抑制回路の生理と逆行輸送の理解に中心的役割を果たした |
| α-BTX | 神経筋接合部のシナプス後膜 | ニコチン性アセチルコリン受容体 | 終板電位消失による神経筋伝達遮断。弛緩性の像に近い | ACh受容体の標識・局在解析を切り開いた |
| ω-コノトキシンGVIA | 神経終末 | N型Ca2+チャネル | Ca2+流入低下による神経伝達物質放出低下 | シナプス前Ca2+チャネル研究の選択的ツールとして使われた |
この5種を並べると、麻痺は一語でも、切れている場所は配線、放出装置、受容体、抑制回路とばらばらです。
症状の差は毒の強弱ではなく、回路上の住所の差から生まれます。
私はこの表を作るとき、教科書的な身体所見の欄を頭の中に重ねています。
筋トーン低下と反射低下が見えたら末梢出力断を疑い、筋トーン上昇と反射亢進が前面に出たら抑制回路の破綻を考える、という読み方です。
毒素名を覚えるだけなら表は暗記カードで終わりますが、回路図と身体所見を結ぶ表として使うと、病態の見え方そのものが変わります。
神経毒はなぜ神経科学を進歩させたのか

チャネル生理学とTTX
神経毒が神経科学を前に進めた最大の理由は、複雑な現象を「一か所だけ止める」道具になったことです。
その象徴がTTXです。
化学式 C11H17N3O8、分子量 319.27 の小分子で、電位依存性Na+チャネルを選択的に塞ぐ。
この選択性のおかげで、活動電位という現象を、漠然とした電気の波ではなく「Na+流入に依存する膜イベント」として切り出せるようになりました。
神経が興奮する仕組みは、理論だけでは定着しません。
どの電流が立ち上がりを担い、どの電流が再分極を担うのかを、薬理学的に一つずつ黙らせて見せる必要がありました。
そこでTTXは、Na+電流成分を消して回路図の輪郭を浮かび上がらせる、典型的な chemical tool になったのです。
私は基礎生理学の講義で、教員がTTXと4-APTEAを並べて、膜電流を成分ごとに考える古典実験の話をしていた場面をよく覚えています。
実験操作そのものより印象に残ったのは、「神経の電気現象は一枚岩ではなく、遮断薬で分けてはじめて見える」という発想でした。
Na+チャネルを止めると立ち上がりの本体が見え、K+側を触ると再分極の意味が変わって見える。
あの説明を聞いたとき、活動電位は教科書の模式図ではなく、複数の分子素子が重なってできた合成波形なのだと腑に落ちました。
TTXの歴史的意義は、単に強い毒であることではなく、電流を分解して理解する神経生理学の作法を定着させた点にあります。
その後の展開でもTTXの役割は続きました。
Na+チャネルの分子実体が絞り込まれ、さらにサブタイプごとの違いを考える段階になると、TTX感受性か抵抗性かという区別が強力な手がかりになりました。
チャネル生理、分子同定、サブタイプ選択性解析という流れのどこを見ても、TTXは「標的を選んで止める」道具として中心にいます。
毒が病態の説明材料から、分子の存在証明に使う試薬へと役割を変えた典型例です。
膜融合研究とBoNT/TeNT
BoNTとTeNTがもたらした転換は、シナプス前終末で起きる放出を、形態学ではなく分子機構として記述できるようにしたことです。
神経終末では、到達した活動電位がCa2+流入を呼び、その合図でシナプス小胞が膜融合して伝達物質を放出します。
シナプス間隙は約20 nmしかなく、この短い距離をまたぐ通信は一見すると瞬間的ですが、実際には小胞のドッキング、プライミング、融合という段階的な分子反応に支えられています。
BoNTとTeNTは、その装置の中核を切断することで、見えにくかった過程を一気に可視化しました。
BoNTは約150 kDaのタンパク質で、重鎖が標的細胞への結合と侵入を担い、軽鎖が細胞質でSNAREタンパク質を切断します。
TeNTも同系統の毒素としてVAMP(シナプトブレビン)を標的にし、ただし回路上の行き先が異なるため、末梢ではなく抑制性介在ニューロンの機能破綻として現れます。
研究史の観点で見ると、この違いは症状の違いだけを意味しません。
SNAP-25、シナプトブレビン、シンタキシンといったSNARE群が、小胞融合に不可欠な共通装置であることを突き止める推進力になりました。
毒素が切る基質をたどることで、放出装置の部品表が見えてきたわけです。
ここで面白いのは、病気を起こす毒が、そのまま神経分泌の教科書を書き換えた点です。
以前は「神経終末から伝達物質が出る」とひとまとめにされがちだった現象が、BoNTやTeNTによって「どの分子が切られると、どの段階で融合が止まるか」という言葉で語れるようになりました。
シナプス生物学が分子生物学と強く接続されたのはこの時代です。
膜融合の研究は神経系だけの話に留まらず、分泌一般の理解にも波及しました。
しかもBoNTは、研究用ツールにとどまらず治療へ反転した点でも特異です。
末梢コリン作動性終末でアセチルコリン放出を抑える作用は、過剰な筋収縮や異常な筋緊張を和らげる方向に使えます。
毒性の本体である「放出を止める力」が、標的と用量を制御することで治療効果へ変わったわけです。
毒が道具になり、その道具が医薬へ移る。
この流れは、毒性学と薬理学が地続きであることを最も鮮やかに示しています。
受容体科学とα-BTX

シナプス後膜の研究で同じ役割を果たしたのがα-BTXです。
74アミノ酸残基、分子量 7,983 のこの毒素は、ニコチン性アセチルコリン受容体(nAChR)に強く結合します。
神経筋接合部では、前シナプスから放出されたアセチルコリンが受容体に結合して終板電位を生みますが、α-BTXがあると受容体側で応答が止まる。
ここまでは毒としての顔です。
研究史ではむしろ、その高親和性結合が標識分子として価値を持ちました。
受容体研究の難しさは、膜タンパク質が見えにくく、追いかけにくいことにあります。
α-BTXが導入されることで、nAChRの局在を可視化し、受容体を精製し、どのサブユニットから成るのかを解析する道が開けました。
受容体という概念は長く薬理学の中心にありましたが、概念だけではなく、実体としてつかめるようになった意義は大きいです。
神経筋接合部のシナプス後膜に受容体が高密度に集まっていることを示し、その分子構成を追えるようになったことで、受容体科学は機能記述から構造記述へ一段進みました。
TTXがチャネル生理学を切り開き、BoNTTeNTが小胞融合の分子基盤を掘り当て、α-BTXが受容体を手で触れられる対象にした。
この並びを見ると、神経科学の重要な柱のいくつかが、毒を「止めるための武器」ではなく「見分けるための道具」として使うことで整備されたことがわかります。
毒が道具に変わると、回路図は分子地図になります。
チャネル生理学、シナプス生物学、受容体科学が体系だった学問として組み上がった背景には、この変換がありました。
現代の応用と限界
BoNTの臨床応用の現在地
BoNTは、神経科学の歴史を動かした研究ツールであると同時に、現代医療では確立した治療手段として位置づいています。
とくに実績が厚いのは、眼瞼痙攣や痙性斜頸のように、局所の過剰な筋収縮が症状の中心になる領域です。
末梢コリン作動性終末でアセチルコリン放出を抑えるという作用は、病態の側から見ると「過剰に入っている運動の出力を静める」ことに相当します。
分子機構の理解が、そのまま適応の論理に結びついているわけです。
2020年代に入ってからは、この古典的な適応だけでなく、ジストニア、痙縮、慢性片頭痛、過活動膀胱、唾液分泌の過剰といった領域まで、臨床での位置づけが整理され直されています。
ここで見えてくるのは、BoNTが単なる「筋弛緩の薬」ではなく、神経終末からの放出制御を利用する精密な生物学的製剤として理解されていることです。
筋緊張の異常だけでなく、末梢神経の異常活動や分泌の偏りが症状を支える病態でも応用の余地が検討されてきました。
この流れを追っていると、基礎研究で培われたSNARE切断という知識が、臨床では病態選別の言葉に置き換わっているのがわかります。
どの患者群で局所的な神経伝達の抑制が利益になるのか、どこまで可逆性を保ちながら機能調整として使えるのか、そうした問いが適応拡張の軸になっています。
毒素の医学利用というと驚きをもって語られがちですが、現場ではむしろ、分子標的が明確であることが長期的な信頼につながっています。
BoNTイノベーションと会議動向
近年のBoNT研究では、既存適応の整理だけでなく、分子改変によって性質を作り分ける発想が前面に出ています。
2023年から2025年にかけてのレビューを読むと、焦点は大きく三つあります。
ひとつは標的指向性の再設計、ひとつは作用の時間幅や組織選択性の調整、もうひとつは新規適応の探索です。
天然毒素をそのまま眺める段階から、どの細胞に、どのくらいの期間、どの出力を抑えるかという工学的な設計思想へ研究の重心が移っています。
私自身、最近の学会プログラムを要旨レベルで追っていて印象的だったのは、基礎と臨床の境界が以前よりずっと薄くなっていることです。
エンジニアードBoNTを扱う演題では、細胞内移行、基質選択性、神経回路への作用という典型的な基礎テーマが並ぶ一方で、そのすぐ隣に疾患適応や翻訳研究のセッションが置かれています。
昔なら「毒素の分子機構」と「治療薬開発」は別会場の話題でしたが、今は同じプログラムの中で連続して読めます。
この並びを見ると、BoNT研究は発見科学と実装科学の往復運動に入ったのだと実感します。
TTXの現代的価値
TTXは医療応用の話題だけで測るとBoNTほど前景には出ませんが、研究ツールとしての価値は今も揺らいでいません。
電位依存性Na+チャネルを選択的に止められるという性質は、神経興奮のどこまでが活動電位依存で、どこから先がシナプスや回路の性質なのかを切り分けるうえで、今なお鋭い切れ味を持っています。
神経細胞の発火、軸索伝導、ネットワーク活動の寄与を分解したい場面では、TTXは古びた古典試薬ではなく、実験の論理を支える基準点です。
この毒素の価値は、作用点が明快であることに尽きます。
BoNTがシナプス前終末の放出装置を止め、α-BTXがシナプス後受容体を押さえるのに対して、TTXはそれ以前、つまり電気信号の生成と伝導の段階を遮断します。
だからこそ、神経活動を層ごとに分けて考えるときの「最初の関門」として使えます。
パッチクランプ、培養神経回路、感覚系の電気生理、薬理学的な切り分け実験のどれを見ても、この位置づけは変わっていません。
毒性学の立場から見ても、TTXは「危険だから遠ざける対象」ではなく、「作用機序が鮮明だからこそ科学を前に進める対象」でした。
分子量319.27の小分子が、神経系という巨大なシステムの入口をぴたりと塞ぐ。
その一点突破の明快さが、Na+チャネル研究の解像度を押し上げてきたのです。
現代の神経科学は光遺伝学や遺伝子改変の手法が豊富ですが、それでも薬理学的に即座に機能を切り分ける道具の価値は失われていません。
TTXは、その代表格として残り続けています。
限界・倫理・安全の原則
応用の広がりを語るときでも、これらが猛毒である事実は後景化できません。
研究利用も医療利用も、厳格な法規制、施設基準、バイオセーフティ、倫理審査の枠内でのみ成立します。
ここで問われるのは「使えるかどうか」より先に、「どの目的で、どの管理体制のもとで扱うのか」です。
毒素は強力だから価値があるのではなく、標的が明確で、管理の原則が制度として埋め込まれているからこそ、研究資源や医療資源になりえます。
限界もはっきりしています。
BoNTは臨床応用が進んだとはいえ、あらゆる神経疾患を広く治せる分子ではありません。
局所性、標的選択性、作用の可逆性という利点は、そのまま適応の境界線でもあります。
TTXもまた、研究の切り分けには有用でも、現代的価値の中心はあくまで実験系での精密な機能解析にあります。
どちらも「よく効く毒」だから持ち上げられているのではなく、どこで役に立ち、どこから先は役割が変わるのかがはっきりしている点に価値があります。
ℹ️ Note
2020年代の毒素研究を見ていると、焦点は毒性の強さそのものではなく、標的特異性をどう理解し、どう制御し、どこまで社会的に許容できる形へ翻訳できるかに移っています。
毒をめぐる倫理は、センセーショナルな言葉よりも、管理と目的の一致で語るほうが本質に近いです。
基礎研究では再現性と封じ込め、臨床では適応と利益相反の透明性、学会では新規性だけでなく実装可能性まで含めて問われます。
そうした枠組みのなかで見ると、BoNTの医療応用も、TTXの研究ツールとしての持続的な価値も、どちらも現代科学の節度の上に成り立っていることが見えてきます。
まとめと次のアクション
三分法の復習
三分法で言い切るなら、TTXはNa+チャネル遮断、BoNTとTeNTはSNARE切断、α-BTXはnAChR遮断です。
見分ける軸は「どこで止めるか」と「何を切るか・塞ぐか」の二つで足ります。
BoNTはシナプス前でACh放出を止めるのに対し、α-BTXはシナプス後で受容体を塞ぎます。
TeNTの痙性は毒そのものが筋を直接興奮させるからではなく、抑制路を遮断した回路効果として読むと腑に落ちます。
講義後の復習では、私は作用点、標的分子、症候の三段リンクを口で言えるかをよく確認します。
たとえば「シナプス前終末、SNARE、弛緩性麻痺」「シナプス後膜、nAChR、神経筋伝達遮断」という形で詰まらず説明できれば、丸暗記ではなく回路として理解できています。
図で理解を固める
ここでいちど本文の「作用点別の神経毒分類図」を見返し、各毒について標的分子を一行で言えるか試してみてください。
理解を定着させるには、「正常なシナプス伝達」と「各毒の遮断点」を一枚で並べた最終図が効きます。
正常系の流れのどこが切れているのかを同じ座標で見比べると、神経毒は種類の暗記ではなく、回路上の停止位置として頭に残ります。
薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
テトロドトキシンとフグの耐性|なぜ自分の毒で死なないのか
フグが自分の毒で死なない理由は、ひとつではありません。テトロドトキシン(TTX、C11H17N3O8、分子量319.27)を主に外部から取り込みながら、同時に自分の電位依存性Na+チャネルのTTX結合性をアミノ酸置換で下げ、神経と筋の麻痺を避けているからです。
毒ヘビの種類と毒の違い|神経毒と出血毒を比較
「コブラ科は神経毒、クサリヘビ科は出血毒」と覚えると入口はつかめますが、毒性学の論文を読み込むほど、その図式だけでは取りこぼすものが増えていきます。3FTx、PLA2、SVMPといった毒素群の一次論文を概観すると、ヘビ毒は単一の化合物ではなく、タンパク質・酵素・ポリペプチドが混ざり合った複合毒であり、
トリカブトとアコニチン|日本三大有毒植物の科学
春の山菜採りの季節になると、毎年のように名前があがるトリカブトは、特定の一種ではなくAconitum属の総称で、日本ではドクゼリドクウツギと並ぶ「三大有毒植物」として記憶されています。
毒の進化|防御と捕食、盗用と共進化の科学
自然史系の特別展「毒」を歩くと、読者の頭にまず浮かぶのは「どれがいちばん危険か」より、「生きものはなぜ、こんな仕組みを持ったのか」という問いだと思います。この記事は、その疑問に答えるために、まずpoisonを食べたり触れたりして効く毒、venomを牙や針で注入する毒、