毒の種類と分類|神経毒・出血毒・細胞毒
毒の種類と分類|神経毒・出血毒・細胞毒
神経毒・出血毒・細胞毒という三つの言葉は、どれも「毒」を指しているのに、実際には傷つける相手が違います。神経毒はニューロンや神経筋接合部、出血毒は凝固系や血管内皮、細胞毒は細胞膜・代謝・核酸合成系を主な標的とし、その違いをNa+/K+/Ca2+チャネル、シナプス、血液凝固、膜障害という分子レベルで並べると、
神経毒・出血毒・細胞毒という三つの言葉は、どれも「毒」を指しているのに、実際には傷つける相手が違います。
神経毒はニューロンや神経筋接合部、出血毒は凝固系や血管内皮、細胞毒は細胞膜・代謝・核酸合成系を主な標的とし、その違いをNa+/K+/Ca2+チャネル、シナプス、血液凝固、膜障害という分子レベルで並べると、毒の分類はずっと立体的に見えてきます。
本記事は、テトロドトキシン、ボツリヌス毒素、クサリヘビ毒、細菌性細胞毒をひとつの地図の上に載せて整理したい人に向けたものです。
実際の毒は教科書どおり一箱には収まらず、ヘビ毒のように神経毒性と出血毒性と細胞障害性が重なって現れる例も珍しくありません。
私自身、安全性研究の現場でLDH、MTT、ATPアッセイを並べて細胞障害を見てきましたが、どの指標を採るかで「細胞毒」の輪郭は思った以上に変わります。
だからこそ本稿では、毒を症状名で覚えるのではなく、どの分子をどう壊し、その知見がテトロドトキシンのNa+チャネル研究やボツリヌス毒素、ω-コノトキシンの医療応用へどうつながったのかまで、横断してたどります。
神経毒・出血毒・細胞毒とは何か
分類の基準と射程
この三分類は、毒を「どこに最も強く当てるか」で整理した便宜的な地図です。
基準になるのは主たる標的組織・機能で、神経毒は神経系、出血毒は凝固系・血管・周辺組織、細胞毒は広い意味での細胞障害を中心に捉えます。
ひとつの毒液が複数の成分を含むことは珍しくなく、実物はこの地図の境界線を何度もまたぎます。
その前提を置いたうえで、標的臓器、分子標的、代表毒、研究史、現代応用という5つの軸で眺めると、この後の見取り図がつかみやすくなります。
神経毒は、ニューロンそのもの、あるいは神経筋接合部の情報伝達を乱す毒です。
分子レベルでは電位依存性のNa+・K+・Ca2+チャネル、受容体、放出装置が主な標的になります。
たとえばテトロドトキシンは電位依存性Na+チャネルを選択的に塞ぎ、活動電位の発生と伝導を止めます。
神経が「電気信号を走らせる配線」だとすると、TTXは配線を切るのでなく、配線の途中に絶縁栓を差し込む毒です。
古典的な神経生理学でTTXが重宝されたのは、この選択性が高かったからです。
脳科学辞典 フグ毒

同じ神経毒でも、標的が変わると見え方は一変します。
ボツリヌス毒素はイオンチャネルを直接ふさぐのではなく、神経終末でアセチルコリン放出に必要な分子機構を切断し、神経筋接合部での伝達を遮断します。
結果として筋肉は命令を受け取れず、弛緩性の麻痺が起こります。
コノトキシン群はさらに多彩で、なかでもω-コノトキシンはシナプス前終末のCaVチャネルを標的にし、Ca2+流入を止めて神経伝達物質の放出を妨げます。
Na+チャネルを止めるTTX、放出機構を止めるボツリヌス毒素、Ca2+依存の放出トリガーを止めるω-コノトキシンは、同じ「神経毒」でも分子標的が別であることを端的に示しています。
Frontiers Naチャネルと神経毒
出血毒は、血そのものだけを傷つける毒ではありません。
主戦場は血管内皮、基底膜、凝固因子、赤血球、周辺組織で、出血、腫脹、凝固異常、組織障害を引き起こします。
ヘビ毒で代表的なのが金属プロテアーゼ群で、血管壁や細胞外マトリックスを壊すことで微小血管をもろくし、局所の出血や皮下血腫につながります。
凝固系をかき乱すセリンプロテアーゼや、膜障害に関与するPLA2が重なると、見かけ上は「出血している」のに、実際には血管破壊、凝固因子の消費、周囲組織の壊死が同時進行していることもあります。
教育現場では「コブラは神経毒、マムシは出血毒」と短く説明されがちですが、研究レビューを読み込むほど、この二分法だけでは毒液全体のふるまいを取りこぼす場面が増えます。
細胞毒は、三分類のなかでいちばん射程が広い言葉です。
細胞膜の破壊、ミトコンドリア障害、DNA複製や転写・翻訳の阻害、アポトーシスやネクローシスの誘導まで含みます。
つまり「特定の臓器系」よりも、細胞という単位で何が壊れるかに注目した分類です。
毒性学の現場では、LDH放出、MTT/XTT、ATP定量のどれで細胞障害を切り取るかによって、同じ試料でも輪郭が少し変わります。
私も安全性試験でこのズレを何度も見てきましたが、その経験から言うと、細胞毒は「毒素の種類」を指す言葉であると同時に、「細胞がどれだけ傷んだか」を測る評価の言葉でもあります。
研究史の軸で見ると、神経毒は単に危険な物質ではなく、分子生物学と薬理学を押し進めた実験ツールでもありました。
TTXはNa+チャネル研究の化学的プローブとして、神経がどのように活動電位を作るのかを切り分ける役目を果たしました。
コノトキシンはCa2+チャネルや受容体サブタイプの機能を分離して考える道具になり、ボツリヌス毒素は神経終末の開口放出機構を理解する入口になりました。
現代応用の軸では、ボツリヌス毒素が医療・美容で使われ、コノトキシン研究が鎮痛薬開発に接続し、細胞毒の概念が抗がん薬評価や安全性試験の基盤になっています。
分類は名称整理で終わるものではなく、研究の蓄積と応用先まで含めた作業台なのです。

フグ毒 - 脳科学辞典
bsd.neuroinf.jp用語の注意点
初心者が最初につまずきやすいのは、言葉がぴったり対応していないことです。
神経毒は比較的わかりやすく、神経系に主作用を示す毒を指しますが、それでも「神経毒」と「神経毒性」は別です。
前者は毒のカテゴリ、後者は物質が神経系に障害を与える性質で、鉛や有機溶媒のように古典的な“neurotoxin”の顔つきをしていなくても神経毒性を持つものはあります。
出血毒は、日常語の感覚だと「血液を壊す毒」と受け取られがちですが、実際にはそれでは狭すぎます。
血管内皮や基底膜の破壊、凝固因子の消費、線溶系の攪乱、赤血球障害まで含めて出血を生むため、厳密には「血液毒」という表現だとずれが出ます。
血だけでなく、血管と組織が標的に入っているからです。
ヘビ毒の解説で「血液毒」という言い方が広く流通している一方、研究レベルではそれだけでは病態を言い表せません。
細胞毒も二重の意味を持つので注意が必要です。
細菌学や毒素学では、特定の細胞を壊す毒素そのものをcytotoxinと呼ぶことがあります。
一方で毒性学や創薬では、cytotoxicityは「細胞死や機能低下を起こす性質」やその評価系を指します。
入門書でこの二つが混ざると、「細胞毒」という実体的な毒素分類と、「細胞毒性」という試験概念が同じ箱に入ってしまいます。
ここを分けておくと、アマトキシンのような転写阻害毒、シアン化物のような代謝毒、膜破壊型毒素が、なぜ同じ“細胞障害”の側に並ぶのかが見えてきます。

教育現場や一般向けの入門書では、神経毒/出血毒の二分法がいまも便利に使われます。
私もその説明が入口として役立つ場面を否定しません。
ただ、レビュー論文ベースで全体を見ると、この整理は「主症状の見え方」を優先した短縮表現です。
実際のヘビ毒には神経毒成分、出血毒成分、筋毒成分、拡散を助ける酵素が同居し、どれが前景に出るかで病像が変わります。
💡 Tip
[!NOTE] 入門段階では「主にどこを狙う毒か」で把握し、次の段階で「実際には複合作用を持つ」と上書きすると、分類と実物のずれで混乱しません。
神経毒を分子レベルで理解するうえでは、症状名より分子標的に目を向けるのが近道です。
Na+チャネルを遮断するテトロドトキシン、Ca2+チャネルを標的にするω-コノトキシン、神経筋接合部でアセチルコリン放出を止めるボツリヌス毒素を並べるだけでも、麻痺という同じ現象の裏に別々の故障点があるとわかります。
この視点を持つと、神経毒・出血毒・細胞毒という言葉は、単なるラベルではなく、標的臓器から分子機構へ降りていくための座標軸として機能します。
神経毒の仕組み|イオンチャネルとシナプスが標的になる

イオンチャネル入門
神経毒を分子レベルで眺めると、まず見えてくるのがイオンチャネルです。
神経細胞の膜には、Na+、K+、Ca2+といったイオンを選択的に通すタンパク質の孔が埋め込まれており、これが電気信号と化学信号の変換装置として働いています。
Na+チャネルは活動電位の立ち上がりを担い、K+チャネルは興奮後の再分極を担い、Ca2+チャネルはシナプス前終末で神経伝達物質放出の引き金になります。
神経筋接合部では、この一連の流れがアセチルコリン放出、筋線維の脱分極、収縮へとつながります。
教科書の模式図では、Na+が入って膜電位が上がり、続いてK+が出て元に戻る、と簡潔に描かれます。
実際に古典的な電位固定実験の記録を重ねてみると、その図は単なる概念図ではなく、膜電流の時間変化をそのまま抽象化したものだと実感します。
私自身、この対応関係を学生に説明するときは、Na+電流が落ちれば活動電位は立ち上がれず、筋肉まで命令が届かないので筋力低下に直結する、と一般化して話します。
逆にK+チャネルが乱れれば再分極のテンポが崩れ、Ca2+チャネルが止まれば終末から放出の合図が出ません。
麻痺という一語の裏に、電気信号の発生、伝導、放出という別々の故障点があるわけです。
私が学生に説明するときは、Na+電流が落ちれば活動電位が立ち上がれず、筋肉まで命令が届かないため筋力低下に直結すると伝えています。
一方で神経毒性は「伝わらない」だけではありません。
神経が過剰に興奮する方向の障害もあり、たとえば報告例では培養系でグルタミン酸が約500 μMに達すると24時間後に神経細胞の大半が死滅することが示されています。
神経毒とは、信号を止める毒だけでなく、興奮を暴走させて細胞を壊す毒性も含む概念です。
Na+チャネル遮断:テトロドトキシン
テトロドトキシンは、電位依存性Na+チャネルの外側に結合してNa+の通り道を物理的に塞ぎます。
すると活動電位の立ち上がりが起こらず、すでに発生している信号の伝導も止まります。
神経は電気的に沈黙し、神経筋接合部まで命令が届かないため、臨床的にはしびれ、筋力低下、進行すると弛緩性麻痺として現れます。
標的が筋そのものではなく、筋に命令を運ぶ配線側にある点がこの毒の本質です。
研究史でもTTXは特別な位置を占めます。
電位依存性Na+チャネルだけを選択的に止めるため、活動電位のどの成分がNa+由来なのかを切り分ける化学ツールになりました。
古典的な実験では、ロブスター巨大神経線維で3×10^-8 g/mL(約94 nM)のTTXが活動電位を遮断したことが示され、膜興奮の理解を一気に前進させました(原典参照)。
この種のデータを読むと、教科書に載っている「Na+が入ると脱分極する」という一文が、実際には薬理学的に切り分けられた現象であることがよくわかります。
TTXは毒であると同時に、チャネル病研究を押し進めた実験道具でもあります。
Na+チャネルのサブタイプ差、組織差、病態差を比較する足場になり、どの細胞がTTX感受性で、どの細胞がTTX抵抗性かという整理から、痛覚や不整脈の研究まで広がりました。
毒物学ではしばしば、危険な分子ほど機序が鮮明で、鮮明だからこそ研究ツールになる、という逆説が起こります。
TTXはその典型です。
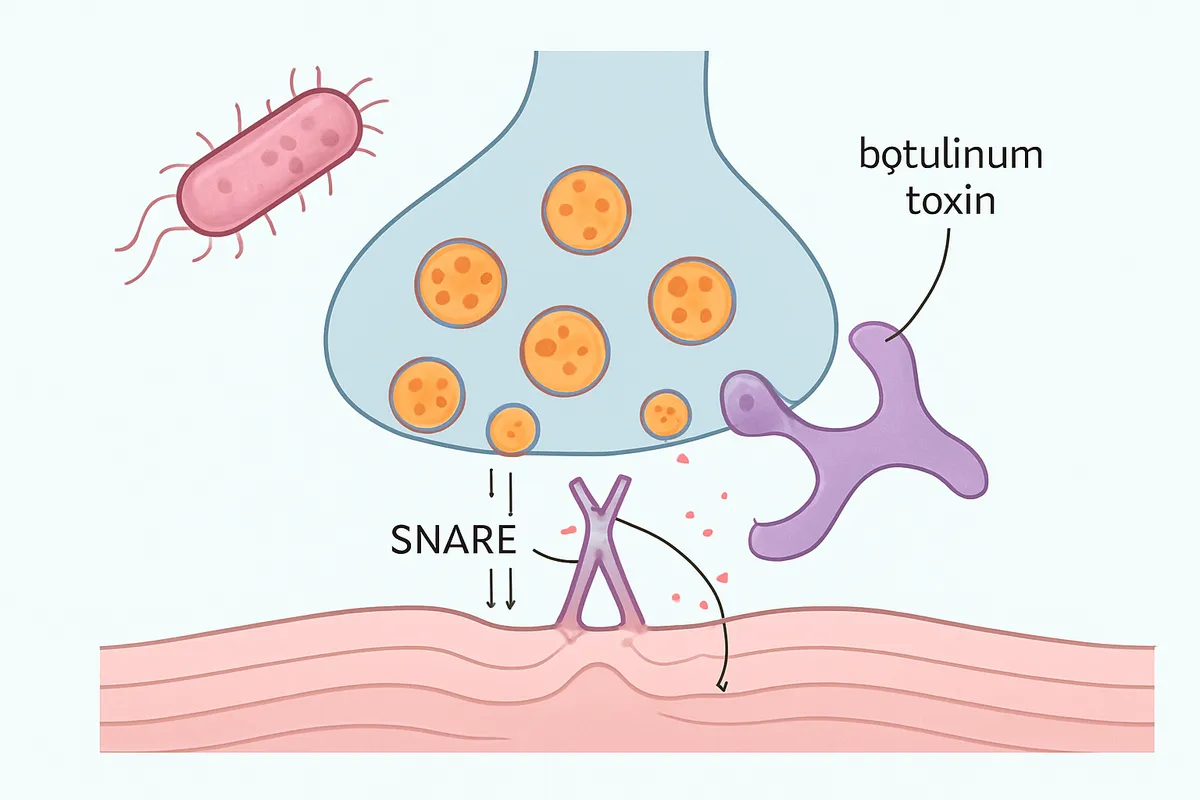
シナプス前阻害:ボツリヌス毒素
ボツリヌス毒素は、Na+チャネルやK+チャネルを直接塞ぐタイプではなく、シナプス前終末の放出 machinery を壊す神経毒です。
神経筋接合部では、運動神経終末に活動電位が到達するとCa2+流入が起こり、SNARE複合体が働いてアセチルコリン小胞が膜融合し、筋へ命令が渡ります。
ボツリヌス毒素はこのSNARE関連タンパク質を切断し、アセチルコリン放出を止めます。
電気信号は終末まで来ていても、化学信号への変換で詰まるため、筋は収縮命令を受け取れません。
結果は弛緩性麻痺です。
この機序は、神経毒の見取り図を立体的にしてくれます。
TTXは配線そのものの通電を止め、ボツリヌス毒素は終端の放出装置を止める。
どちらも筋力低下を招きますが、壊している段階が違います。
神経筋接合部を学ぶ場面でこの違いを押さえると、麻痺の病態が一気に整理されます。
なお、しばしば引用されるLD50の数値は桁のインパクトが先行しがちです。
今回参照した範囲で流通している0.001 μg/kgという例示値については、動物種・投与経路を含む原典の明記が必要であり、ここでは確定値として扱いません。
局所投与で神経筋接合部の伝達を薬理学的に制御している、という理解のほうが本質に近いです。
ℹ️ Note
ボツリヌス毒素を「最強の毒」とだけ覚えると、医療応用の意味が見えません。局所で、限られた神経終末に、放出阻害を起こす量だけ届けると薬になる、という整理のほうが実態に沿っています。
CaV遮断:ω-コノトキシン
ω-コノトキシンは、イモガイ由来のペプチド毒群のうち、電位依存性Ca2+チャネル(CaVチャネル) を標的にするタイプです。
シナプス前終末では、活動電位の到達に伴ってCaVチャネルが開き、流入したCa2+が神経伝達物質放出の直接の引き金になります。
ここを遮断すると、小胞融合の合図が出ないため、アセチルコリンを含む伝達物質放出が落ちます。
神経筋接合部で見れば、結果はやはり伝達遮断です。
ただし停止しているのはNa+による伝導ではなく、Ca2+依存の放出トリガーです。
ω-コノトキシンの価値は、毒性そのものだけではありません。
CaVチャネルには複数のサブタイプがあり、どのサブタイプがどの神経回路や放出機構を担っているかを切り分けるうえで、この毒素群は鋭い道具になりました。
疼痛研究で存在感が大きいのもそのためです。
痛みの伝達に関わるCaVサブタイプを選択的に抑える発想は、神経毒を鎮痛薬へつなぐ発想そのものでもあります。
神経科学では「毒がチャネルの地図を描く」と言われることがありますが、ω-コノトキシンはまさにその役を果たしました。
この比喩は分かりやすさのための表現ですが、ω-コノトキシンはCaVチャネルの機能地図を描く上で重要な道具でした。
Na+、K+、Ca2+チャネルを並べると、この枠組みでは神経毒の世界は「麻痺を起こす物質の寄せ集め」ではなく、膜興奮とシナプス伝達のどこを断つかで整理できる体系として見えてきます。
Na+を止めれば信号は走らず、Ca2+を止めれば放出が起こらず、K+チャネルに作用すれば興奮の幅や反復性が変わる。
そこに神経筋接合部という具体的な現場を重ねると、分子の出来事が筋力低下や麻痺としてどう現れるかまで、一本の線でつながります。
出血毒の仕組み|血管・凝固系・組織破壊が連鎖する
凝固系の破綻
出血毒は、単に「血が止まらなくなる毒」ではありません。
実際には、プロテアーゼによる凝固系の攪乱、血管壁そのものの傷害、局所組織の破壊が同時進行し、その結果として出血が前景に出てきます。
とくにクサリヘビ科やマムシ類の毒では、この連鎖が典型的です。
咬まれた直後は局所の痛みや腫れが目立っていても、時間がたつにつれて凝固異常が加わり、見えている傷以上に全身の止血システムが揺さぶられていることがわかってきます。
凝固系の破綻の中心には、ヘビ毒中のセリンプロテアーゼや金属プロテアーゼがあります。
これらは血液凝固カスケードの一部を勝手に作動させたり、逆に必要な基質を分解したりします。
代表的なのがフィブリノーゲン分解です。
フィブリンの材料になるフィブリノーゲンが分解されると、血液は見かけ上「固まりそうな反応」を起こしていても、実際には安定した血栓を作れません。
さらに凝固因子が次々と消費されると、病態は凝固因子消費を伴う消費性凝固障害へ傾きます。
これは「固まりすぎる病態」と「出血する病態」が同じ系の破綻としてつながっている、という意味です。
救急の症例レビューを読んでいると、この進み方はよく似た輪郭を持っています。
受傷の初期には咬傷部の腫脹と疼痛が前面にあり、数時間のうちに皮下出血や血液検査の異常がはっきりし、やがて止血に必要な成分が足りなくなることで、穿刺部位からのにじみ出るような出血や広範な出血傾向が目立ってきます。
見た目には「血が出ている」のですが、分子レベルではその前段階として、フィブリン形成の材料が削られ、凝固因子が空回りのように使い尽くされているわけです。
ここで「出血毒=血液毒」とひとまとめにすると、本質を見失います。
標的は血液だけではなく、止血を支える血管壁、凝固因子、周囲組織まで含まれています。
しかもヘビ毒は単一成分ではなく混合物です。
クサリヘビ科やマムシ類で出血傾向が目立つ一方、同じ毒液の中に神経毒性を持つ成分を併せ持つ種もいます。
したがって、神経毒・出血毒という分類は病態の中心を示すラベルであって、毒液の実体を一語で言い切るものではありません。
血管内皮障害と浮腫・出血
出血毒のもう一つの柱は、血管内皮障害です。
血液が血管の外へ漏れ出ないのは、凝固因子が働いているからだけではなく、そもそも血管内皮と基底膜が物理的な壁として保たれているからです。
出血毒はこの壁を壊します。
とくにSVMPは、基底膜や細胞外マトリックスのタンパク質を切断し、毛細血管の支えを失わせます。
すると血管は「栓が作れない」以前に、「容器として破れやすい」状態になります。

この段階で起こるのが、毛細血管透過性の亢進、浮腫、皮下出血です。
咬傷部位が短時間で張るように腫れ、緊満感が強くなり、紫斑や血腫が広がるのは、単純な炎症だけでは説明しきれません。
内皮が傷つき、血漿成分や赤血球が組織側へ漏れ、そこへ炎症メディエーターと組織破壊が重なるからです。
マムシ咬傷や海外のクサリヘビ科咬傷で、腫脹が目に見えて拡大していく経過はこの機序に沿っています。
私がこの病態を読むときにいつも意識するのは、出血が「結果」であって「起点」ではないということです。
典型例では、受傷後しばらくして患肢全体の腫れが増し、局所の圧痛と熱感が強まり、その後に皮下出血や凝固異常が追いかけてきます。
これはまず血管壁と周辺組織が壊され、次に凝固系の余力が削られ、最後に止血不能が表面化している流れです。
外から見える出血点だけを追っても、病態の中心には届きません。
💡 Tip
出血毒を理解するときは、「血が外へ出た」という現象より、「血管壁が壊れ、止血材料が減り、周囲組織が崩れる」という三段階で見ると、腫脹・血腫・凝固異常がひとつの連続した出来事として見えてきます。
組織破壊酵素群(SVMP/SVSP/PLA2)の位置づけ
出血毒の実体は、ひとつの毒素ではなく複数の酵素群の協働です。
その中核をなすのは金属プロテアーゼで、一般にSVMPと呼ばれます。
次にセリンプロテアーゼで、SVSPと略されます。
さらにホスホリパーゼA2はPLA2と称され、これらが協調して作用します。
加えて、ヒアルロニダーゼのような拡散促進因子も、毒液全体の攻撃性を押し上げます。
SVMPは、出血毒の「構造破壊担当」と言える存在です。
細胞外マトリックスや基底膜を分解し、微小血管を脆くして出血を起こします。
加えて、フィブリノーゲンに作用するタイプではフィブリノーゲン溶解にも関わり、血管の壁を壊しながら止血材料まで削ります。
Bothrops属をはじめとするクサリヘビ科の毒でこの性格が強く、局所出血と組織障害が前面に出る病態像とよく一致します。
SVSPは、凝固カスケードに割り込む「反応改変担当」です。
セリンプロテアーゼとしてペプチド結合を切断し、トロンビン様に振る舞うもの、フィブリノーゲンを異常に処理するものなどが知られています。
見かけ上は凝固を促しているようでも、できあがるフィブリンが不安定だったり、必要な因子だけを先に使い切ったりすると、帰結はむしろ出血です。
ここが出血毒のややこしいところで、凝固の促進と出血傾向が矛盾せずに同居します。
個々のSVSPの酵素学的パラメータや臨床相関については、総説や一次研究での確認が必要です。
PLA2は、出血毒の文脈では「膜障害と炎症増幅、そして筋壊死の推進役」として位置づけると全体像がつかみやすくなります。
PLA2はリン脂質を加水分解し、細胞膜を傷つけ、炎症反応を強め、種によっては抗凝固的に働いたり筋壊死を誘導したりします。
咬傷部位の強い疼痛、腫脹、筋組織の障害は、この成分の寄与を考えると整理しやすくなります。
局所壊死が目立つ症例では、出血だけでなく細胞レベルの破壊が並走しています。
ヒアルロニダーゼも見逃せません。
これはヒアルロン酸を分解して組織間隙をゆるめ、他の毒成分が周囲へ広がる道を作ります。
いわゆる spreading factor で、SVMPやPLA2が届く範囲を押し広げる役目です。
単独で劇的な病態を作るというより、毒液全体の浸潤力を上げる補助線として働きます。
こうして並べると、出血毒は「出血を起こす物質」ではなく、プロテアーゼが凝固系と血管壁を崩し、PLA2などが膜障害と壊死を重ね、ヒアルロニダーゼがそれを拡散させる複合システムとして理解したほうが正確です。
クサリヘビ科やマムシ類の毒が典型例ですが、毒液は分類名ほど単純ではありません。
出血性の病態を中心にしながら、神経毒成分や筋毒成分を同時に含む種もあるため、実際の咬傷では「出血毒か神経毒か」と二分するより、どの標的がどの順番で壊されているかを見るほうが、病態の輪郭がよく見えます。
細胞毒の仕組み|膜破壊からアポトーシス誘導まで
cytotoxinとcytotoxicityの違い
細胞毒という言葉は、文脈によって二つの意味を持ちます。ここを曖昧にすると、感染症の毒素の話と、培養細胞を使った安全性評価の話が混線します。
ひとつは、細菌や動物、植物などが産生する「細胞を傷害する実体としての毒素」です。
この意味でのcytotoxinは、たとえば細菌性細胞毒のように、細胞膜を破ったり、細胞内に侵入して代謝や合成系を止めたりして、標的細胞を死に向かわせる分子を指します。
膜に孔を開ける毒素なら、溶血や溶細胞という形で短時間に細胞内容物が漏れ出しますし、タンパク質合成を止める毒素なら、見た目の破裂を伴わずにじわじわ機能停止へ向かいます。
もうひとつは、ある物質や処置が細胞にとってどれだけ有害かという性質・評価概念です。
こちらがcytotoxicityで、毒そのものの名前ではありません。
抗がん剤候補化合物、ナノ粒子、界面活性剤、細菌毒素、抽出物などを細胞に加えたとき、増殖が止まるのか、膜が壊れるのか、代謝が落ちるのか、最終的に死ぬのかを測る枠組みです。
毒性学や創薬ではこちらの意味で使われる場面が多く、実験系では「この化合物は cytotoxic だった」という表現が定着しています。
この二つは無関係ではありません。
細菌性細胞毒は cytotoxin であり、その作用の強さは cytotoxicity として測定されるからです。
ただし、前者は「何が攻撃するか」、後者は「どれだけ傷んだか」を表す言葉です。
ここを分けておくと、毒素分類の話と、LDH や MTT を使った評価の話がひとつの地図の上でつながります。
主な分子機序の整理
細胞毒の仕組みは一枚岩ではありません。
標的が細胞である以上、入口は複数ありますが、大きく見ると膜、エネルギー産生、遺伝情報の流れ、酸化還元恒常性、細胞死プログラムのどこかが崩されます。
もっとも直感的なのは細胞膜障害です。
膜作用性の毒素は脂質二重層に結合し、膜を不安定化させたり、孔を形成したりします。
赤血球で起これば溶血、一般の培養細胞で起これば溶細胞として観察されます。
膜が破綻すると、イオン勾配が保てず、水が流れ込み、細胞は膨化し、やがて破裂します。
LDH のような細胞内酵素が培地へ漏れ出るのは、このタイプの障害をよく反映します。
コブラ由来のcardiotoxinが示す膜作用性や、ヘビ毒PLA2によるリン脂質分解は、この軸で理解すると位置づけが明瞭になります。
次に、ミトコンドリア代謝阻害があります。
細胞が生きるには ATP が必要で、ミトコンドリアの電子伝達系が止まると、細胞は酸素があってもエネルギーを作れません。
シアン化物がシトクロム c オキシダーゼを阻害して ATP 産生を止めるのは、この典型です。
膜がまだ保たれていても、代謝は先に崩れます。
実験系では ATP 定量や MTT 系の還元能低下として先に現れ、LDH 放出は遅れて出ることがあります。

DNA・RNA・タンパク質合成阻害も、細胞毒の大きな柱です。
DNA 損傷そのものを起こす物質もあれば、転写や翻訳を止めて生存に必要なタンパク質供給を断つ物質もあります。
アマトキシンが RNA ポリメラーゼ II を阻害して mRNA 合成を止め、結果としてタンパク質合成障害から肝細胞壊死へ進む流れは、細胞毒の「合成系阻害」の代表例です。
見た目にはすぐ破裂しなくても、細胞内では修復不能な飢餓状態が進みます。
加えて見逃せないのが酸化ストレスです。
活性酸素種の産生が増える、あるいは抗酸化防御が破綻すると、脂質過酸化、タンパク変性、DNA 損傷が連鎖します。
膜障害、代謝阻害、DNA 損傷は別々の箱に見えて、実際には酸化ストレスを介して互いを増幅します。
ミトコンドリアが傷むと活性酸素が増え、活性酸素が増えるとさらにミトコンドリアが壊れる、という循環に入ります。
その先で起こるのがアポトーシス誘導です。
細胞が即座に破裂するのでなく、カスパーゼ経路を介して自律的な死へ進む型です。
ミトコンドリア外膜の透過性が変わり、シトクロム c が放出され、カスパーゼが順に活性化されると、核の凝縮、DNA 断片化、細胞の縮小が進みます。
これは単なる「壊れた結果」ではなく、細胞がプログラムされた終了手順に入った状態です。
抗がん剤研究では、この経路を意図的に引き起こせるかどうかが評価軸になります。
こうして並べると、細胞毒とは「膜を壊す毒」だけではありません。
細胞膜障害、代謝阻害、DNA・タンパク質合成阻害、酸化ストレス、カスパーゼ経路を介したアポトーシス誘導まで含む広い概念です。
細菌性細胞毒はその中の具体例であり、毒性試験における cytotoxicity は、これらのどの層がどこまで崩れたかを読み取る作業だと考えると全体がつながります。
細胞死
細胞毒の帰結として起こる細胞死は、主にネクローシスとアポトーシスに分けて考えると輪郭がつかめます。
実際の試料では両者が重なりますが、病態の読み方は大きく変わります。
ネクローシスは、図にすると細胞が膨らみ、膜が裂け、中身が外へ流れ出るイメージです。
膜障害や急激な ATP 枯渇が強いとこちらへ傾きます。
細胞内容物が周囲へ放出されるため、周辺組織はそれを危険信号として受け取り、炎症反応が立ち上がります。
局所の腫脹、発赤、二次的な組織障害が目立つのはこのためです。
細菌性細胞毒で膜破壊型のものが強く働くと、ネクローシス優位の像になりやすくなります。
アポトーシスは、図で描くなら細胞が縮み、核が凝縮し、小さな断片に整理されて処理される流れです。
膜は終末期まで比較的保たれ、周囲に中身をぶちまけにくいため、炎症はネクローシスほど前面に出ません。
ミトコンドリア障害、DNA 損傷、成長因子シグナルの遮断などが引き金となり、カスパーゼのカスケードが進みます。
抗がん剤や放射線、各種ストレスによる細胞死でよく問題になるのはこちらです。
両者の違いは、単なる形態学の分類にとどまりません。
ネクローシスは炎症性帰結を伴いやすく、アポトーシスは比較的静かに片づくという差があります。
同じ「細胞が減った」という結果でも、組織レベルではその後の反応が変わります。
毒素学の現場でこの区別が必要になるのは、病変の広がりや、炎症を介した二次被害を見積もるためです。
もっとも、現実の細胞は教科書ほど整然とは死にません。
膜障害で始まりつつ、まだ生き残った細胞群ではカスパーゼ経路が回ることがありますし、代謝阻害が進んだ末にアポトーシスの実行に必要な ATP すら足りなくなってネクローシス様に崩れることもあります。
培養皿の上でも、同じウェルの中に縮んだ細胞と膨れた細胞が混在する像は珍しくありません。
細胞毒を「一つの死に方を起こすもの」と決め打ちしないほうが、観察像とデータのズレを説明できます。
ℹ️ Note
細胞死を読むときは、「膜が先に破れたのか」「代謝が落ちてから自殺プログラムに入ったのか」を分けると、ネクローシス優位かアポトーシス優位かが見えてきます。炎症が強い組織障害か、比較的静かな細胞減少かという違いも、この入口の差から説明できます。
細胞毒性試験(LDH/MTT/ATP)の読み方
細胞毒性試験では、何を“死”の指標にしているかを外すと解釈を誤ります。LDH、MTT、ATP 定量はどれも定番ですが、見ている現象は同じではありません。
LDH 放出法は、膜が破れて細胞内酵素が培地へ漏れた量を測る方法です。
したがって、膜障害やネクローシス寄りの傷害に敏感です。
溶血毒、膜作用性ペプチド、界面活性剤のような試料では変化が出やすく、短時間の急性障害も拾えます。
反対に、代謝は落ちていても膜がまだ保たれている段階では、LDH はあまり上がりません。
MTT や XTT は、生きた細胞の還元能、言い換えれば代謝活性を見ています。
ミトコンドリア由来の還元反応が中心になるため、エネルギー代謝が落ちる処置では早めに低下します。
膜が無事でも、細胞が弱っていればシグナルは下がります。
抗増殖作用と細胞死が混ざって見えるのもこの系の特徴です。
細胞数が減ったのか、1個あたりの代謝が落ちたのかを切り分けないと、結果の意味がぶれます。
ATP 定量は、細胞内エネルギー残量を直接に近い形で読みます。
エネルギー代謝障害に鋭敏で、細胞数の変化とも相関しやすい一方、ミトコンドリア機能に強く依存する処置では早い段階から低下します。
シアン化物のような代謝阻害、あるいはミトコンドリア毒性が前景にある条件では、ATP はとても素直に落ちます。
ただし、それが即座の膜破綻や不可逆的な死と同義とは限りません。
実務で厄介なのは、同じサンプルでも LDH と MTT が一致しない場面があることです。
安全性試験や保護薬効評価でよく出会うのは、保護候補物質を加えると LDH 放出は下がるのに、MTT の回復は鈍い、あるいはその逆というパターンです。
前者は膜破綻を抑えていても代謝の立て直しが追いついていない像、後者は代謝活性は持ち直していても一部の細胞では膜障害が残っている像として読むと納得がいきます。
私自身、培養神経系のデータを読むときは、MTT が改善したから保護されたと即断せず、LDH や形態観察を並べて、どの層が救われたのかを切り分ける癖がつきました。
方法が違えば、救っている相手も違うからです。
このズレは失敗ではなく、毒性の階層が違うことを教えてくれる情報です。
膜、代謝、ATP、増殖、カスパーゼ活性、核形態はそれぞれ別の窓です。
細菌性細胞毒のように膜障害が主役なら LDH が前に出ますし、合成阻害やミトコンドリア障害が主役なら MTT や ATP が先に落ちます。
ひとつのアッセイだけで「細胞毒性の全貌」を決めるのでなく、何を壊している毒なのかに合わせて読み分けることが、cytotoxin と cytotoxicity の両方を正しく理解する近道です。
3分類を代表例で比較する
代表例の比較表
三つの分類は言葉だけで覚えると混線しますが、代表例を横に並べると、どこを壊してどんな症状に結びつくのかが見えてきます。
私は初学者向けの原稿をまとめるとき、まず「症状の違い」を並べるのではなく、「分子標的の違い」を先に表に置くようにしています。
その順番にすると、麻痺、出血、細胞死がばらばらの現象ではなく、標的の違いから連続的に読めるからです。
| 分類 | 代表例 | 主標的 | 分子標的・主機序 | 主要症状 | 定量データ | 研究・応用 |
|---|---|---|---|---|---|---|
| 神経毒 | テトロドトキシン | ニューロン、神経線維 | 電位依存性 Na+ チャネル遮断 | しびれ、伝導停止、筋力低下、麻痺 | ロブスター巨大神経線維で活動電位遮断が約94 nM。ベラトリジン系に対する保護作用 IC50 は 30 nM | イオンチャネル研究、神経生理学の古典的ツール |
| 神経毒 | ボツリヌス毒素 | 神経筋接合部 | 神経伝達物質放出装置の切断によりアセチルコリン放出を阻害 | 弛緩性麻痺、複視、嚥下障害、呼吸筋麻痺 | LD50 0.001 μg/kg の例示があるが、品質ガイド上の参考値であり原典の再確認が必要 | 神経筋接合部研究、医療用途では局所投与製剤としても利用 |
| 出血毒の代表 | クサリヘビ毒 | 血管内皮、基底膜、凝固系、周辺組織 | SVMP による基底膜・細胞外マトリックス分解、SVSP による凝固攪乱、PLA2 などによる組織障害 | 腫脹、皮下出血、血疱、組織壊死、凝固異常 | 単一の代表 LD50 はここでは示せません。毒液は多成分混合物で、成分ごとに作用点が異なるためです | 凝固研究、出血機序解析、抗毒素評価 |
| 細胞毒の代表 | 細菌性細胞毒 | 細胞膜、細胞内小器官、合成系 | 膜破壊、代謝阻害、タンパク質合成阻害、アポトーシス/ネクローシス誘導 | 細胞死、炎症、局所組織障害、臓器障害 | グルタミン酸は 500 μM で、培養神経細胞の大半が 24 時間後に死滅 | 感染症研究、安全性評価、細胞死の機序解析 |
| 境界事例 | マイトトキシン | 細胞膜、イオン恒常性 | 強い膜作用と Ca2+ 恒常性破綻を介した全身毒性 | 興奮性異常、循環・筋・神経系の重篤障害 | (マウス、腹腔内投与の報告例)LD50 は 0.05 μg/kg | 単純な神経毒・細胞毒の二分法に収まらない高毒性事例 |
この表で見たいのは、同じ「強い毒」でも止めているものが違うという点です。
テトロドトキシンは電気信号そのものを走らせなくし、ボツリヌス毒素は神経終末からの伝達物質放出を止めます。
どちらも麻痺を起こしますが、前者は配線の電流を遮断し、後者は配線の末端でメッセージを渡せなくする毒です。
一方、クサリヘビ毒は血管壁や凝固系を壊すので、前面に出るのは麻痺ではなく出血、腫脹、壊死です。
細菌性細胞毒では、そもそも細胞そのものが破綻するため、局所炎症や組織障害という景色になります。

症状が異なる理由
初学者が混同しやすいのは、「麻痺も重症、出血も重症、細胞死も重症なのだから、全部まとめて危険な毒でよいのではないか」という感覚です。
実際には、症状の見え方は毒の“強さ”より、どの階層を攻撃しているかで分かれます。
テトロドトキシンでは Na+ チャネルが塞がれるため、活動電位が立ちません。
すると感覚神経ではしびれ、運動神経では筋収縮の指令が届かず、結果として麻痺が出ます。
ここで壊れているのは主に情報伝達です。
組織が目に見えて溶けるわけではないので、外から見た局所所見は派手ではありません。
ボツリヌス毒素も神経毒ですが、標的はチャネルではなくシナプス終末の放出装置です。
神経は発火しても、筋肉へアセチルコリンを渡せないので弛緩性麻痺になります。
見かけの症状がテトロドトキシンと近くても、分子レベルでは止めている場所が一段階ずれています。
編集の現場では、この「似た症状でも詰まっている場所が違う」という線を入れておくと、読者の理解が急に安定します。
クサリヘビ毒では景色が一変します。
主役のひとつである SVMP は血管基底膜や細胞外マトリックスを分解し、血管の支えを崩します。
そこに凝固系を乱す成分や、拡散を助ける成分、筋障害を起こす PLA2 系成分が重なると、局所では腫脹や血腫、全身では出血傾向や消費性凝固障害に向かいます。
つまりここで壊れているのは神経の配線ではなく、血管と止血システムの構造です。
症状が赤い、腫れる、壊死するといった方向へ寄るのは当然の帰結です。
細菌性細胞毒はさらに広いカテゴリーで、膜を破るもの、代謝を止めるもの、合成系を止めるものが含まれます。
見えてくる症状は、細胞が壊れる場所と数に依存します。
局所感染なら壊死や炎症、全身に回れば多臓器障害という形を取ります。
神経毒のように「配線のトラブル」として捉えるより、細胞そのものが脱落していく障害として読むほうが筋が通ります。
マイトトキシンは、この整理に対するよい境界事例です。
神経毒と細胞毒をきれいに分けたくなる場面でも、現実の毒は Ca2+ 恒常性や膜機能を広い範囲で破綻させ、神経・筋・循環の症状をまたいで現れます。
分類は理解の地図として便利ですが、毒そのものがその枠に従ってくれるわけではありません。
用量指標(LD50/IC50)の注意点
比較表に数値を入れると説得力が増す一方で、読み方を誤ると別の誤解を生みます。
LD50 と IC50 はどちらも毒性の強さを示す指標として使われますが、同じ土俵の数字ではありません。
IC50 は、ある実験系で作用を半分にする濃度です。
テトロドトキシンの 30 nM は、ベラトリジン系の神経毒性に対して保護作用を半分まで示す濃度で、細胞系の現象を読んでいます。
約94 nM という活動電位遮断の値も、ロブスター巨大神経線維という古典的な神経生理実験の条件で得られた数字です。
ここからわかるのは、テトロドトキシンが低濃度で Na+ チャネル機能を変えることですが、それをそのまま全身毒性の大小に読み替えることはできません。
LD50 は半数致死量で、動物個体にどれだけ投与すると半数が死亡するかという指標です。
マイトトキシンの 0.05 μg/kg はマウス腹腔内投与の値であり、ボツリヌス毒素の 0.001 μg/kg という数字は例示として流通しているものの、ここでは品質ガイド上の参考値として扱うのが妥当です。
原典の再確認が必要な数値を、確定値として扱うのは避けるべきです。
表の数字を横一列に見て「どれが最強か」と決めたくなりますが、その読み方では肝心の条件が抜け落ちます。
動物種、投与経路、測定系、観察時間、評価項目が違えば、数値の意味は変わります。
腹腔内投与の LD50 と、培養細胞での IC50 を並べて大小比較しても、片方は個体レベルの致死、もう片方は in vitro の作用濃度です。
単位が似ていても、見ている世界が違います。
⚠️ Warning
LD50 は「どれだけで死ぬか」、IC50 は「どれだけで半分効くか」を示します。数字の桁だけで優劣を決めるのでなく、何に、どう入れて、何を終点にした数値かまで含めて読むと、比較表が単なる強さランキングではなくなります。
細胞毒の数字でも同じことが言えます。
グルタミン酸 500 μM で培養神経細胞の大半が 24 時間後に死滅するというデータは、興奮毒性の強さを示すには有用ですが、これは細胞培養系の時間依存データです。
急性の致死量を示しているわけではありません。
私は比較表を組むとき、初学者がここで迷子になりやすいと感じています。
そこで、数値の欄にはできるだけ「何の系で測った値か」を一緒に書き、安易な横比較を止める設計にしています。
毒性の比較は数値を並べる作業ではなく、条件の違いごと並べる作業だからです。
この分類はどこまで有効か|複合毒と例外
ヘビ毒の複合性
ヘビ毒を神経毒と出血毒に二分して覚えると、入口としては便利です。
ところが実際の毒液は、ひとつのラベルで収まるほど単純ではありません。
クサリヘビ類の毒だけを見ても、血管基底膜を崩すSVMP、凝固系を乱すSVSP、筋障害や膜障害に関わるPLA2、さらに組織内への広がりを助けるヒアルロニダーゼが同時に入っています。
症状はその混合比で決まり、神経症状が前景に出るか、出血や腫脹が前景に出るかも、単一成分ではなくカクテル全体の設計で変わります。
この視点に立つと、毒蛇咬傷のレビューで繰り返し指摘される「同じ種なのに症状がぶれる」という現象も理解しやすくなります。
私はこの記述に触れるたび、診断名の揺れというより、毒組成の揺れが臨床像に投影されているのだと考えるようになりました。
同一種でも、ある地域の個体では出血傾向が目立ち、別の地域では筋障害や神経症状が前に出ることがあります。
そこには個体差だけでなく、地理差、成長段階による年齢差が反映されます。
幼若個体と成体で獲物が変われば、選択される毒の成分比も変わり得ます。
教科書の分類が静的なのに対して、自然の毒液は動的です。

臨床像が混ざるのは、分類が間違っているからではありません。
分類が見ている軸が粗いからです。
たとえば「出血毒」と呼ばれるヘビ毒でも、実際には局所で筋壊死を起こし、横紋筋融解症に近い所見を伴うことがあります。
逆に「神経毒性の強いヘビ」とされる種でも、局所壊死や循環器系への影響が無視できない例があります。
つまり、神経毒か出血毒かを問うだけでは、患者に起きている病態の全景を描けません。
この視点に立つと、毒蛇咬傷で症状がぶれるのは分類が誤りというより、毒組成の揺れが臨床像に反映されているためだと理解できます。
3分類の外側にある周辺分類
この限界を埋めるために、毒性学では周辺分類が使われます。
代表的なのが筋肉毒(ミオトキシン)です。
これは骨格筋細胞を標的にし、筋細胞膜の破壊やカルシウム流入の増加、あるいはPLA2活性による膜リン脂質分解を通じて筋壊死を起こします。
臨床では筋痛、筋力低下、ミオグロビン尿、CK上昇という形で見えてきます。
「出血毒の一部」として片づけるより、筋を直接壊す成分として切り出したほうが病態に合います。
心毒性も三分類からこぼれやすい領域です。
コブラ毒に含まれるcardiotoxinは、名前の通り心筋に作用するだけでなく、骨格筋膜にも直接作用し、膜脱分極や膜障害を介して筋線維を傷つけます。
ここでは神経伝達の遮断より、興奮膜そのものの障害が本体です。
症状だけ眺めると神経筋のトラブルに見えても、実際の標的は神経ではなく膜そのものということがあります。
さらにヘパトトキシンのような分類もあります。
アマトキシンはRNAポリメラーゼIIを阻害してタンパク合成を止め、遅れて肝細胞壊死を起こします。
これは神経毒でも出血毒でもなく、広義の細胞毒に含めることはできますが、臓器特異性を前面に出して「肝毒性」と呼ぶほうが病態の像がはっきりします。
毒の現場では、どの細胞を壊すかだけでなく、どの臓器に傷害が集中するかも同じくらい意味を持ちます。
こうした周辺分類を入れると、三分類は「間違い」ではなく「粗い地図」だったと見えてきます。
入口では神経毒・出血毒・細胞毒で十分でも、実際の病態を追う段階では、ミオトキシン、cardiotoxin、ヘパトトキシンのような補助線がないと景色がぼやけます。
💡 Tip
ヘビ毒を読むときは、毒全体に一枚ラベルを貼るより、どの成分が血管、筋、神経、凝固系にどう分担しているかを見ると、症状の混ざり方に筋道が通ります。
境界事例から学ぶ再分類の視点
境界事例として典型的なのがマイトトキシンです。
この毒は細胞膜レベルでCa2+流入を促進し、筋の異常収縮、膜障害、細胞死を引き起こします。
見かけ上は神経・筋・循環の症状をまたぐため、「神経毒か細胞毒か」という問い自体が少しずれています。
主軸にあるのはカルシウム恒常性の破綻で、そこから筋異常収縮も細胞障害も派生してくるからです。
分類名を一つ選ぶより、分子標的を先に置いたほうが現象を正確に追えます。
シアン化物も同じことを教えてくれます。
急速に致死的になり得るので神経症状ばかり注目されがちですが、一次標的はニューロンそのものではなく、ミトコンドリア電子伝達系のシトクロムcオキシダーゼです。
細胞が酸素を使えなくなり、ATP産生が止まり、代謝の高い組織から崩れていきます。
これは神経毒というより、細胞呼吸阻害による細胞毒性として置くほうが筋が通ります。
脳症状が強いのは、脳がエネルギー欠乏に弱いからです。
この見方を広げると、従来の分類は「症状ベース」、再分類は「分子標的ベース」と言えます。
神経毒、出血毒、細胞毒という語は臨床像を素早くつかむのに向いています。
一方で、イオンチャネル阻害、シナプス放出阻害、基底膜分解、膜リン脂質分解、ミトコンドリア呼吸阻害、RNAポリメラーゼ阻害といった軸で並べ替えると、境界事例の居場所が定まります。
私自身、毒を解説するときは、まず大きな三分類で輪郭を出し、その後に「どの分子装置を止めたのか」「どの細胞系が先に破綻したのか」で見直すようにしています。
この二段構えにすると、同じヘビ毒で症状がそろわない理由も、マイトトキシンのような例外が分類を壊しているのではなく、分類の解像度を上げる必要を示しているだけだと見えてきます。
毒の研究が科学と医学をどう進めたか
化学ツールの誕生とチャネル研究
毒の研究が基礎科学を前に進める場面では、まず「生体を壊す分子」としてではなく、特定の機能だけを切り出して止める道具として価値が立ち上がります。
薬理学ではこの流れが繰り返し現れます。
ある毒素がひとつの分子装置を選択的に止める。
すると、その装置が本当にその生理機能を担っているのかを検証できる。
そこで標的妥当性が固まると、次は毒素そのものではなく、扱いやすく調整しやすい薬へと橋渡しが始まる。
基礎研究から医療応用までの典型的なパスは、機能阻害、標的妥当性、創薬という三段階で整理すると見通しがよくなります。
その古典例がテトロドトキシンです。
TTXは電位依存性Na+チャネルを鋭く見分けて遮断するため、活動電位という神経の基本現象を、ほかの膜機能から切り分けて観察できるようにしました。
神経生理学の歴史でTTXの意義が大きいのは、単に強い毒だからではありません。
Na+電流だけを静かに消して、何が残るかを見せたことにあります。
ロブスター巨大神経線維で活動電位を遮断した古典実験は、その後のチャネル生理学の座標軸になりました。
研究史の整理にはTetrodotoxin—A brief history—PMCがまとまっています。
私自身、薬理学を学び始めた頃にTTXの位置づけを理解して、毒の見え方が変わりました。
毒は「危険物」でもありますが、研究室の文脈では、生体の複雑さを一段だけ静かにするための精密工具でもあります。
遺伝子改変や構造生物学が発達した今でも、化学ツールの強みは即効性と可逆性、そして実験系をまたいで比較できる点にあります。
チャネルを一つ止めたときに神経発火が消えるなら、そのチャネルは飾りではなく、回路の成立条件そのものだったとわかります。

TTXはその後、Na+チャネルのサブタイプ差やTTX感受性・抵抗性の概念整理にもつながりました。
ここからチャネロパチー研究が伸びていきます。
てんかん、不整脈、疼痛、筋疾患の一部は、チャネル蛋白の異常を通じて理解されるようになりましたが、その土台には「どの電流を止めると何が消えるか」を確かめる古典薬理があります。
選択性の高い毒素は、病態をいきなり治す薬ではなくても、何を狙えば病態を動かせるかを先に教えてくれるのです。
この流れは、次節のコノトキシン研究がCaVチャネルの機能分化や疼痛研究に与えた影響へとつながります。
Na+チャネル研究でTTXが果たした役割に対応するものとして、Ca2+チャネル研究ではコノトキシン群が大きな足跡を残しました。
とくにω-コノトキシンは電位依存性Ca2+チャネルのサブタイプを機能的に切り分けるうえで決定的であり、その知見が疼痛研究や標的選定に直接結びつきました。
この地図化が疼痛学へ直結した点が面白いところです。
神経終末へのCa2+流入が止まれば、興奮性伝達物質や神経ペプチドの放出も落ちます。
すると痛みの入力が脊髄レベルで弱まる。
つまり、CaVチャネルは単なる電気生理の話ではなく、痛みの伝達量を決めるレバーだったわけです。
ω-コノトキシン由来の知見は、どのサブタイプを抑えれば鎮痛に近づくかを具体的に示し、標的妥当性の輪郭をくっきりさせました。
Ca2+チャネル標的毒素の整理にはω-コノトキシンとCaVチャネルの総説が役立ちます。
ここでも、毒素研究から医療応用への道筋は明快です。
まず天然毒素が標的分子に結びつき、機能を止める。
次に、その阻害で痛み回路がどう変わるかを実験で積み上げる。
そこで「このチャネルを抑えると鎮痛が得られる」という標的妥当性が見える。
そこから薬剤化へ進む。
この順番を踏むと、毒素そのものが即座に万能薬へ変わるわけではない理由も見えてきます。
標的が正しくても、投与経路、分布、持続時間、安全域の設計は別問題だからです。
創薬は、毒素が示した“効く場所”を、人間が扱える形に翻訳する作業だと言えます。
疼痛研究の現場では、こうした毒素は教科書の脇役ではありません。
神経回路のどこでシグナルが減るのか、末梢感作と中枢感作のどちらに効いているのかを追うとき、選択的な阻害分子があるだけで議論の質が変わります。
チャネル研究は分子生物学の洗練で進んだ面も大きいのですが、機能をその場で止めてみせる薬理ツールの説得力は今も強いままです。
ボツリヌス毒素の医療応用
ボツリヌス毒素は、「毒と薬は紙一重」という言葉をもっとも鮮やかに体現する分子のひとつです。
作用点は神経筋接合部で、アセチルコリン放出に必要な装置を切断し、筋を収縮させる命令が末端で途切れるようにします。
毒として見れば弛緩性麻痺を起こす分子ですが、医療ではこの作用を局所的かつ制御された形で利用することで価値が反転します。
過剰な筋収縮や異常な分泌を抑えたい場面では、まさにその遮断作用が治療になるからです。
臨床応用の広がりは神経筋疾患から始まり、痙縮、眼瞼けいれん、斜頸のような不随意運動の制御へと伸び、その後に多汗症や美容領域へも拡大しました。
この広がりを見ていると、薬理作用が一つでも適応は一つではないことがよくわかります。
同じ分子でも、どの筋に、どの深さで、どの程度の局所作用を与えるかによって、治療の意味が変わります。
毒性学の言葉で言えば、ここで実践されているのは用量と局在の制御です。
パラケルススの「用量が毒を決める」という命題は抽象論ではなく、ボツリヌス毒素製剤の臨床そのものに埋め込まれています。
私がこの分子にいちばん科学史的なおもしろさを感じるのは、毒が薬になったという単純な美談ではなく、作用機序が明快だったからこそ医療へ翻訳できた点です。
何を切断し、どの伝達を止め、どこまで局所にとどめるかが薬理学的に整理できていたから、適応も投与設計も積み上げられました。
毒だから危険、薬だから安全、という二分法ではこの展開は説明できません。
危険な分子でも、標的、量、投与部位、製剤化が制御されれば医療資源になる。
逆に言えば、その制御を失えば薬も毒性を前面に出します。
ℹ️ Note
毒素研究が医療へつながるときは、「危険なものを薄めて使う」という発想だけでは足りません。どの分子標的を、どの組織で、どれだけ止めると治療効果になるのかが定義されて、はじめて薬になります。
なお、この領域の2024年から2026年の動向は、原理そのものが短期間で塗り替わる局面ではありません。
新規適応、投与設計、製剤ごとの差異、長期成績の評価といった論点が学会発表やレビューを通じて積み上がっており、更新は連続的に進んでいます。
つまり、TTX、ω-コノトキシン、ボツリヌス毒素に共通する本質はすでに確立していて、現在の焦点は「どこまで精密に使いこなせるか」に移っています。
毒の研究は、生命を壊す分子を恐れるだけでは見えてこない科学の伸び方を、いまも静かに示し続けています。
学びを深めるための次のアクション
ここまで読んだら、比較表に一度戻って、神経毒・出血毒・細胞毒の違いを自分の言葉で言い直してみてください。
私自身、分類を覚えたつもりでも、標的、主機序、症状の向きの3点を口頭で説明しようとすると曖昧さが残ることがよくありました。
そこで、見直すときは「何を壊す毒か」「その結果どんな症状が前面に出るか」「研究では何の道具になったか」の3項目だけを先に確認すると、頭の中の地図が締まります。

当サイトには関連記事がまだありません。
- 神経毒は、神経回路や神経筋接合部の伝達を止める、または乱す分類です。
- 出血毒は、血管壁、基底膜、凝固系の破綻を中心とする分類です。
- 細胞毒は膜、小器官、合成系を傷つけて細胞死へ向かわせる分類か
そのうえで、代表毒を一つずつ取り出し、作用点から症状までの因果をたどる練習に進むと理解が深まります。
テトロドトキシンなら電位依存性Na+チャネル遮断から伝導停止と麻痺へ、ボツリヌス毒素なら神経伝達物質放出阻害から弛緩性麻痺へ、SVMPなら基底膜分解と血管障害から出血へ、アマトキシンならRNAポリメラーゼII阻害からタンパク合成障害と肝細胞壊死へ、という流れです。
症状名だけを暗記するより、分子標的を起点に一本の線で結べるかを確かめるほうが、複合毒や例外に出会ったときにも崩れません。
私は学習後の確認用に、短いフォームのような設問を自分で作ることがあります。
「神経毒を1〜2文で定義してください」「テトロドトキシンで麻痺が起こる因果を、標的分子から説明してください」「SVMPで出血が起こる理由を、血管壁の変化まで含めて書いてください」といった形です。
定義問題と、代表例から症状への因果説明を組み合わせるだけで、用語暗記なのか機序理解なのかがすぐに見分けられます。
特定の代表毒や機序に強く引っかかったなら、その枝をそのまま深掘りすると知識が立体になります。
神経毒の分子メカニズムを追いたいならテトロドトキシンやボツリヌス毒素の系統、遅発性の肝毒性に関心があるならアマトキシン、呼吸鎖阻害の即効性をつかみたいならシアン化物というように、興味のある標的からサブトピックへ降りていく読み方が有効です。
分類を覚える段階から、分子がどこを叩き、なぜその症状になるのかを説明できる段階へ進むと、このテーマは一気に面白くなります。

薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
テトロドトキシンとフグの耐性|なぜ自分の毒で死なないのか
フグが自分の毒で死なない理由は、ひとつではありません。テトロドトキシン(TTX、C11H17N3O8、分子量319.27)を主に外部から取り込みながら、同時に自分の電位依存性Na+チャネルのTTX結合性をアミノ酸置換で下げ、神経と筋の麻痺を避けているからです。
毒ヘビの種類と毒の違い|神経毒と出血毒を比較
「コブラ科は神経毒、クサリヘビ科は出血毒」と覚えると入口はつかめますが、毒性学の論文を読み込むほど、その図式だけでは取りこぼすものが増えていきます。3FTx、PLA2、SVMPといった毒素群の一次論文を概観すると、ヘビ毒は単一の化合物ではなく、タンパク質・酵素・ポリペプチドが混ざり合った複合毒であり、
トリカブトとアコニチン|日本三大有毒植物の科学
春の山菜採りの季節になると、毎年のように名前があがるトリカブトは、特定の一種ではなくAconitum属の総称で、日本ではドクゼリドクウツギと並ぶ「三大有毒植物」として記憶されています。
毒の進化|防御と捕食、盗用と共進化の科学
自然史系の特別展「毒」を歩くと、読者の頭にまず浮かぶのは「どれがいちばん危険か」より、「生きものはなぜ、こんな仕組みを持ったのか」という問いだと思います。この記事は、その疑問に答えるために、まずpoisonを食べたり触れたりして効く毒、venomを牙や針で注入する毒、