アマトキシン|RNAポリII阻害と肝障害の因果線
アマトキシン|RNAポリII阻害と肝障害の因果線
アマトキシン中毒の怖さは、食べた直後ではなく、RNAポリメラーゼIIを止めてmRNA合成を断ち、タンパク質を作れなくなった肝細胞があとから崩れるところにあります。熱や乾燥でも失活しにくいこの“時間差の毒”は、タマゴテングタケやドクツルタケだけでなく、
アマトキシン中毒の怖さは、食べた直後ではなく、RNAポリメラーゼIIを止めてmRNA合成を断ち、タンパク質を作れなくなった肝細胞があとから崩れるところにあります。
熱や乾燥でも失活しにくいこの“時間差の毒”は、タマゴテングタケやドクツルタケだけでなく、Galerina属やLepiota属にもまたがり、通常6時間以降、10〜24時間前後に症状が前面化してから一時的軽快を挟み、肝・腎障害へ進みます。
本記事は、毒キノコのニュースを「危ないらしい話」で終わらせたくない人、とくに分子機序から臨床まで一本の線で理解したい読者に向けた解説です。
分子機序、臓器標的、経過、尿中LFIAやLC-HRMS/MSによる検出、支持療法とシリビニン・N-アセチルシステインの位置づけ、そして2025〜2026年のカリフォルニア集団発生までつなげて読むことで、古典的な猛毒が現代の公衆衛生課題であることが見えてきます。
秋のニュースで「遅れて重症化」という見出しを見たとき、この記事を読んだあとなら、その遅れが偶然ではなく、細胞の中でmRNAとタンパク質が枯渇していく時間と対応していると頭の中で結びつくはずです。
アマトキシンを理解する鍵は、症状の派手さより先に、見えない分子の遅延をつかむことにあります。
アマトキシンとは何か──毒キノコの主要毒をまず整理する
分類と代表成分
アマトキシンは、毒キノコに含まれる環状オクタペプチド毒の総称です。
ここで用語をそろえると、アマトキシンは毒群全体の名前、アマニチンはその中の個々の成分名、α-アマニチンは代表成分のひとつ、という関係になります。
実際の中毒解説でこの3つが混在すると話がぼやけますが、毒性の中心を担う代表としてまず押さえるべきなのはα-アマニチンで、加えてβ-アマニチン、γ-アマニチンが主要成分として並びます。
含有菌の範囲も、Amanita属だけに閉じると実態を見誤ります。
古典的な代表はAmanita phalloides(タマゴテングタケ)やAmanita virosa(ドクツルタケ)、Amanita verna(シロタマゴテングタケ)です。
同じ毒群はGalerina marginataのような小型の朽木性キノコや、Lepiota brunneoincarnataのようなLepiota属の毒性種にも広がっています。
つまり、「白いテングタケ型だけが危険」という理解では足りず、系統の違う複数属にまたがる毒群として捉える必要があります。

量の感覚も持っておくと、毒性の議論が抽象論で終わりません。
アマトキシン含有キノコでは、乾燥した傘組織に総アマトキシンが2〜4 mg/g含まれる例が多いと整理されています。
乾物ベースとはいえ、傘の組織1 gあたりミリグラム単位で主毒が入っている計算です。
ペプチド毒という言葉だけ聞くと、どこか繊細で壊れやすい印象を持ちがちですが、実際には後述するように料理や保存で片づく相手ではありません。
化学構造と性質
代表成分のα-アマニチンは、8個のアミノ酸からなる環状構造を持ちます。
一直線の鎖ではなく、輪になったペプチド骨格が分子の頑丈さを支えている点が特徴です。
この「小さいのに輪で締めた構造」が、アマトキシンの扱いにくさを生んでいます。
タンパク質というより、むしろ壊れにくく設計された小型分子機械に近い振る舞いをすると考えるとイメージしやすいはずです。
性質としてまず外せないのが熱安定性です。
アマトキシンは一般的な加熱調理では失活しにくく、乾燥でも毒性を保ちます。
炒める、煮る、汁物にする、干すといった家庭で思いつく処理を並べても、分子の側は平然と残る、というのがこの毒の厄介なところです。
食経験の浅い人ほど「火を通せば何とかなる」と考えがちですが、アマトキシンではその発想が通用しません。

この構造がなぜ危険な臓器障害につながるのかは、前節で触れた通りです。
アマトキシンは消化管から吸収されたのち、門脈を通って肝臓へ入り、RNAポリメラーゼIIを阻害してmRNA合成を止めます。
細胞から見ると、設計図の写しが作れなくなる状態です。
すると新しいタンパク質が補充できず、代謝の回転が高い肝細胞ほど先に行き詰まります。
症状の立ち上がりが遅れるのは、毒が効いていないからではなく、分子レベルの供給停止が細胞破綻として表面化するまで時間がかかるからです。
共存毒(ファロトキシン/ビロトキシン)との違い
Amanita属の猛毒種では、アマトキシンと並んでファロトキシンやビロトキシンが同じ子実体に共存することがあります。
ただし、中毒の主役として優先順位をつけるなら、臨床的な中心はやはりアマトキシンです。
理由は明快で、ファロトキシンやビロトキシンは消化管からの吸収性が低く、全身毒として前面に出にくいからです。

この違いは、同じキノコの中に入っていても「どの毒が実際に人を重症化させるのか」を分けます。
ファロトキシン類は細胞骨格への作用で毒性学的には興味深い存在ですが、経口中毒の主毒という位置づけではありません。
ビロトキシン類も同様で、名前の強さほど臨床上の比重は大きくないのです。
現場で問題になる遅発性の激しい消化器症状から肝障害へ進む典型像を組み立てているのは、アマトキシン群だと考えるのが筋です。
ℹ️ Note
同じAmanitaに複数の毒群が入っていても、「共存していること」と「主毒であること」は別問題です。経口中毒で致死性の軸を作るのはアマトキシン、という整理にしておくと全体像がぶれません。
なぜ肝臓が狙われるのか──吸収から肝細胞到達まで
消化管吸収と門脈初回通過
アマトキシンが肝臓を主標的にする理由は、作用機序そのものだけでなく、体内への入り方にあります。
経口摂取された毒はまず消化管から吸収され、腸管の静脈血に乗って門脈へ集められます。
門脈は腸から吸収された物質を肝臓へ最初に運ぶ太いルートなので、アマトキシンも全身循環へ広がる前に、まず肝臓で大きな曝露を受けます。

この流れは薬理でいう門脈初回通過の発想で捉えると理解しやすくなります。
飲み込まれた直後の毒は、いきなり全身へ均等に散るのではなく、最初の関門として肝臓に集中して流れ込みます。
肝臓は栄養や異物を仕分ける「税関」のような臓器ですが、アマトキシンではその税関が真っ先に高濃度の荷物を受け取る形になります。
結果として、肝臓が最初の主要標的臓器になります。
ここで起きるのは、単なる通過ではありません。
肝臓は流れてきた物質を積極的に取り込む臓器であり、しかも肝細胞はタンパク質合成が盛んなため、前節で述べたRNAポリメラーゼII阻害の影響をまともに受けます。
消化器症状が前面に出る時間帯があっても、病態の中心は早い段階から肝に形成されているわけです。
臨床で肝障害が軸になるのは、毒の強さだけでなく、吸収後の血流動線が肝臓優位にできているからです。
OATPトランスポーターと肝細胞内移行
門脈で肝臓に届いたアマトキシンは、血液中にあるだけでは十分ではありません。
実際に肝障害を起こすには肝細胞内への取り込みが必要で、この段階で注目されるのが基底側膜にある取り込み輸送体です。
研究は肝取り込み輸送体(OATP 系)が関与することを示唆しており、とくに OATP1B3(および関連輸送体の NTCP)に関するエビデンスが比較的強く示されています。
ただし、OATP1B1 と OATP1B3 の相対的な寄与をヒトの in vivo 条件で定量的に示す決定的データはまだ得られていません。
現時点では、OATP 系の関与が肝選択性を説明する有力な要素であるとしつつ、その定量化は未確定であると慎重に整理するのが適切です。
腎障害などの二次標的
アマトキシン中毒では肝臓ばかりが語られがちですが、障害は肝だけで完結しません。
腎臓も二次標的として障害されうる臓器で、重症例では肝・腎障害が並行して問題になります。
尿中にアマトキシンが検出されることからもわかる通り、毒は腎排泄の経路に乗るため、腎実質も曝露を受けます。
ただし、病態の中心をどこに置くかという話になると、軸はやはり肝臓です。
吸収直後の門脈曝露、OATPを介した肝細胞内移行、そしてRNAポリメラーゼII阻害に対する肝細胞の脆弱性が重なるため、初期から全体像を支配するのは肝障害です。
腎障害はその後景にある合併病変ではなく無視できない所見ですが、最初の主要標的臓器は肝臓という整理は崩れません。
実際の経過でも、激しい下痢や嘔吐のあとに一時的な小康状態を挟み、そこから肝機能悪化が前面化して、必要に応じて腎機能の悪化も加わってきます。
病態を一本の線で見るなら、消化管で吸収された毒が門脈で肝へ集まり、肝細胞へ取り込まれ、そこで細胞障害の主戦場が形成され、その影響が腎を含む他臓器へ広がる流れです。
こう捉えると、アマトキシン中毒が「肝障害を中心に全身化する中毒」であることが見えてきます。

RNAポリメラーゼII阻害という決定打
RNAポリメラーゼIIの役割
アマトキシン中毒の中核は、細胞の「エネルギーが奪われる」ことでも「膜が直接溶ける」ことでもありません。
決定打になるのは、RNAポリメラーゼIIが止められることです。
この酵素は、DNAに書かれた遺伝情報を読み取り、mRNA(メッセンジャーRNA)という形に写し取る役割を担います。
mRNAは、いわばタンパク質を作るための作業指示書です。
細胞の中では、DNAそのものが毎回工場の現場に持ち出されるわけではありません。
まずDNAの情報をmRNAに転写し、そのmRNAをもとにリボソームがタンパク質を合成します。
流れを単純化すると、こうなります。
DNA → mRNA → タンパク質
この真ん中にあるmRNAが途切れると、細胞は新しいタンパク質を補充できません。
肝細胞では、代謝酵素、膜輸送体、解毒に関わる分子、細胞骨格を保つタンパク質まで、常に作っては入れ替える作業が続いています。
前節で見た通り、アマトキシンは血流と輸送体の条件が重なることで肝細胞内に入り込みます。
そこでRNAポリメラーゼIIが止まると、肝細胞は設計図の複製ができない工場になってしまいます。
ここで押さえたいのは、DNAが無事でも細胞は助からないという点です。
設計図の原本が金庫に残っていても、現場へ配るコピーが作れなければ生産は止まります。
アマトキシン中毒が遅れて悪化するのは、この「コピー停止」がじわじわ効いてくるからです。
α-アマニチンの選択的阻害
アマトキシンの中でも、病態の説明で軸になるのがα-アマニチンです。
これはRNAポリメラーゼIIを選択的に阻害し、mRNA合成を止めます。
細胞内で無差別に何でも壊す毒ではなく、転写という生命維持の要所を狙い撃ちするタイプの毒だと捉えると、本質が見えます。
「選択的」という言い方は、影響が小さいという意味ではありません。
むしろ逆で、最も止めてはいけない工程をピンポイントで止めるため、結果が深刻になります。
細胞は多くの障害に対して一時的な代償ができますが、mRNA供給が断たれると、新規タンパク質を作る回路そのものが詰まります。
肝細胞のように合成と代謝の回転が速い細胞では、この打撃が致命傷になりやすいのです。
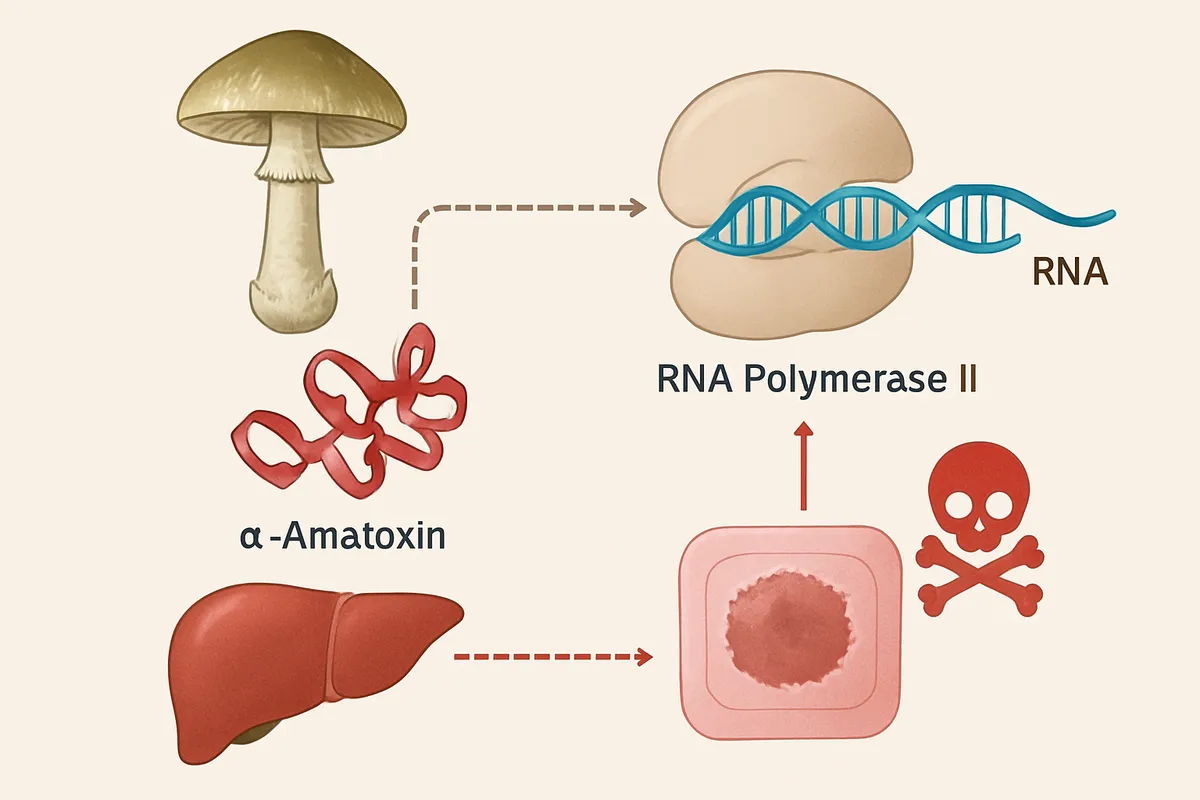
図式化すると、因果関係は次のように整理できます。
α-アマニチン結合 → RNAポリメラーゼII阻害 → mRNA合成停止 → 新しいタンパク質が補充されない → 代謝維持に必要な部品が欠ける
この流れがアマトキシン中毒の「本丸」です。
消化器症状や臓器障害は臨床像として目に入りますが、その背後では、細胞レベルで転写停止が静かに進んでいます。
見た目に派手な破壊ではなく、補給線を断つ毒だと考えると、遅発性の重症化ともつながります。
ℹ️ Note
α-アマニチンの怖さは、細胞をその場で爆発させることではなく、新しいタンパク質を一切補給できない状態に追い込む点にあります。工場の機械を壊すというより、設計部門を停止させる毒です。
mRNA欠乏→タンパク質枯渇→細胞死のカスケード
RNAポリメラーゼIIが止まっても、細胞はその瞬間に崩れるわけではありません。
なぜなら、細胞内にはすでに作られたタンパク質の「在庫」があるからです。
ここが、アマトキシン中毒で時間差を伴って悪化する理由です。
転写停止の直後は、既存の酵素や構造タンパク質がまだ働いています。
ところが在庫は永遠には持ちません。
使われ、分解され、入れ替えが必要になった時点で補充不能が表面化します。
流れを一本の線で書くと、こうなります。
DNAは残る → mRNAが作れない → 新規タンパク質合成が止まる → 既存タンパク質の在庫が減る → 代謝系が順に止まる → 細胞の恒常性が崩れる → 細胞死に至る
この「代謝系が順に止まる」という部分が肝障害の実体です。
肝細胞は、糖代謝、脂質代謝、胆汁関連の輸送、解毒反応、アンモニア処理など、多数の工程を同時並行で回しています。
どれか一つの酵素が切れるだけでも負荷になりますが、mRNA欠乏では複数の系が時間差で傷みます。
するとATP産生、膜機能、イオンバランス、酸化還元の維持まで崩れ、細胞は回復不能の段階に入ります。
細胞死の形式も一様ではありません。
まだ制御が保たれている段階ではアポトーシスの方向へ進み、傷害が深くなってエネルギーも尽きると壊死の比重が増します。
つまり、最初は「静かに片づけられる死」に向かっていた細胞が、補給断絶と代謝破綻が進むにつれて「破綻したまま崩れる死」へ押し流されるわけです。
臨床でみる遅発性の肝不全は、この分子カスケードの帰結です。
摂取直後に何事もないように見える時間があっても、その裏では転写停止が始まり、mRNAが減り、タンパク質の在庫が減り、代謝の足場が抜け落ちています。
アマトキシン中毒が危険なのは、症状の時間経過が毒の作用開始と一致しないからではなく、転写阻害から細胞崩壊までに一段ずつ段差があるからです。
ここを理解すると、なぜ肝細胞が「あとから」一気に持ちこたえられなくなるのかが見えてきます。
症状が遅れて現れる理由──偽回復期をどう理解するか
アマトキシン中毒の時系列像
アマトキシン中毒の厄介さは、食べてすぐ倒れるタイプではないことにあります。
典型像では、摂取直後は目立った症状が出ず、まず潜伏期をはさみます。
この無症状の時間は文献によって幅がありますが、通常は6〜24時間前後で、さらに長めに記載されることもあります。
ここで「半日近く何もないなら軽いのでは」と見えてしまうのが落とし穴です。
その後に前景化するのが、激しい消化器症状です。
急な嘔吐、水様性の下痢、腹痛がまとまって出て、脱水を伴うこともあります。
臨床経過としては、まずこの段階が最も派手に見えます。
毒が直接その場で全身を壊しているように感じられますが、実際には前節までで見た転写停止のダメージが、まだ臓器不全として表に出きっていない時期でもあります。
さらに紛らわしいのが、一時的に症状が軽くなる時間帯があることです。
吐き気や下痢が落ち着き、本人も周囲も「峠を越えた」と受け取りやすい。
この段階がいわゆる偽回復期です。
名称どおり、回復に見えても病態の中心は終わっていません。
むしろ細胞レベルでは、肝細胞や腎臓の障害が静かに進行していることがあります。
そこから数日たって、3〜5日目前後に肝障害と腎障害がはっきりしてきます。
記載によっては4〜5日目を強調するものもあり、時系列にはある程度の幅がありますが、流れとしては共通です。
消化器症状のあとに一瞬静かになり、その後に肝・腎障害が前面に出る。
この時間差が、アマトキシン中毒を臨床的に読みにくくしている核心です。
偽回復期のメカニズム的説明
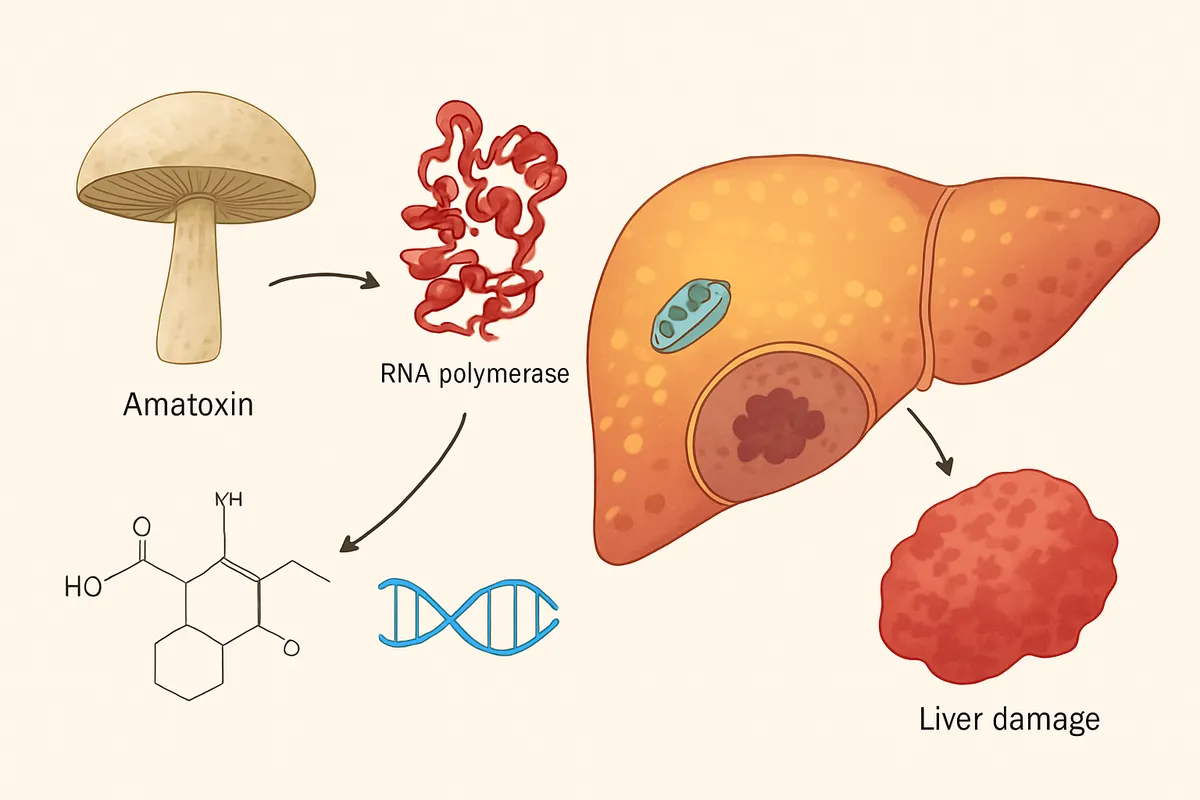
偽回復期を理解する鍵は、「毒の作用開始」と「臓器が壊れたと見える時点」が一致しないことです。
アマトキシンは肝細胞に取り込まれたあと、RNAポリメラーゼIIを阻害してmRNA合成を止めます。
ところが、転写が止まった瞬間に細胞が崩れるわけではありません。
細胞内には、すでに作られていた酵素や構造タンパク質、輸送体といった既存タンパク質の在庫が残っているからです。
言い換えると、工場の設計室が閉まっても、倉庫の部品が残っているあいだは現場が少し動いてしまう、ということです。
肝細胞も同じで、新しいmRNAを作れなくなっても、既存のタンパク質がしばらく機能するため、症状は遅れて表面化します。
これが摂取後すぐではなく、6〜24時間ほどたってから初発症状が出る生物学的な背景です。
では、なぜ消化器症状が先に目立ち、そのあと一時的に軽快するのでしょうか。
初期の嘔吐や下痢には、消化管への直接的な刺激や、共存しうる他の毒成分の関与が論じられることがあります。
一方で、病態の本丸であるアマトキシンの転写阻害は、その裏で進み続けています。
消化器症状が落ち着いても、肝細胞の中では「補給不能」が解消していないため、見かけの改善と実際の障害進行がずれてしまいます。
偽回復期とは、症状が引いた時間ではなく、細胞の在庫が尽きるまでの猶予時間と捉えると実態に近づきます。
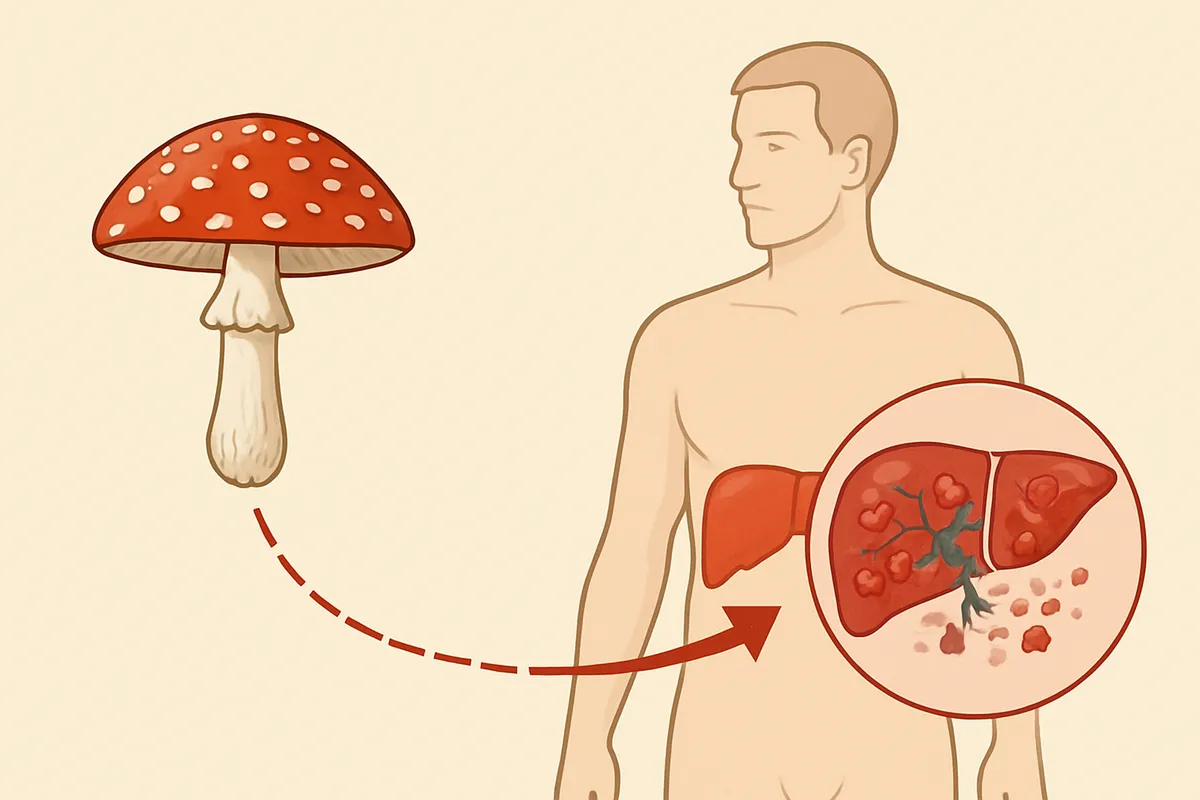
💡 Tip
偽回復期は「治ってきた時間」ではなく、転写停止の影響が臓器機能低下としてまだ出そろっていない時間です。臨床で厄介なのは、患者の体感と細胞内で起きていることが逆向きに見える点にあります。
このため、アマトキシン中毒では静かな時間ほど安心材料になりません。
むしろ、症状の波が引いたように見える局面こそ、肝障害が血液検査で姿を現し始めることがあります。
遅発性という言葉は単なる観察結果ではなく、既存タンパク質が尽きるまで機能が保たれるという分子レベルの事情に支えられています。
重症化のサイン
重症化を見分けるうえで目を向けるべきなのは、消化器症状の強さそのものより、臓器障害が検査値として立ち上がってくる流れです。
アマトキシン中毒では、偽回復期のあとにAST・ALTの上昇がはっきりしてきます。
これは肝細胞傷害が表面化してきたサインで、見かけの体調よりも病態をよく映します。
肝障害が進むと、単に酵素が上がるだけでは済みません。
肝臓は凝固因子を作る臓器でもあるため、凝固異常が出てきます。
ここまで進むと、肝細胞が「傷んでいる」段階から「機能を維持できない」段階へ傾いていることを意味します。
偽回復期のあとに検査値が悪化していく経過は、まさに転写停止の帰結が臓器機能不全へつながってきた形です。
腎障害にも注目が必要です。
アマトキシンは肝臓だけでなく腎臓も標的になり、経過の後半で腎機能の悪化が加わることがあります。
血液検査で腎機能指標が悪化してくる、尿量が落ちる、といった変化は、病態が全身的な臓器障害へ広がっていることを示します。
臨床像としては、消化器症状→見かけの軽快→肝酵素上昇・凝固異常・腎機能悪化という並びで理解すると、アマトキシン中毒の危険な時間差がつかめます。
この経過で怖いのは、本人の自覚が検査所見に追いつかない場面があることです。
吐き気や下痢が引くと「楽になった」と感じても、血液の側では肝不全への坂を下り始めていることがある。
アマトキシン中毒の重症化サインは、体感の改善ではなく、肝・腎の機能が数日遅れで崩れてくること自体にあります。
アマトキシンを含む代表的なキノコ
Amanita属
アマトキシンを語るとき、まず具体名として挙がるのがAmanita属です。
なかでも代表格はタマゴテングタケ(Amanita phalloides)で、世界的に見ても致命的中毒の中心にある種として扱われます。
和名に「タマゴ」とつきますが、幼菌期の丸い外観だけを手がかりにすると危険で、成長すると傘・ひだ・つば・つぼがそろった典型的なテングタケ型になります。
広葉樹林下に発生することで知られ、海外文献では“death cap”として定着しています。

国内の行政資料で繰り返し整理されているのは、ドクツルタケ(Amanita virosa)と、白色の猛毒種としてまとめられるシロタマゴテングタケ(Amanita verna)を含む“Destroying angel”群です。
これらは白く端正な見た目をしており、いかにも危険そうというより、むしろ清潔感のある外観のせいで油断を誘います。
ドクツルタケは日本でも知名度が高く、厚生労働省の自然毒資料でもアマトキシン類を含む代表的毒キノコとして扱われています。
シロタマゴテングタケも同様にアマトキシン類とファロトキシン類を含む種として整理され、白色テングタケ類の識別が事故防止の要所になっています。
この属が厄介なのは、危険種が「いかにも毒キノコ」に見えないことがある点です。
白色のAmanita属は、採取者の頭の中で「白くて上品な食用きのこ」という先入観と結びつきやすく、食用のハラタケ類や若い個体の別種と取り違えられます。
しかも、幼菌では全体がつぼに包まれていて特徴が十分に出そろわず、成長段階によって印象が変わります。
見分けの理屈を知っていても、実地では「一つの特徴だけで決める」同定が破綻しやすいのです。

💡 Tip
Amanita属の猛毒種では、白色・つば・つぼ・白いひだという組み合わせがよく話題になりますが、現場ではこの“定番特徴”だけで安全判定に進むと危険です。問題は特徴を知っているかどうかより、似た種がその場で同じ顔をしてしまうことにあります。
Galerina属
Galerina属は、Amanita属ほど一般名が広く浸透していない一方で、アマトキシン中毒の実地リスクという意味では見逃せないグループです。
代表として挙がるのがGalerina marginataで、日本語資料ではヒメアジロガサの名が使われます。
文献や流通外の俗称ではニガクリタケと混同的に呼ばれることもありますが、名称のぶれ自体がこの属の危うさを物語っています。
小型で褐色系の地味な見た目をしており、派手な警告色はありません。
この属のポイントは、朽木や材の上に出る朽木性菌だということです。
山奥の天然林だけではなく、倒木、切り株、木材片、庭木まわりの腐朽材にも発生しうるため、採取の場面が日常空間に近づきます。
つまり、「危険なのは深い山の特殊なキノコ」という感覚が通用しません。
庭や公園、ウッドチップ周辺で見つかる小型のきのこでも、アマトキシンを含むグループが紛れてくるわけです。

見た目のうえでは、褐色の小型きのこは食用・非食用・有毒が入り乱れていて、属まで絞るだけでも簡単ではありません。
しかもGalerina属は、ナメコ様、センボンイチメガサ様、朽木に出る食用小型種のイメージと重なりやすく、採取者が「いつもの雑きのこ」と見流す余地があります。
アマトキシンというと白いテングタケ類ばかりが記憶に残りがちですが、木の上に出る茶色い小型種にも同じ系統の毒があるという点は、実地ではむしろ印象に残しておくべき部分です。
Lepiota属
Lepiota属は、属全体のすべてがアマトキシンを持つわけではありません。
それでも中毒の解説でこの属が注意対象として挙がるのは、一部の小型カラカサタケ類にアマトキシン含有種が含まれるからです。
代表例として知られるのがLepiota brunneoincarnataで、海外では致命的中毒例と結びつく種としてしばしば言及されます。
国内では和名が広く統一されているとは言いにくく、一般向けには「Lepiota属の毒性種」として把握されることが多いグループです。

この属で注意が必要になる背景には、小型のカラカサタケ型きのこが身近で、しかも“食べられそう”に見えるという事情があります。
傘が開き、中央がやや濃色で、ひだがあり、柄に細いつばが見える。
こうした形は、きのこ図鑑を眺めた経験がある人ほど「カラカサタケの仲間らしい」と受け取りやすいのですが、その“らしさ”が安全性を保証しません。
むしろLepiota属では、食用の大型カラカサタケ類のイメージが先に立つぶん、小型種の危険が見えにくくなります。
行政資料や中毒情報の整理で一貫しているのは、属名だけで安心も危険判定もできないのに、属内に致命的な例外がいるという点です。
これがLepiota属を厄介にしています。
見た目の輪郭だけなら「白っぽいひだを持つ小型カラカサタケ」で終わってしまうものが、実際には毒成分の面で別物ということが起こります。
三つの属を並べると、アマトキシン中毒の誤食リスクは「猛毒種が珍奇な姿をしているから起きる」のではなく、食用種や無害そうな種に似た“そっくりさん問題”で起きることが見えてきます。
Amanita属では白色種が清潔感のある外観で紛れ、Galerina属では朽木の小型褐色菌が日常風景に溶け込み、Lepiota属では小型カラカサタケ型が食用イメージに引っぱられます。
公的機関が毎年同じ構図で注意喚起を続けるのは、同定の難しさが知識不足だけでなく、外見の似方そのものに根ざしているからです。
発見史と分析法の進歩──1941年から2025年の検出技術まで
1941年の単離と毒性学史
免疫学的迅速検査(LFIA)と尿検体の意義
免疫法の系譜は、RIA から ELISA を経て、ベッドサイドや現場で使えるLFIAへ伸びました。
LFIA(ラテラルフロー免疫測定法)は尿中の α-、β-、γ-アマニチンを抗体で捕まえ、約5〜10分で判定できます。
LFIA の臨床評価やカットオフ設定に関する詳細は、小規模臨床評価を含む専門報告を参照してください(後出の出典節や検出法の出典にリンクを付しています)。
⚠️ Warning
迅速検査の価値は、病名をその場で確定することより、アマトキシン中毒を疑うべき患者を短時間で浮かび上がらせるところにあります。5〜10分で得た情報が、後続の採血、肝機能評価、専門機関との連携の順番を前倒しにします。
LC-MS/MS・LC-HRMS/MSによる確定分析
迅速検査だけでは、臨床毒性学は完結しません。
LFIAは入口として鋭い一方、最終的な同定と記録には質量分析が必要になります。
そこで確定法の中心にあるのがLC-MS/MSです。
液体クロマトグラフィーで成分を分け、タンデム質量分析で分子量とフラグメントを読み取るこの方法は、アマトキシンを高感度かつ高特異度で確認できます。
臨床では「本当にアマトキシンか」「どのアナライトが出ているか」を詰める工程に相当し、法医学や症例報告でも軸になる技術です。

さらに近年は、LC-HRMS/MSが検出の幅を広げています。
2024年には、ヒト尿中アマトキシンを対象にしたLC-HRMS/MS迅速分析法が報告され、親和性カラムを組み合わせて、尿中の微量成分をより整理して拾う流れが示されました。
高分解能質量分析の強みは、既知のα-、β-、γ-アマニチンを確かめるだけでなく、近縁成分や夾雑物の中から目標分子を見分ける力にあります。
言い換えると、LFIAが「現場で疑いを立てる目」だとすれば、LC-HRMS/MSは「研究室で身元を照合する指紋鑑定」に近い役割です。
さらに近年は、LC-HRMS/MSが検出の幅を広げています。
2024年には、ヒト尿中アマトキシンを対象にしたLC-HRMS/MS迅速分析法が報告され、親和性カラムを組み合わせることで尿中の微量成分を高感度に検出する手法が示されました。
高分解能質量分析は既知のα-、β-、γ-アマニチンだけでなく近縁成分や夾雑物の中から目標分子を識別するのに有利です。
言い換えると、LFIAが現場で疑いを立てる目なら、LC-HRMS/MSは研究室で身元を照合する指紋鑑定に近い役割を果たします。
アマトキシン中毒の治療で、現時点でもっともはっきりしている前提はひとつです。
確立した特異的解毒剤はありません。
そのため治療の軸は、毒そのものを「打ち消す薬」に頼るのではなく、脱水、電解質異常、肝障害、腎障害といった全身の破綻を支える支持療法に置かれています。
ここは、作用機序の研究が進んだことと、臨床で使える決定打があることが同義ではない、という臨床毒性学らしい難しさが表れる部分です。
実際の医療現場では、初期の激しい消化器症状を越えたあとに肝障害が前景化するため、経過観察の焦点も「いま何が起きているか」から「次に何が崩れるか」へ移っていきます。
アマトキシンはRNAポリメラーゼIIを止めて細胞のタンパク質合成を断つ毒ですから、症状が落ち着いて見える時間帯があっても、肝細胞の内部では障害が進んでいることがあります。
治療が支持療法中心になるのは、まさにこの“見かけの回復”と“臓器障害の進行”がずれるからです。
この文脈で名前が挙がる薬剤としては、シリビニン(シリビン)やN-アセチルシステイン(NAC)があります。
ただし、これらは「確立した解毒剤」とは位置づけられていません。
臨床では補助的治療候補として扱われ、支持療法の上に積み上げる形で検討されます。
言い換えると、土台はあくまで全身管理であり、薬剤はその上で重症化を食い止める可能性を探るピースです。
薬剤候補のエビデンスの強弱
薬物治療の評価でよく参照されるのが、入院症例2,108件を集めた20年分の後ろ向き解析です。
この規模のレビューは歴史的にも重みがありますが、同時に「後ろ向き解析」である限界も抱えています。
治療開始のタイミング、重症度、併用療法、搬送までの経過がそろっていないため、薬効をきれいに切り分けることができません。
ここを踏まえると、アマトキシン中毒の薬物治療は有望な候補はあるが、強固な確定証拠は少ないという整理になります。
その中で相対的に期待を集めてきたのが、シリビニン(シリビン)とNACです。
シリビニンは、アマトキシンの肝細胞への取り込みを抑える可能性が議論されてきた薬剤で、後ろ向きデータでは転帰改善を示唆するシグナルがあります。
NACも、急性肝障害の場面で理にかなう補助療法として併用されることがあり、同じく有望視されています。
ただし、どちらも無作為化比較試験で確立した標準治療と呼べる段階には達していません。
研究が進んだ結果として見えてきたのは、「使う価値が検討される薬」はあるが、「これで決まり」と言える薬はまだない、という現実です。
一方で、長く使われてきたベンジルペニシリン(ペニシリンG)単独の位置づけは、以前より後退しています。
歴史的には頻用されましたが、上記の解析では明確な有効性を裏づける材料が乏しいと評価されました。
使用実績の多さと、効果の強さは一致しなかったわけです。
臨床で名前が知られている治療ほど効くとは限らない、という典型例でもあります。
💡 Tip
アマトキシン中毒の薬剤評価は、「理論上よさそう」と「患者の転帰を実際に改善した」が一致しにくい領域です。分子レベルの仮説、症例集積、後ろ向き解析が積み上がっても、なお決定打が生まれていない点に、この中毒の手ごわさが出ています。
肝移植と専門機関への相談
重症例で視野に入るのが肝移植です。
アマトキシン中毒は、肝細胞障害が一定の閾値を超えると、支持療法や補助的薬物治療だけでは立て直せない段階に入ります。
このとき肝移植は“最終手段”ではなく、救命のために現実的に検討される治療選択肢になります。
近年の大規模集団発生でも、死亡例だけでなく移植例が報告されており、アマトキシン中毒が今なお移植医療の対象になる毒性疾患であることは変わっていません。
ここで臨床上の分かれ目になるのは、診断の確度だけではありません。
肝障害の進行をどの時点で専門施設につなぐか、移植を扱える体制にどれだけ早く乗せるかが転帰に直結します。
アマトキシン中毒は、消化器症状の病気として始まりながら、途中から急性肝不全の病気へ姿を変えることがあります。
現場感覚でいえば、救急・集中治療・中毒対応・肝臓内科・移植外科が一本の線でつながっていないと追いつきません。
国内でこの連携の起点になるのが、日本中毒情報センターのような公的相談窓口です。
野生キノコ摂取後の中毒が疑われる場面では、日本中毒情報センターや地域の医療機関、公衆衛生の窓口が情報集約のハブになります。
加えて、国内の菌種情報や自然毒の整理には厚生労働省の毒キノコ資料や食品安全委員会のハザード概要シートが使われています。
アマトキシン中毒は、ひとつの病院だけで完結するというより、検査・中毒相談・肝不全対応・移植判断を束ねる医療として見ると全体像がつかみやすくなります。
現代の公衆衛生課題としてのアマトキシン
2025–2026年:カリフォルニアの集団発生
アマトキシンは、博物館の標本ラベルに閉じ込めて語れる毒ではありません。
そのことを最も端的に示したのが、2025年冬から2026年初頭にかけてのカリフォルニア州の集団発生です。
地域保健の報告では州内で複数の入院・死亡・肝移植例が確認されています(地域報告: Sacramento County Public Health, 2026-01-06 の発表参照)。
この数字が重いのは、単に患者数が多いからではありません。
アマトキシン中毒がいまもなお、救急医療、集中治療、毒物相談、移植医療を同時に動かす現役の公衆衛生問題だと示したからです。
しかも今回のような集団発生は、単独の“珍しい事故”では片づきません。
地域で同時多発すると、保健当局の注意喚起、医療機関の検査手配、毒物コントロールとの連携が一気に必要になります。
アマトキシン中毒は患者1人の診断で終わらず、地域全体の情報伝達速度まで問う毒だということです。
とくに注目したいのは、死亡例だけでなく肝移植例が現実に発生している点です。
前のセクションで触れた通り、アマトキシンは初期の消化器症状を越えたあとに急性肝不全へ姿を変えることがあります。
今回の州内集計は、その病態が教科書上の可能性ではなく、現代の医療圏で実際に移植適応へ進むレベルの傷害を引き起こしていることを、きわめて具体的に示しました。
なぜ毎年誤食が起きるのか
野生キノコの誤食が繰り返される背景には、偶然では片づかない科学的な理由があります。
まず大きいのは外見の類似です。
アマトキシンを含むタマゴテングタケドクツルタケや一部のGalerina属、Lepiota属は、食用種や無害に見える種と見分けがつきにくい場面があります。
傘の色、ひだ、つば、つぼ、発生環境といった形態的特徴は重要ですが、採取現場では成長段階や損傷で手がかりが崩れます。
図鑑の写真1枚と目の前の個体が一致して見える、そこに事故の入口があります。
次に、加熱で毒性が消えないことも誤食を重くします。
アマトキシンは調理で失活するタイプの不安定な毒ではありません。
山菜や野生キノコの文脈では「よく火を通せば大丈夫」と誤解されることがありますが、この毒には通用しません。
見た目で取り違えたうえに、調理で安全になるという期待まで重なると、危険な個体がそのまま食卓に乗ります。
さらに厄介なのが、症状の遅発です。
アマトキシン中毒では、摂取直後ではなく6〜24時間以上たってから消化器症状が前景化することがあります。
食べてすぐに体調が崩れないため、原因の結びつきが弱くなり、受診のタイミングが後ろへずれます。
しかもその遅れは、単なる時間差ではありません。
前述の通り、この毒はRNAポリメラーゼIIを止め、mRNA合成を断つことで細胞のタンパク質産生を失わせます。
症状が出るころには、肝細胞の中で障害のプログラムがすでに進行しているわけです。

現場感覚でいうと、この中毒は「食後すぐ苦しくなる毒」ではなく、「半日ほど平穏に見せてから本体を出してくる毒」です。
そこが毎年の誤食を止めにくくしている核心です。
見た目で油断し、調理で安心し、症状の遅さで受診が遅れる。
この三つが連鎖すると、公衆衛生上の警戒が毎年必要になる理由が見えてきます。
ℹ️ Note
参考文献: 大規模な後ろ向き解析として Enjalbert F. et al., 2002がしばしば参照されます。 アマトキシン中毒が厄介なのは、毒性の強さだけでなく、人が誤判断しやすい条件を毒そのものが備えている点です。似ている、火で消えない、しかも遅れて現れる。この組み合わせが事故の再発性を高めます。
最新レビューが示す研究前線
アマトキシン研究は、古典毒性学の整理で完結していません。
2025年のレビュー群をみると、焦点はむしろ現在進行形です。
ひとつは検出法の前進で、もうひとつは細胞障害の機序をどこまで臨床に接続できるかという問題です。
臨床では「アマトキシンらしい」と思ってから確定に至るまでの速度が転帰に響くため、分析法の改善はそのまま公衆衛生の武器になります。
実務面では、迅速スクリーニングとしてのLFIAと、確定分析としてのLC-HRMS/MSの組み合わせが見えてきました。
LFIAは尿中のα-アマニチンとγ-アマニチンを10 ng/mL、β-アマニチンを100 ng/mLで捉える設定が報告され、判定時間は約5〜10分です。
救急外来でこの速度は大きく、野生キノコ摂取の情報があいまいな段階でも初動の方向づけができます。
確定には質量分析系が欠かせません。
尿中では摂取後最大4日程度まで検出できる報告があり、2024年にはLC-HRMS/MSを用いた迅速分析法も示されました。
アマトキシン中毒は「症状から推定するしかない病気」から、「尿検体で追いかける病気」へ少しずつ変わっています。
機序研究でも前線は動いています。
肝障害の中心にRNAポリメラーゼII阻害があることは確立していますが、そこへ至る肝取り込み輸送体の役割、なかでもOATP1B1OATP1B3の関与は、治療戦略と直結する論点です。
毒が肝細胞へどう入るかを詰めれば、単なる支持療法にとどまらない介入の余地が見えてきます。
前のセクションで触れたシリビニンが注目され続けるのも、この取り込み過程をどこまで遮断できるかという発想とつながっています。
ここで公衆衛生が担う役割も明瞭です。
研究レビューが示しているのは、検査法と機序研究が進んでいるという事実だけではありません。
注意喚起、毒物相談、検体搬送、確認検査、重症例の専門施設紹介が一つの流れとして機能しないと、研究の成果が患者の転帰改善に届かないという現実です。
カリフォルニアの集団発生が浮かび上がらせたのは、アマトキシンが“知っているかどうか”の問題ではなく、“地域がどれだけ早くつながるか”の問題でもある、という現代的な姿でした。
アマトキシンと他毒の比較で整理する
アマトキシン vs ファロトキシン/ビロトキシン
Amanita phalloidesAmanita virosaAmanita vernaのような猛毒種では、アマトキシンだけでなくファロトキシン類やビロトキシン類が同時に見つかることがあります。
ただし、臨床像の中心を作っているのはアマトキシンです。
ここを混同すると、「同じキノコに入っている毒=同じ重みで効く」と誤解してしまいます。
アマトキシンの本体は、前述してきた通りRNAポリメラーゼII阻害です。
mRNA合成を止め、タンパク質を補充できなくなった細胞が時間差で崩れていきます。
標的はとくに肝臓で、そこに腎臓の障害が重なります。
症状の見え方は胃腸炎に始まっても、毒の本丸は消化管ではなく肝細胞の機能停止にあります。
一方、ファロトキシン類やビロトキシン類は同じキノコに共存していても、消化管からの吸収性が低いため、アマトキシンのように全身性の致死毒として臨床の主役にはなりません。
初期の消化器症状に多少関与している可能性は語られますが、重症化の軸を説明するには足りません。
救急の現場で「なぜ数時間から半日以上たって肝不全へ向かうのか」を説明するなら、焦点はファロトキシンではなくアマトキシンに置くべきです。
読者が自分の言葉で整理するなら、要点は次の4つに絞れます。
- アマトキシンは肝毒性の中心で、作用点はRNAポリメラーゼIIです。
- ファロトキシン/ビロトキシンは共存しても、主毒としての位置づけは低く、全身重症化の中心ではありません。
- 症状の時間軸では、アマトキシンは遅発性で、食後しばらく平穏に見える時間を挟みます。
- 標的臓器で見ると、アマトキシンは肝臓と腎臓、ファロトキシン/ビロトキシンは少なくとも臨床上その軸には立っていません。
この違いは、同じテングタケ属の毒でも「どの分子が転帰を決めているか」を見分ける作業だと言えます。
名前が並ぶと横並びの毒に見えますが、実際にはアマトキシンが病態の骨格を作り、他の環状ペプチド毒は脇役に回るという理解のほうが、臨床像ときれいに一致します。
アマトキシン vs イボテン酸・ムシモール
比較対象をAmanita muscaria、いわゆるベニテングタケ側へ移すと、違いはさらに明瞭になります。
こちらの代表毒はイボテン酸とムシモールで、中心になるのは神経作用です。
アマトキシン中毒を「遅れて肝臓を壊す毒」と表すなら、イボテン酸・ムシモール中毒は「比較的早く中枢神経症状を前面に出す毒」と言えます。
アマトキシンでは、食後すぐに激烈な神経症状が来るわけではありません。
むしろ初発は消化器症状で、その後に肝障害が前景化します。
これに対してイボテン酸・ムシモールでは、意識の変容、錯乱、興奮、眠気といった中枢神経系の異常が理解の中心になります。
同じ「毒キノコ」でも、障害される臓器と時間の流れがまるで違います。
ここも、説明できる形にしておくと混乱しません。
- アマトキシンは細胞毒性が中心で、主標的は肝臓、次いで腎臓です。
- イボテン酸・ムシモールは神経作用が中心で、主標的は中枢神経系です。
- 発症の見え方は、アマトキシンが遅発性、イボテン酸・ムシモールは比較的早い神経症状が前面に出ます。
- 危険の質も異なり、アマトキシンは偽回復期を挟みながら肝不全へ向かうのに対し、イボテン酸・ムシモールは神経症状の強さが問題の中心になります。
💡 Tip
毒キノコの説明で迷ったら、まず「肝臓を狙うのか、中枢神経を狙うのか」で分けると輪郭が見えます。アマトキシンは前者、イボテン酸・ムシモールは後者です。
現場感覚でいうと、アマトキシン中毒は静かに進む細胞毒で、イボテン酸・ムシモール中毒は早めに姿を見せる神経毒です。
症状の派手さだけを見ていると逆に見誤ります。
食後しばらく落ち着いて見えるのに後から肝障害が立ち上がるならアマトキシン系、早い段階から意識や行動の異常が前に出るならイボテン酸・ムシモール系、という整理なら、毒の種類と病態が一本につながります。
数値で押さえるアマトキシンのリスク
LD50
アマトキシンの毒性を数値でつかむとき、もっともよく参照される指標がLD50です。
これは実験動物で「半数致死量」を示す値で、アマトキシンではマウス腹腔内投与で 0.3〜20 mg/kgという幅が報告されています。
ここで幅が大きいのは、単に毒が「強いか弱いか」だけの話ではなく、動物種の違い、投与経路の違い、評価したアマトキシン分画の違いが重なるためです。
この数値はアマトキシン群が少量で致死域に入り得ることを示す一方、そのままヒトに機械的換算できる数字ではありません。
ヒトの致死量については、断片的な症例記述はあっても、条件がそろった一次データが十分にそろっているわけではありません。
摂取したキノコ種、乾燥か生か、摂取量の推定精度、嘔吐や下痢による実吸収量、治療介入の有無が混在するため、「ヒトでは何 mg で致死」と断定する書き方は避けるのが妥当です。
アマトキシンのリスク評価では、単純な致死量の暗記よりも、遅発性の経過と検査タイミングをどう読むかのほうが、実務では意味を持ちます。
含有量・カットオフ・検出期間
実際の診断や公衆衛生対応で役立つのは、「キノコ側にどれだけ入っているか」と「体液でどこまで拾えるか」を一続きで見ることです。
アマトキシン含有キノコでは、乾燥した傘組織 1 g あたりの総アマトキシン量が 2〜4 mg/g に入る例が多いとされています。
乾燥組織ベースで mg/g の桁に乗るという事実は、見た目には小さな摂取でも、化学的には無視できない負荷になり得ることを示します。
尿を使う迅速検査では、LFIA の実用的な境界値がはっきりしています。
α-アマニチンと γ-アマニチンは 10 ng/mL、β-アマニチンは 100 ng/mLがカットオフです。
報告例では、尿中最高濃度としてα-アマニチン 4820 ng/mL、β-アマニチン 7103 ng/mLに達したケースもあります。
数字を並べると、ピーク時にはカットオフを大きく上回る一方、時間の経過とともに濃度は下がるので、検査の価値は「どの検査を使うか」だけでなくいつ採るかで大きく変わります。
尿中での検出可能期間は摂取後、最大で約4日がひとつの目安です。
現場感覚で言えば、食後しばらくして受診した患者でも、尿が残っていればまだ情報を引き出せる時間帯があります。
逆に、採尿が遅れると、病態は進んでいるのにスクリーニングは陰性へ傾くことがある。
このズレがあるため、数値は単なる知識ではなく、「到着直後に尿を確保する」「初日の陰性を絶対視しない」という判断につながります。
💡 Tip
アマトキシンの数値は、毒性の強さを誇張するためではなく、検体採取の優先順位を決めるための道具として読むと実務に結びつきます。乾燥傘組織では mg/g、尿では ng/mL という桁の違いを意識すると、体内動態の見え方がそろいます。
迅速検査と確定分析の関係
LFIA の強みは、約5〜10分で判定できる点にあります。
救急外来で野生キノコ摂取が疑われたとき、この速さは治療と搬送判断の初動に直結します。
しかもカットオフが明示されているので、結果の意味づけが比較的しやすく、単なる「陽性・陰性」の二分法ではなく、検体採取時点が適切だったかまで含めて読めます。
ただし、LFIA はあくまでスクリーニングです。
臨床記録や法医学的裏づけまで含めて確証を取りに行く段階では、LC-MS/MS や LC-HRMS/MSが接続先になります。
こちらは分子種をより特異的に見分けられ、低濃度域まで追えるため、LFIA の陽性確認だけでなく、疑いが強いのに迅速検査で拾い切れないケースの整理にも向いています。
この2段構えは、検査を競わせる関係ではありません。
むしろ、LFIA が「いま判断する」ための道具で、LC-MS/MS や LC-HRMS/MS が「その判断を裏づける」ための道具です。
アマトキシン中毒では、遅発性という病態の性質上、検査を待ってから動くのでは遅れます。
だからこそ、最初の数分で走る検査と、その後に精度を詰める分析法が一つの流れとして組み合わさります。
数値を押さえる意味はそこにあり、いつ、何を、どれだけ測るかが診断と公衆衛生対応の速度を左右します。
まとめ──因果線でつなぐ理解と次のアクション
核となる因果線を一文で再提示
アマトキシン中毒の芯は、α-アマニチンがRNAポリメラーゼIIを阻害し、mRNA合成が止まり、タンパク質が枯渇した肝細胞が壊死へ向かうため、症状の山が遅れて立ち上がるという因果線にあります。
本記事の学びを広げるための次のアクション
理解を一段深めるなら、まずアマトキシンとα-アマニチン、そしてRNAポリメラーゼIIの関係を言葉として切り分けると、毒成分と作用点が頭の中で混線しません。
そのうえで、信頼できる公的資料として厚生労働省や日本中毒情報センターの公開資料を起点に読むことを推奨します。
薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
テトロドトキシンとフグの耐性|なぜ自分の毒で死なないのか
フグが自分の毒で死なない理由は、ひとつではありません。テトロドトキシン(TTX、C11H17N3O8、分子量319.27)を主に外部から取り込みながら、同時に自分の電位依存性Na+チャネルのTTX結合性をアミノ酸置換で下げ、神経と筋の麻痺を避けているからです。
毒ヘビの種類と毒の違い|神経毒と出血毒を比較
「コブラ科は神経毒、クサリヘビ科は出血毒」と覚えると入口はつかめますが、毒性学の論文を読み込むほど、その図式だけでは取りこぼすものが増えていきます。3FTx、PLA2、SVMPといった毒素群の一次論文を概観すると、ヘビ毒は単一の化合物ではなく、タンパク質・酵素・ポリペプチドが混ざり合った複合毒であり、
トリカブトとアコニチン|日本三大有毒植物の科学
春の山菜採りの季節になると、毎年のように名前があがるトリカブトは、特定の一種ではなくAconitum属の総称で、日本ではドクゼリドクウツギと並ぶ「三大有毒植物」として記憶されています。
毒の進化|防御と捕食、盗用と共進化の科学
自然史系の特別展「毒」を歩くと、読者の頭にまず浮かぶのは「どれがいちばん危険か」より、「生きものはなぜ、こんな仕組みを持ったのか」という問いだと思います。この記事は、その疑問に答えるために、まずpoisonを食べたり触れたりして効く毒、venomを牙や針で注入する毒、