ボツリヌス毒素からボトックスへ|最強の毒が美容医療を変えた
ボツリヌス毒素からボトックスへ|最強の毒が美容医療を変えた
ボツリヌス毒素は「最強の毒」とだけ語ると、本質を見失います。毒性学の実務でまず見るのは、何mgかではなく、どこに、どれだけ、どの経路で入るかという三つで、全身に回る中毒と、医師が局所へごく微量を打つ医療は、同じ物質でも意味がまるで変わります。 ボツリヌス毒素は毒と薬という二面性を持つ分子です。
ボツリヌス毒素は「最強の毒」とだけ語ると、本質を見失います。
毒性学の実務でまず見るのは、何mgかではなく、どこに、どれだけ、どの経路で入るかという三つで、全身に回る中毒と、医師が局所へごく微量を打つ医療は、同じ物質でも意味がまるで変わります。
ボツリヌス毒素は毒と薬という二面性を持つ分子です。
分子機構(SNAREの切断)、医療転用の歴史、日本における承認・製剤の違い、臨床・美容利用に伴う実務上の注意点を順に整理します。
あわせて、日本での承認適応、製剤ごとに互換できない「単位」の考え方、未承認・不適切製品が引き起こす現代のリスクまで視野に入れます。
ボツリヌス毒素は、毒が薬に変わる典型例である一方、名前の混同と用量・経路の誤解が、そのまま安全性の誤解につながる物質でもあります。
ボツリヌス毒素とは何か――毒としての正体
毒素そのもの:食品由来の中毒原因
ボツリヌス毒素は、嫌気性細菌である Clostridium botulinum が産生する神経毒性タンパク質です。
分子量は約150 kDaで、型はA〜G型に分けられます。
ヒトで主に問題になるのはA型・B型・E型で、F型はまれです。
神経筋接合部ではアセチルコリンの放出を止め、結果として弛緩性麻痺を起こします。
分子レベルではSNAREタンパク質を切断する仕組みで働き、A型とE型はSNAP-25、B型・D型・F型・G型はシナプトブレビン、C型はSNAP-25とシンタキシンを標的にします。
名称の由来も、毒としての歴史をよく表しています。
botulism の語源はラテン語の botulus、つまりソーセージです。
保存食由来の食中毒として古くから恐れられ、1895年にはエミール・ヴァン・エルメンゲムが原因菌を突き止めました。
まず「中毒の原因物質」として認識され、そこから長い時間をかけて医療利用へ転じていったわけです。
A型の推定ヒト中間致死量は報告により、静注・筋注でおおむね1.3〜2.1 ng/kg、吸入で10〜13 ng/kg、経口で約1 μg/kgとされています。
これらは推定値であり、曝露経路や評価条件に強く依存します。
中毒としてのボツリヌス症では、曝露後12〜36時間で発症することが多く、全身性の弛緩性麻痺が問題になります。
眼瞼下垂、複視、嚥下障害、構音障害から始まり、進行すると呼吸筋麻痺に至ることがあります。
ここで起きているのは「狙った筋肉の働きを少し弱める」ことではなく、「全身の神経伝達が障害される」ことです。
この違いを混同すると、毒そのものと薬としての製剤を同じ言葉で雑に扱ってしまいます。
この先の議論では、あえて三つを分けて扱います。
ひとつは自然界の毒素そのもの、ひとつは規格化された医療用製剤、もうひとつはボトックスという商標名です。
なお、ここで扱うのは性質と安全性の理解までで、製造や取得、悪用の具体には踏み込みません。
医療用製剤:規格化・精製・力価試験を経た薬
医療現場で使われるものは、「毒素そのもの」をそのまま注射しているわけではありません。
実際には、精製され、規格化され、力価試験を経た医療用製剤です。
ここに毒性学の転換点があります。
同じ分子でも、どの程度の純度で、どの単位系で、どの適応に、どの投与部位へ使うのかが固定されると、文脈は中毒学から薬理学へ移ります。
1970年代後半、米国で斜視治療への応用が進んだことが医療利用の大きな転機になりました。
過剰に収縮する筋肉を局所で抑えるという発想が成立し、眼瞼痙攣、片側顔面痙攣、痙性斜頸、痙縮、多汗症へと適応が広がっていきます。
美容領域での普及は、眼瞼痙攣の治療患者でしわ改善が観察され、1992年に眉間じわへの効果報告が広まったことがきっかけでした。
毒が薬へ変わったというより、全身中毒を起こす分子を、局所作用の道具として制御可能にしたと表現したほうが正確です。
製剤を理解するうえで外せないのが、「単位」は質量そのものではなく力価であるという点です。
ボトックス注の1単位は、マウス腹腔内投与LD50値に基づいて定義されています。
これは直感に反するのですが、臨床現場での「何単位」は、mgやμgのような単純な重さではありません。
私はこの点を初学者に説明するとき、同じ“1単位”と書かれていても秤で同じ重さを測っている感覚では読めない、と必ず言い換えます。
単位はあくまで製剤ごとの力価表現なので、製剤間でそのまま換算してはいけません。
Botox、Dysport、XeominはいずれもA型ボツリヌス毒素製剤ですが、単位互換はありません。
日本で知られる美容用途の承認製剤としてはボトックスビスタが代表的です。
一方で、医療用としての安全性は「ボツリヌス毒素だから安全」「承認薬だから一律に安全」という単純な話でもありません。
適応、用量、投与部位、製剤管理がそろって初めて薬として成立します。
2025年の英国では、美容注射に関連した医原性ボツリヌス症のアウトブレイクが25例報告され、未承認製品や不適切な管理が現代的なリスクとして可視化されました。
ここで問題になったのは、毒素の名前そのものより、どの製剤を、どの管理下で、どう使ったかです。
商標としての「ボトックス」:一般名ではない
日常会話では「ボトックスを打つ」が一般名のように使われますが、ボトックスは本来、特定製品の登録商標です。
一般名として整理すべき語は「ボツリヌス毒素」あるいは「ボツリヌストキシン」であり、ボトックスはその総称ではありません。
この区別は細かい言葉遣いの問題ではなく、製剤の取り違えを防ぐための最低限の整理です。
たとえば、BotoxとDysportとXeominは、いずれもA型ボツリヌス毒素製剤として語られますが、同一製品ではありません。
配合や製剤設計が異なり、単位も互換しません。
それなのに「全部ボトックス」とひとまとめにすると、一般名、商標名、製剤差が一気に崩れます。
医学記事でここを曖昧に書くと、読者は「どの成分の話をしているのか」「どの製品の安全性情報なのか」を追えなくなります。
この記事でボトックスという語を使うときは、商標としての意味に限ります。
毒としてのボツリヌス毒素、薬としての医療用製剤、商標としてのボトックス。
この三層を分けておくと、「最強の毒なのになぜ美容医療で使えるのか」という一見矛盾した問いも、言葉の混線ではなく、経路・用量・製剤設計の違いとして読めるようになります。
なぜ筋肉が動かなくなるのか――SNARE切断という分子機構
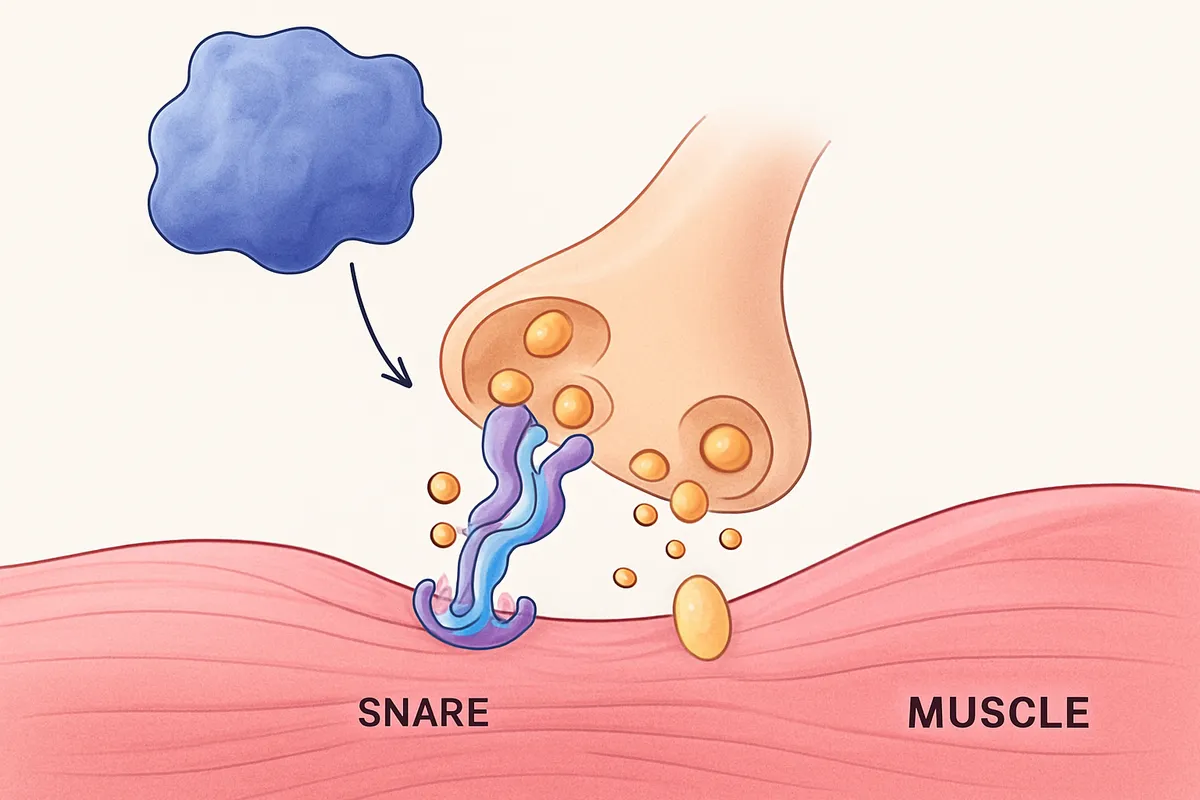
神経筋接合部とアセチルコリン放出
ボツリヌス毒素で筋肉が動かなくなる理由は、筋肉そのものを壊すからではありません。
止められるのは、神経筋接合部で運動神経終末から放出されるアセチルコリンです。
通常は神経終末にある小胞が細胞膜と融合し、その中身のアセチルコリンをシナプス間隙へ放出します。
放出されたアセチルコリンが筋線維側の受容体に結合すると、筋収縮の電気信号が始まります。
毒素の軽鎖はプロテアーゼ活性を持ち、神経終末内のSNAREタンパク質を切断してアセチルコリン放出を阻害します。
SNARE複合体は、小胞膜と神経終末膜をぴたりと引き寄せて融合させるための装置です。
ここが切断されると、小胞は膜融合できず、アセチルコリン放出阻害が起こります。
私はこの機序を図にするとき、小胞融合を担うSNARE、そこに入る切断、そしてアセチルコリンが出なくなる流れの順に並べます。
専門外の読者には、最初から分子名を並べるより、「神経の荷物が出口で止まる」と見えたほうが、筋肉がゆるむまでの因果が頭に入りやすいからです。
型ごとの標的SNARE
ボツリヌス毒素はA〜G型に分類されますが、どの型も同じ場所を無差別に壊すわけではありません。
共通しているのはSNARE複合体を標的にすること、違うのはどのSNAREタンパク質を切るかです。
A型とE型はSNAP-25を切断します。
B型、D型、F型、G型はシナプトブレビン(VAMP)を切断します。
C型は少し特殊で、SNAP-25とシンタキシンの両方を切断します。
つまり、型が違えば切断部位も違い、神経終末で小胞融合を止める入り口が異なります。
ただし、読者がまずつかむべき芯は一つです。
標的がSNAP-25であれシナプトブレビンであれシンタキシンであれ、帰結は同じで、SNARE複合体が組めなくなり、神経終末からアセチルコリンが放出できなくなるという点です。
分子標的の違いは、毒素型の分類や製剤設計を理解するうえで欠かせませんが、筋肉が弛緩する理由としては「神経伝達物質の放出を遮断する毒素」と捉えると全体像がぶれません。
効果の時間経過:発現の遅れと可逆性
ボツリヌス毒素の効果は、注射した瞬間に最大化するわけではありません。
神経終末に取り込まれ、軽鎖がSNAREタンパク質を切断し、既存の伝達が尽きていく過程をたどるため、数日遅れて作用が表面化します。
臨床で「打ってすぐ凍る」のではなく、少し時間をおいて表情筋や痙縮筋の力が落ちてくるのはこのためです。
その一方で、作用は永久ではありません。
化学的去神経化が起きても、神経は回復の方向へ動きます。
神経終末の再スプラウティングや、元の終末機能の再建が進むことで、伝達は徐々に戻ります。
ここに、毒としては長引く麻痺を生み、薬としては可逆的な局所抑制として扱える理由があります。
美容と医療の現場でよく経験される持続は、通常3〜4か月です。
長時間作用型のA型製剤では4〜6か月程度と整理されることもあります。
これは「毒が消えたから急にゼロに戻る」というより、切断された神経伝達機構を神経側が組み直していく時間を反映した長さです。
分子機構で見ると冷たい話に見えますが、臨床での時間経過はむしろ生体の回復力をそのまま映しています。
毒性学ではしばしば、壊す仕組みばかりが注目されます。
しかしボツリヌス毒素は、壊される側が再建する時間まで含めて薬効が決まるという点で、毒と薬の境目をもっとも鮮明に見せる分子の一つです。
ソーセージ中毒から眼科治療へ――医療転用の歴史
1895年:ヴァン・エルメンゲムの発見
ボツリヌス毒素の医療史は、美容医療から始まったわけでも、神経内科の発想から始まったわけでもありません。
出発点は食中毒研究でした。
1895年、ベルギーの細菌学者エミール・ヴァン・エルメンゲムが、ハムの摂取に関連した集団食中毒を調べる過程で、後にClostridium botulinumと呼ばれる菌を同定します。
語源の botulus がラテン語でソーセージを意味することからも、この毒素の原点が「ソーセージ中毒」にあったことが見えてきます。
この時代の関心は、もちろん治療応用ではなく、なぜ人が弛緩性麻痺を起こすのか、どのような食品が危険なのかという公衆衛生上の問題でした。
毒性学の歴史を振り返ると、こうした「事故の原因究明」が、のちに分子機構の理解へ進み、さらに医療技術へつながる流れが繰り返し現れます。
ボツリヌス毒素もその典型です。
猛毒として見つかったものが、神経伝達を局所的に止めるという性質ゆえに、のちには治療の道具へ変わっていきました。
私はこの歴史を年表に落とし込むとき、1895年を単なる発見年としてではなく、「毒として認識された瞬間」に置きます。
ここが起点にあるからこそ、その後の医療転用が逆説として際立つからです。
毒の正体を知ることが、毒を制御する第一歩だったとも言えます。
1970年代後半:斜視治療への応用開始
転換点が訪れるのは、20世紀後半です。
1970年代後半、米国でボツリヌス毒素を斜視治療に使う試みが始まりました。
眼球運動は外眼筋の微妙なバランスで成り立っていますが、斜視ではその力のつり合いが崩れます。
そこで、過活動の筋に局所投与して収縮を弱め、眼位を整えるという発想が生まれました。
ここで画期的だったのは、「全身性の麻痺を起こす毒」を「狙った筋だけ抑える薬」として再定義した点です。
前節で見たSNARE切断の機序は同じでも、投与経路と用量、そして局在の設計が変わると、文脈そのものが中毒学から治療学へ移ります。
斜視への応用は、ボツリヌス毒素を神経筋接合部の病態に対する治療手段として扱う最初期の実践であり、その後の眼瞼痙攣、顔面けいれん、痙縮などへの展開を開く入口になりました。
眼科領域から医療転用が進んだことには、理由があります。
外眼筋や眼輪筋は小さく、標的を定めた局所注射の効果を評価しやすいからです。
全身作用ではなく、局所の過活動を落ち着かせるという考え方が臨床で形になったのは、この領域だったわけです。
医療史として見ると、ボツリヌス毒素は「毒を弱めた」のではなく、「毒の届く範囲を精密に狭めた」ことで薬になった、と表現したほうが実態に近いと感じます。
1992年:眉間じわの効果報告
美容用途への扉を開いたのは、狙って見つけた効果というより、治療の現場で拾われた観察でした。
眼瞼痙攣の患者に対して眼輪筋周囲へ投与したところ、けいれんの軽減だけでなく、表情じわが目立たなくなる変化が目に留まったのです。
医療転用の歴史では、こうした「本来の評価項目ではない変化」が次の用途を生むことがあります。
ボツリヌス毒素の美容化は、その代表例です。
1992年には、眉間じわ、いわゆる glabellar lines への効果報告が広く知られるようになり、表情筋の局所抑制を美容医療へ応用する流れが加速しました。
眉間は皺眉筋や鼻根筋の反復収縮で縦じわが刻まれやすい部位です。
そこへボツリヌス毒素を用いると、筋収縮が抑えられ、動的なしわが浅く見える。
この原理は眼科や神経筋疾患での治療経験と地続きであり、美容だけが突然出現したわけではありません。
私がこの1992年の出来事を転換点として強調したいのは、医学史の教訓が凝縮されているからです。
新しい分野は、革新的な仮説からだけ生まれるとは限りません。
診療中の偶然の観察を、単なる副次的変化として流さず、再現性のある現象として捉え直したときに、治療の地図が書き換わります。
年表図を設計する場面でも、私はこの部分を一本の直線ではなく、小さな分岐が本流へ変わる節目として描きます。
医学的転用では、偶然の観察がパラダイムシフトの引き金になることがあるからです。
日本の承認年表へのブリッジ
こうして並べると、流れは明瞭です。
1895年に食中毒研究から菌が見つかり、1970年代後半に斜視治療で局所投与の価値が立ち上がり、眼瞼痙攣の診療現場でしわ改善が観察され、1992年の眉間じわ報告で美容用途が定着へ向かう。
毒の発見から治療薬、さらに美容医療へと文脈が移るまでには、ひとつの直線というより、観察と再解釈の積み重ねがありました。
日本でこの流れがどう承認制度に組み込まれていったかを見ると、科学史はさらに立体的になります。
研究室と診察室で起きた転換が、どの適応症から公的に認められ、どの製剤がどの順で位置づけられたのか。
その国内の年表を追うことで、ボツリヌス毒素が「危険な毒」でも「美容の代名詞」でもなく、厳密な適応の上に成り立つ医薬品として整備されてきた過程が読めます。
次では、その日本の承認史を時系列でたどります。
ボトックスは何を変えたのか――治療薬から美容医療へ

医療での適応例と作用の狙い
ボトックスが医療にもたらした変化は、猛毒の作用を「消した」ことではありません。
過活動を起こしている部位だけに、局所で、微量を、狙って使うという設計を臨床の中に持ち込んだことです。
神経筋接合部でアセチルコリン放出を抑えるという基本機序は同じでも、全身中毒では弛緩性麻痺として現れ、医療では過剰な収縮や分泌を静める方向へ使われます。
この文脈の転換こそが、ボトックスの本質です。
適応の広がりを見ると、その考え方がよくわかります。
眼瞼痙攣では、まばたきや開瞼に関わる筋の異常収縮を和らげます。
片側顔面痙攣では、顔の片側に反復して起こる不随意なけいれんを抑えます。
痙性斜頸では、首の筋の過活動によって頭位が引っ張られる状態を局所治療します。
さらに四肢の痙縮では、脳卒中や神経疾患の後に生じる筋緊張の高まりを落とし、姿勢や介助、リハビリテーションの妨げになる過剰収縮を減らします。
多汗症では筋肉ではなく汗腺を標的にし、交感神経終末からの信号伝達を抑えて発汗を減らします。
つまり対象は一枚岩ではなく、筋の過活動、顔面の不随意運動、異常姿勢、発汗過多と広いのですが、共通しているのは「出過ぎている神経信号を、その場で弱める」という一点です。
この局所性は、毒としてのボツリヌス毒素との対比でいっそう鮮明になります。
中毒では経口や創傷などから体内に入り、全身のコリン作動性終末に影響が及ぶことで、眼瞼下垂、複視、嚥下障害、呼吸筋麻痺へ連なります。
医療用A型製剤はそこを逆転させ、医師が標的筋や標的部位へ局所投与し、過活動を抑える治療として成立させました。
毒素そのもの、医療用A型製剤、美容用途のボトックス系製剤は、同じ分子機序を共有しながら、侵入経路、投与量、標的の限定という三条件で意味が変わります。
製剤の選択も単純ではありません。
臨床現場で中心になるのはA型製剤で、Botox/ボトックスDysportXeominのように複数の製品があります。
ただし単位は互換ではありません。
そもそも1単位はマウス腹腔内投与LD50に基づく力価表現で、製剤ごとにその「単位」の定義系が閉じているからです。
B型製剤が使われる場面もありますが、こちらはA型と置き換え可能な汎用品ではなく、適応や反応性の文脈で使い分ける別枠の選択肢と考えたほうが実態に合います。
私は毒性試験に関わっていた立場から、この「単位」という言葉が一見シンプルでいて、実は製剤差を抱え込んだ記号だと強く感じます。
mgで横並びに比べる感覚では読めません。
患者の実感としても、この薬は鎮痛薬のような即効型ではありません。
打ったその場で表情が止まるというより、数日たってから効き始め、数か月かけて元の状態へ戻っていくという時間軸を持っています。
臨床でよく共有される使用感としても、効き目は数日遅れて立ち上がり、持続はおおむね数か月です。
この「遅れて効いて、少しずつ戻る」という性質があるからこそ、過活動をゼロにする薬ではなく、病的な出力を一定期間だけ下げる調整薬として位置づけたほうが理解しやすいのが利点です。
美容:動的なしわへの適用範囲
美容でのボトックスは、しわ全般を消す魔法の注射ではありません。
中心にあるのは動的なしわ、つまり表情筋が収縮したときに皮膚に折れ目として現れるタイプです。
眉を寄せたときの眉間、額を上げたときの額、笑ったときの目尻が典型で、いずれも表情筋の反復収縮が皮膚表面に刻む線です。
ここに局所投与すると、筋の収縮が一時的に弱まり、折れ目が入り続ける力が減るため、見た目のしわが浅くなります。
この仕組みは、医療で眼瞼痙攣や顔面けいれんを抑える考え方の延長線上にあります。
違うのは治療対象の評価軸で、神経症状の軽減ではなく、表情によって生まれる線の目立ち方を整える点です。
私はこの美容応用を「毒が軽くなった」とは表現しません。
むしろ、表情筋という小さな標的に対して、必要な範囲だけ神経伝達を弱める精密化が進んだ結果だと考えています。
筋肉の出力を局所で絞るから、皮膚の折れ目にも変化が出る。
論理は一貫しています。
一方で、静的なしわ、つまり無表情でも深く刻まれて残る線は、ボトックス単独で説明しきれない領域です。
表情運動の反復で始まったしわでも、長年の皮膚変化が重なると「動かないときにも残る線」へ移ります。
ボトックスが最も得意なのは、その手前にある動的な成分を弱めることです。
この適用範囲を外すと、期待と現実がずれます。
美容医療でボトックスが広く定着したのは、対象を表情筋の過活動に絞ると、作用機序と見た目の変化がきれいにつながるからです。
持続期間の感覚も、美容用途では理解の軸になります。
一般的な美容効果は3〜4か月前後で、長時間作用型製剤では4〜6か月程度まで伸びるものがあります。
ただ、どの製剤でも永続的に筋を止めるわけではありません。
数日後から変化が出て、数か月で戻る。
このリズムを前提にすると、美容のボトックスは「顔を固定する処置」ではなく、「動きの強さを一定期間だけ弱める介入」と捉えるのが実態に近いです。
患者さんの感想を聞いていても、最初の数日はまだ動くのに、ある時点から眉間に力が入りにくくなり、その後3〜4か月ほどで少しずつ元へ戻っていく、という表現がいちばんしっくりきます。
美容の文脈ではボトックスという名称が一般名のように使われがちですが、日本では商標名としての意味合いが強く、実際にはA型ボツリヌス毒素製剤の総称として雑に消費されている面があります。
Botox/ボトックスDysportXeominはすべてA型製剤でも、単位互換はありませんし、立ち上がりや持続の説明のされ方にも違いがあります。
Xeominは複合タンパクを含まない“naked toxin”として語られることがあり、免疫原性の話題で比較されることがありますが、読者がまず押さえるべきなのはブランド名の知名度ではなく、同じ「ボトックス」と一括りにできないという点です。
用量が毒を決めるの現代的実証
パラケルススの「用量が毒を決める」は、ボトックスほど現代医学で可視化された例が少ない原理です。
ボツリヌス毒素はA型でヒトの推定経口致死量が1 μg/kg、静注・筋注では1.3〜2.1 ng/kgという桁の小ささで語られる猛毒です。
毒として体内に広く入れば、呼吸不全を含む重い全身中毒を引き起こします。
ところが医療では、その同じ分子を局所・微量・標的限定で使い、神経伝達を狙った場所だけ抑える薬に変えています。
理論の上だけでなく、制度、製剤設計、投与手技の三つを揃えて「用量が毒を決める」を実装したのが医療用ボツリヌストキシンだと言えます。
この差を整理すると、三層構造が見えてきます。
毒素としてのボツリヌス毒素は、経口や創傷などから侵入して全身性の弛緩性麻痺を起こしうる存在です。
医療用A型製剤は、医師が局所投与して過活動筋や発汗を抑える治療手段です。
美容用途では、その局所治療の考え方を動的なしわへ適用し、表情筋の出力を下げて皮膚表面の線を目立ちにくくします。
分子は同系統でも、文脈はまったく同じではありません。
毒性学でいう「曝露の条件」が、そのまま意味の違いになります。
💡 Tip
ボトックスを理解するときは、「何の分子か」だけでは足りません。どこに、どれだけ、どの経路で入るかまで含めて読むと、毒と薬と美容施術が一本の線でつながります。
この原理は安全性の議論にも直結します。
医療用製剤には1回の成人同時投与量として合計400単位という上限が設定され、局所投与の枠内で管理されます。
しかも単位は前述の通り製剤ごとに独立しており、他社製剤と単純換算できません。
こうしたルールは面倒な事務処理ではなく、猛毒を薬に変えるための境界線そのものです。
医療で成立しているのは、毒性が消えたからではなく、毒性が現れる条件を細かく制御しているからです。
反復投与の話題も、この「現代的実証」の一部です。
美容で年2回、3〜6か月ごとに顔面へ施術するような使い方では、年間の総使用量は数十単位規模に収まることが多く、臨床的な中和抗体の発生率は系統解析で2.1%以下にとどまります。
とはいえ、ここでも見ているのは単なる有無ではなく、累積投与量、投与間隔、適応の違いです。
毒性学はいつも「ゼロか百か」ではなく、条件の積み重ねで結果を見ます。
ボトックスは、その考え方を教科書ではなく実臨床で示している薬です。
日本での承認と注意点――ボトックスは一般名ではない

商標と一般名:ボトックス/ボツリヌス毒素/製剤名の区別
ここは用語を一度きれいに分けておかないと、医療の話と美容施術の話がすぐ混線します。
ボトックスはアラガン由来の登録商標であって、ボツリヌス毒素そのものの一般名ではありません。
一般名としての軸にあるのはボツリヌス毒素、より実務的にはA型ボツリヌス毒素製剤です。
そのうえで製品名としてボトックスボトックスビスタ®DysportXeominのような銘柄が並びます。
日本で美容目的の承認製剤として位置づけられているのはボトックスビスタ®です。
この点が、日常会話で「ボトックスを打つ」と言うときの曖昧さの源でもあります。
読者の多くはボトックス=一般名と受け取りがちですが、実際には「商標」「一般名」「製剤名」の三つは別レイヤーです。
私はこの誤解をほどくとき、文章だけで押し切るより、3列対比の図表にしたほうが認識のずれが一気に減ると感じています。
商標にボトックス、一般名にボツリヌス毒素、製剤名にボトックスビスタ®や各社製剤を並べるだけで、読者がどこで言葉を取り違えていたかが見えてきます。
国内の承認拡大の流れも、この整理に沿って読むと理解しやすくなります。
日本では1996年に眼瞼痙攣、2000年に片側顔面痙攣、2001年に痙性斜頸へと適応が広がり、2009年に美容適応としてしわ治療が加わりました。
つまり、日本で先に育ったのは美容より治療の文脈です。
美容医療で名前が先行した結果としてボトックスが総称のように広まったものの、制度上も製品上も、あくまで固有の商標と承認製剤の話として読む必要があります。
単位と力価:LD50由来の定義と換算不可
ボトックス注用100単位の「1単位」は、マウス腹腔内投与LD50に基づく力価として定義されています。
ここでいう単位は、日常的な質量の単位ではなく、その製剤がどれだけの生物活性を持つかを表す尺度です。
数字だけ見ると共通規格のように見えますが、実態はそうではありません。
この定義から直結するのが、製剤間で単位を相互換算できないという事実です。
Botox/ボトックスDysportXeominはいずれもA型ボツリヌス毒素製剤ですが、1単位同士を同じ量として扱うことはできません。
単位の土台にある力価試験や製剤設計が同一ではないからです。
銘柄をまたいで「前回は何単位だったから今回は別製剤でも同じ数字でよい」と置き換える発想は、医療上のリスクをそのまま持ち込みます。
添付文書には、成人の同時投与総量として合計400単位という記載があります。
この数字も「どの製剤でも400単位まで同じ意味で使える」という話ではなく、承認された当該製剤の力価体系の中で読むべき上限です。
毒性学の視点で見ると、ここで管理されているのは単なる量ではなく、局所投与される生物活性の範囲です。
前のセクションで触れた「用量が毒を決める」は、この単位の読み方にもそのまま当てはまります。
💡 Tip
20単位という表記だけでは情報が足りません。必要なのは「どの製剤の20単位か」で、銘柄名まで入って初めて医療情報として意味が定まります。
国内承認・自由診療・救済制度の整理
日本の美容医療では、承認製剤と自由診療の範囲がきれいに一致しているわけではありません。
美容目的の承認製剤としてはボトックスビスタ®が基準になりますが、自由診療の現場では未承認製剤が使われることもあります。
ここで差が出るのは名前の知名度ではなく、国内試験、流通管理、そして健康被害が起きた際の制度上の扱いです。
承認製剤は、日本の審査を通過した品質・有効性・安全性の枠組みの中で流通し、添付文書、承認情報、審査資料を国内の制度に沿ってたどれます。
未承認製剤では、この前提が崩れます。
国内試験が実施されていないことがあり、流通経路も個人輸入などを含み、同じA型製剤でも制度上の位置づけは別物です。
さらに、医薬品副作用被害救済制度は適正使用された医薬品による健康被害を対象とする仕組みですが、未承認製剤や流通管理が不明な製品では、対象の考え方に差が生じます。
ここを「成分が同じなら同じ」と扱うと、制度面の見取り図を誤ります。
安全性の話題では、一般論だけを広げるより一次情報への導線を明確にしたほうが読者の役に立ちます。
私はこの種の記事を書くとき、具体的な施術可否の断定には踏み込まず、PMDAで添付文書と承認情報を確認し、厚生労働省の美容医療注意喚起で制度上の位置づけを読む、という流れが自然につながる構成を意識しています。
記事本文では原理と制度の骨格を示し、個別判断の根拠は公的情報に戻せるようにしておくと、情報の温度が上がりすぎません。
近年の事例として見逃せないのが、2025年の英国で報告された美容注射由来の医原性ボツリヌス症アウトブレイクです。
報告症例は25例にのぼり、未承認または不適切な製品管理と施術の危うさが、抽象論ではなく現実の公衆衛生問題として現れました。
ボツリヌス毒素は、正しく制度化された医療では薬になりますが、その枠を外れると「同じ名前で語れない別のリスク」が立ち上がります。
美容医療はあくまで医療行為であり、商品比較の感覚だけでは読み切れない領域です。
最強の毒が教えること――毒と薬は連続体である
パラケルススの「用量が毒を決める」というテーゼは、古い警句として読むと半分しか見えません。
現代薬理の視点で読み直すと、そこで問われているのは量だけではなく、どの標的に、どの経路で、どの範囲に作用を閉じ込めるかという設計そのものです。
ボツリヌス毒素は、そのことを最も鮮明に見せた分子でした。
全身に広がれば呼吸不全を含む重篤な中毒を起こしうる神経毒が、局所に、制御された力価で、狙った筋や神経終末に届くよう組み立て直されると、痙縮や眼瞼痙攣、多汗、表情ジワの治療に使える。
毒性と治療効果は向かい合う別物ではなく、同じ作用機序が用量・標的・投与経路という三つの変数で分岐した結果です。
私自身、毒性学の文脈でパラケルススを学んだときは、「量を間違えると危ない」という素朴な教訓として受け取っていました。
ただ、ボツリヌス毒素の歴史と製剤設計を追うほど、その言葉はもっと工学的に読めるようになりました。
毒を薬へ変える鍵は、毒性を消し去ることではありません。
作用点を限定し、全身暴露を避け、再現可能な単位系で管理することです。
ボツリヌス毒素が示したのは、「猛毒を無毒化した」のではなく、「猛毒の作用を医療目的に合わせて局所化・定量化した」という設計原理だった、と私は理解しています。
この意味で、ボツリヌス毒素は毒性学、神経科学、美容医療を一本の線でつないだ象徴例です。
中毒学の対象だった分子が、神経筋接合部でアセチルコリン放出を止める精密なツールとして神経科学を前進させ、その延長線上で医療用A型製剤やボトックスビスタ®のような美容適応製剤へと展開したからです。
ここで起きたのは、単なる用途追加ではありません。
「毒だから排除する」「薬だから安全だとみなす」という二分法を外し、同じ分子を文脈に応じて読み替える知の再編でした。
毒から薬へという言い回しは比喩に見えて、実際には作用機序、製剤学、制度設計が重なって成立した現実の変化です。
その連続体の発想は、楽観論とは逆です。
連続しているからこそ、境目を曖昧に扱えません。
承認製剤かどうか、局所投与として管理されているか、単位体系を正しく読んでいるか、その枠を一つ外すだけで、薬としての振る舞いは毒の側へ戻ります。
前述の制度や製剤の違いが細かく見えても、あれは枝葉ではなく、この連続体のどこに立っているかを示す境界線です。
読者の立場で必要なのも、極端な恐怖や安易な慣れではなく、情報の当たり先を間違えないことだと思います。
安全性や承認の確認はPMDAや厚生労働省の公的資料に置き、施術の可否や適応の判断は医師の診療に委ねる。
この距離感が、ボツリヌス毒素のように「最強の毒」と「日常的な医療」が同居する対象では、そのまま安全の土台になります。
毒と薬は紙一重、という表現は印象的ですが、実際には紙一枚ではありません。
用量、標的、投与経路、製剤、制度という複数の層が重なって、はじめて薬として成立しています。
FAQ:よくある疑問

Q1. ボトックスは菌そのもの?
いいえ。
注射されるのは生きた菌ではなく、精製されて規格化されたA型ボツリヌス神経毒素を含む医療用製剤です。
ここを混同すると、「食中毒の原因菌を入れるのか」という誤解が生まれます。
実際の医療用製剤は、感染を起こすためのものではなく、神経終末でアセチルコリン放出を一時的に抑える目的で局所投与されます。
毒性学では「何という物質か」だけでなく、「どの形で、どの経路で、どう規格化されているか」を分けて考えます。
ボツリヌス症の文脈にある毒素と、医療現場で使うボトックスボトックスビスタディスポートゼオミンのような製剤は、同じA型ボツリヌス毒素を含んでいても、扱うレイヤーが違います。
私自身、このFAQのような読者の疑問が多い箇所では、誤解を残さないために回答の末尾に公的・専門的な情報へ戻れる導線を置くようにしています。
作用機序の整理には脳科学辞典|ボツリヌス毒素、中毒としての全体像にはWHO Botulism Fact Sheetが役立ちます。
Q2. 効果が切れると悪化する?
多くの場合、前より悪くなるというより、元の状態へ少しずつ戻ると考えるのが実態に近いです。
ボトックス系製剤の作用は可逆的で、筋肉や神経が永久に失われるわけではありません。
そのため、効いている間は表情ジワや筋収縮が抑えられ、作用が薄れるにつれて元の筋活動が戻ってきます。
「効いていた期間の落差」で悪化したように感じることはあります。
たとえば、眉間の緊張が抑えられていた数か月のあとに元の収縮が再開すると、施術前と同じ状態でも印象として強く戻ったように見えます。
ただし、長期的に見てボトックスをやめると以前より悪化する、と断定できる高品質エビデンスは限られます。
美容医療の印象論と生理学的な変化は分けて読む必要があります。
施術効果の持続と戻り方の確認にはアラガン・エステティックス|ボツリヌストキシン治療ガイドが整理されています。
Q3. 反復が必要なのはなぜ?
作用が永続しないからです。
ボツリヌス毒素は神経終末でSNAREタンパク質を切断し、アセチルコリン放出を止めますが、この状態は固定されません。
時間がたつとSNAREは再生し、神経終末では再スプラウティングも起こるため、神経筋伝達は回復に向かいます。
薬として見れば、これは「切れたら終わり」ではなく「回復するように設計された局所作用」です。
美容領域では持続は通常3〜4か月前後で、長時間作用型では4〜6か月程度まで見込まれる製剤もあります。
だから定期的に打つ、というより、効き目の窓が数か月単位だから反復投与という形になるわけです。
私はこの点を説明するとき、「依存性があるから続ける」のではなく、「薬理作用が可逆的だから更新する」と言い換えます。
そのほうが、漫然と回数だけを追う見方から離れられます。
治療としての基本的な作用機序は脳科学辞典|ボツリヌス毒素、美容用途の持続イメージはアラガン・エステティックス|ボツリヌストキシン治療ガイドで確認できます。
Q4. 承認品と未承認品の違いは?
違いは成分名の表面だけではなく、国内試験、流通管理、制度上の位置づけにあります。
承認製剤は日本の審査を通ったうえで、添付文書、承認情報、審査資料を追える状態で流通しています。
未承認製剤では、この国内の検証と流通管理の枠組みが前提になりません。
見た目や説明が似ていても、制度上は同列ではありません。
この差は、健康被害が起きたときにも響きます。
承認製剤は国内制度の中で扱われますが、未承認製剤や流通経路が不明な製品では、救済制度の対象性を含めて扱いが変わります。
さらに、不適切管理や偽造製品の問題は抽象的な不安ではなく、現実の有害事象として現れています。
2025年の英国では、美容注射に関連した医原性ボツリヌス症のアウトブレイクが報告され、症例は25例に達しました。
承認の有無は「お墨付き」の話ではなく、品質管理と追跡可能性の差です。
国内承認情報はボトックス注 電子添文、制度面はPMDAの救済制度案内、施術前の確認事項は厚生労働省の美容医療注意喚起サイトで押さえられます。
Q5. 中和抗体はどれくらい起こる?
A型ボツリヌス毒素製剤に対する中和抗体の発生率は2.1%以下と整理された系統的解析があります。
数字だけ見ると高頻度ではありませんが、ゼロではありません。
しかも、抗体が見つかったことと、臨床的に「効かない」と感じることは同義ではありません。
検査上の抗体陽性と、実際の非応答にはずれがあります。
リスク因子としては、累積投与量が多いこと、投与頻度が高いこと、間隔が短いことが挙げられます。
美容領域の通常用量では大きな問題として遭遇する場面は多くありませんが、長期反復の設計を考えるうえでは無視できません。
たとえば年に2回の施術を数年続けるだけでも累積単位は積み上がるので、「毎回効くか」だけでなく「長く使う設計になっているか」という視点が入ります。
私がFAQに公的・論文ベースの導線を必ず添えるのも、こうした低頻度だけれど判断を誤りやすい論点ほど、一次情報に戻れるほうが読後の混乱が少ないからです。
整理にはImmunogenicity of Botulinum Toxin Type A reviewが有用です。
Q6. 単位は換算できる?400単位とは?
メーカー間で単位は換算できません。
ボトックスの1単位、ディスポートの1単位、ゼオミンの1単位は同じ意味ではありません。
理由は、単位が単純な質量ではなく、各製剤の力価試験に基づく定義だからです。
ボトックス注では1単位がマウス腹腔内投与LD50値に基づくとされており、この時点で「mgのように横並びで比べる数字」ではないことがわかります。
正式な定義と上限量はボトックス注 電子添文(PMDA:
薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
毒から薬へ|毒性のある物質が医薬品になる条件
毒はなぜ薬になりうるのか。この問いに答える鍵は、毒=悪、薬=善という単純な線引きではなく、用量・投与経路・標的選択性・規制という4つの条件にあります。非臨床安全性研究で用量反応曲線を組むとき、初期毒性兆候をどこで拾い、どの投与量をNOAELやLOAELとして切るかを詰める作業そのものが、
トリカブトと漢方の附子|毒が薬になるまで
山菜と見分けを誤れば命に関わるトリカブトは、塊根を加工し、規格の中で管理すると、生薬附子(ブシ)として医療の現場に入ってきます。この記事は、毒草としての植物が、どうやって処方に組み込まれる医薬の素材へ変わるのかを知りたい人に向けて、その道筋を一本の線でたどるものです。
ジギタリスの物語|毒から薬、そして再評価
花壇では優美に見えるジギタリスは、ひとたび体内に入れば心臓に触れる毒でもあります。その危うい植物が、18世紀の観察医学から現代の薬理学へどう橋を架け、心不全治療の景色をどう変えたのかを追うのが本稿です。
抗毒素と血清療法|北里柴三郎が開いた道
北里柴三郎を語るとき、主役は人物名だけでは足りません。焦点に置くべきなのは毒素そのものと、それを狙い撃ちで中和する抗毒素、そしてその抗体を投与して即効性を引き出す血清療法という発想です。