トリカブトと漢方の附子|毒が薬になるまで
トリカブトと漢方の附子|毒が薬になるまで
山菜と見分けを誤れば命に関わるトリカブトは、塊根を加工し、規格の中で管理すると、生薬附子(ブシ)として医療の現場に入ってきます。この記事は、毒草としての植物が、どうやって処方に組み込まれる医薬の素材へ変わるのかを知りたい人に向けて、その道筋を一本の線でたどるものです。
山菜と見分けを誤れば命に関わるトリカブトは、塊根を加工し、規格の中で管理すると、生薬附子(ブシ)として医療の現場に入ってきます。
この記事は、毒草としての植物が、どうやって処方に組み込まれる医薬の素材へ変わるのかを知りたい人に向けて、その道筋を一本の線でたどるものです。

製薬企業の安全性研究でNa⁺チャネル作動薬の電気生理データを見ていたとき、細胞膜の電位が戻れなくなる波形は、押した鍵盤が戻らず鳴りっぱなしになるピアノのように見えました。
トリカブトのアコニチン系アルカロイドが起こす持続脱分極と不整脈も、その延長線上で理解できますし、附子の安全性は単なる「少量だから」ではなく、加熱や加圧加熱による修治で毒性を落とし、日本薬局方や加工ブシ末の規格管理でばらつきを抑えているところに支えられています。
本稿では、トリカブト属という植物の正体から、アコニチン系の毒性機序、文献で特定条件下に報告される長時間加熱で毒性が約200分の1に低下するという目安、そして八味地黄丸真武湯などの処方に届くまでを、毒と薬の境目がどこで引き直されるのかという視点で整理していきます。
なお「200分の1」は特定の実験条件に基づく目安であり、温度・時間・圧力・原料の由来などで大きく変わる点は本文中で繰り返し注意します。
トリカブトは1つの植物名ではない
トリカブト属(Aconitum)の範囲
まず用語を三層で切り分けると、この記事のテーマがぶれません。
- 植物:トリカブト。正確にはキンポウゲ科トリカブト属(Aconitum)に属する植物群の総称です。
- 生薬:附子(ブシ)。トリカブト属植物の塊根を原料にし、修治を経て医療用の生薬として扱うものです。
- 漢方処方:附子を含む処方。附子単独ではなく、複数の生薬を組み合わせて設計された医薬の形です。八味地黄丸牛車腎気丸真武湯麻黄附子細辛湯などがここに入ります。
この区別を置かないまま「トリカブトは薬になる」と言ってしまうと、猛毒の植物そのものと、規格化された生薬、さらに処方としての漢方薬が一つに混ざってしまいます。
実際には、野外に生えているトリカブトと、医療で使われる附子のあいだには、分類・加工・規格という何段階もの壁があります。

トリカブトは「1つの花の名前」のように聞こえますが、分類学では属名に近い呼び方です。
世界には約300種前後が知られ、日本でも約30〜35種の自生種があります。
資料によって数え方が少し動くのは、近縁種の扱いや分類の整理が絡むためで、ここでは幅を持たせて捉えるのが妥当です。
どの種であっても共通して押さえるべきなのは、全草有毒だという点です。
葉、茎、花、根のいずれにもアコニチン系アルカロイドが含まれますが、なかでも毒性が強いのが塊根です。
附子の原料になるのもこの部分で、薬になる入口と、もっとも危険な部位が同じ場所にあるところに、トリカブトのやっかいさがあります。
フィールドガイドを何冊か見比べると、日本で「トリカブト」と呼ばれるものの花色、花序、葉の切れ込み、草丈には細かな差があります。
ただ、その差は観察の慣れを要するものが多く、一般の人が現地で即断できる種類ではありません。
山野で複数のトリカブト属植物が並ぶと、写真では区別できそうでも、実物では湿り気、光の向き、成長段階で印象が変わります。
現場での同定が難物だとされる理由は、まさにそこにあります。

日本の自生種は約30〜35種
日本に自生するトリカブト属植物は約30〜35種とされます。
単に「日本にもある」ではなく、本州から北海道、山地から亜高山帯まで、地域ごとに異なる種や変種が見られる規模です。
そのため、日常語の「トリカブト」は便利な総称である一方、植物学の精度では少し粗い言い方でもあります。
この幅広さは、毒性の話を読むときにも意味があります。
トリカブト中毒の記事で出てくる「トリカブト」は、必ずしも同じ1種を指しているわけではありません。
共通するのはアコニチン、メサコニチン、ヒパコニチンといったアコニチン系アルカロイドを持つこと、そしてそれらが電位依存性Na⁺チャネルに作用して持続的な活性化と脱分極を起こすことです。
私が安全性研究で電気生理の波形を読んでいた感覚で言えば、チャネルが「開いては閉じる」という本来の拍を失い、戻るべきところへ戻れなくなるイメージに近いです。
属としての多様さはあっても、毒性のコアにはこの共通機構があります。
種数が多いことは、見た目の多様さにも直結します。
花の兜のような形は共通していても、葉の裂け方や花のつき方は一様ではありません。
山菜の誤採取が起きる背景には、「トリカブトはこれ」という単純な一枚絵で覚えられない事情があります。
野外では若い芽、食べ頃の山菜、開花前の草姿が似て見える組み合わせがあり、しかもトリカブト側も日本列島の中で複数の姿を取ります。
「危険植物を1枚の図鑑写真で覚え切るのは無理がある」と感じる場面があるのは、そのためです。

ここで押さえたいのは、種類が多いから危険が分散するのではなく、種類が多いのに総称で呼ばれがちだから認識が粗くなるという点です。
記事の後半で附子や漢方処方を扱うときも、出発点はあくまでこの多様なトリカブト属植物です。
植物・生薬・処方の用語整理
同じ「ブシ系」の話でも、段階ごとに意味が変わります。混同しやすい4つを並べると、違いがはっきり見えます。
- 生のトリカブト
野外に生育するトリカブト属植物そのものです。全草有毒で、とくに塊根の毒性が強く、誤食中毒の対象になります。安全性を担保する加工も規格も入っていません。
- 修治前の附子原料
生薬の原料として見た塊根です。
植物体から切り出した部位という意味では生のトリカブトと連続していますが、この段階でも毒性はなお強く、医療で使える状態には達していません。
- 加工附子(ブシ・加工ブシ末)
修治によってアコニチン系成分が加水分解され、低毒性側の成分へ寄った生薬です。
文献では特定条件下において長時間加熱で毒性が約200分の1になるという目安が示されることがありますが、この数値は処理条件や原料によって大きく変わるため、あくまで一つの目安として理解してください。
とはいえ、作用の強い生薬である事実は変わりません。

- 附子を含む漢方処方
加工附子を、甘草、桂皮、朮、茯苓など他の生薬と組み合わせ、処方設計の中で用いる段階です。
ここでは附子単独の性格だけでなく、全体の配合、製剤化、品質管理が効いてきます。
真武湯と八味地黄丸で附子の位置づけが同じにならないのは、このためです。
この4つは、機能・安全性・使われ方がそれぞれ違います。
生のトリカブトは有毒植物であり、修治前の附子原料もまだ危険物の延長線上にあります。
加工附子になると医療資源としての輪郭が立ち、漢方処方に入ると今度は「附子そのもの」ではなく「処方全体の働き」の一部になります。
毒と薬の境目は一点ではなく、植物学、薬学、製剤学の各段階で引き直されているわけです。
日本薬局方のような規格基準が意味を持つのもこの層構造のためです。
植物をそのまま使う話ではなく、どの部位を原料とし、どのように品質を揃え、どの範囲の医薬品として扱うかが定義されているから、附子は「猛毒の根」から医療の言葉に翻訳されます。
トリカブトを理解するうえで、この翻訳の途中工程を飛ばさないことが欠かせません。
猛毒の正体はアコニチン系アルカロイド
主要成分と化学的特徴

トリカブトの猛毒を担う中心は、アコニチン系アルカロイドです。
代表的な成分として挙がるのが、アコニチン、メサコニチン、ヒパコニチンで、いずれも同じ系統の毒性を示します。
名前は別でも、神経や心筋の興奮を制御する膜タンパク質に食い込むという点で共通しており、トリカブトの危険性はこの化学群でほぼ説明できます。
ここでいう「アルカロイド」は、植物がつくる含窒素化合物の一群です。
ニコチンやモルヒネと同じく、微量でも生体機能を大きく動かすタイプの分子が多く、アコニチン系もその典型です。
しかもトリカブトでは、これらが葉や茎だけでなく塊根にも含まれます。
前述の通り、附子が薬学の対象になるのも塊根ですが、同じ場所に強い毒性の本体も集まっているわけです。
化学的には、アコニチン、メサコニチン、ヒパコニチンは互いに類縁体で、構造の細部は違っても、電位依存性Na⁺チャネルへ作用するという薬理の芯はそろっています。
この「類似構造が類似作用をもつ」という並びは、毒性学ではむしろ扱いが難しい部類です。
単一成分だけを見れば済む話ではなく、植物中に複数の関連成分が同居し、総体として毒性を形づくるからです。

附子への加工で毒性が下がるのも、このアコニチン系アルカロイドが加熱や加圧加熱で加水分解を受け、低毒性側の成分へ寄っていくためです。
長時間加熱でアコニンへ変化し、毒性が約200分の1になるという目安が示されるのはこの文脈です。
つまり、トリカブトの「毒が薬になる」という変化は、精神論ではなく、主成分の化学構造が変わることで生体作用の強さが落ちるという、きわめて物質的な現象です。
歴史的には矢毒として語られたり、推理小説で即効性の毒としてモチーフ化されたりもしますが、そうした描写には創作上の誇張も混ざります。
現実の危険性を支えるのは、神秘的な逸話ではなく、アコニチン系アルカロイドという分子群の具体的な作用です。
Na⁺チャネル持続活性化と症状の因果
アコニチン系アルカロイドの怖さは、電位依存性Na⁺チャネルを持続活性化する点にあります。
通常、Na⁺チャネルは一瞬だけ開いてNa⁺を流入させ、その後は速やかに不活化して、細胞膜電位を元へ戻すサイクルに入ります。
神経も心筋も骨格筋も、この「開く、閉じる、戻る」の拍子で動いています。
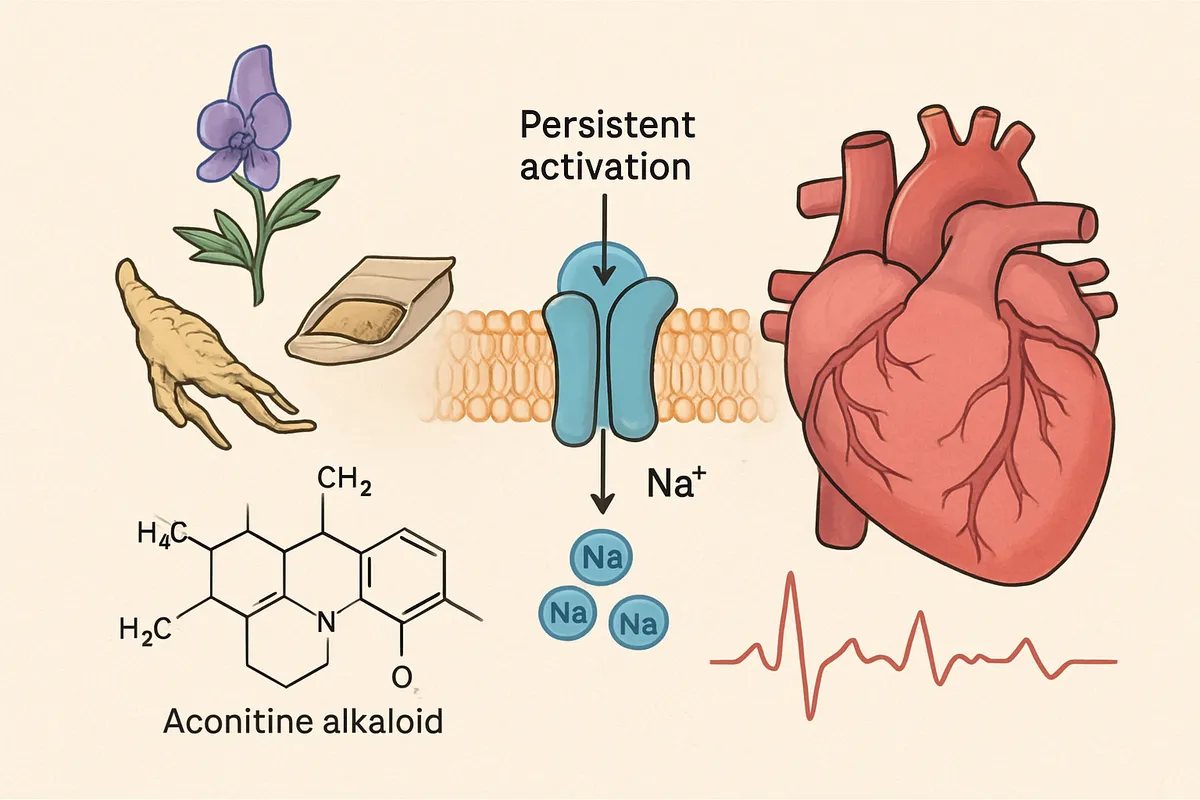
ところがアコニチンが結合すると、この拍子が壊れます。
チャネルが開口側に引き寄せられ、Na⁺の流入がだらだら続き、脱分極の持続が起こります。
私はNa⁺チャネル作動薬の電気生理波形を読んでいたとき、この状態を、立ち上がった活動電位の線が基線へ戻りきれず、中途半端に浮いたまま次の拍を待っている図として頭に刻みました。
押した鍵盤が戻らず鳴りっぱなしになるピアノという前の比喩を、もう少し電気生理寄りに言い換えるなら、スパイクを打ったあと膜電位が休める位置へ戻れず、やがて次の発火そのものができなくなる状態です。
これが脱分極ブロックです。
この機序から症状は一本の線でつながります。
神経では異常興奮がまず起こるため、口唇や四肢のしびれ、感覚異常、灼熱感が出ます。
その後、膜電位が戻れない時間が長くなると、今度は興奮を伝えられなくなり、筋力低下や麻痺へ傾きます。
興奮し続けた結果として、むしろ動けなくなるのがこの毒の厄介なところです。
心筋と刺激伝導系では、影響はさらに致命的です。
Na⁺チャネルの異常な活性化は、活動電位の立ち上がりと伝導タイミングを乱し、興奮伝導異常を引き起こします。
その帰結が不整脈です。
心室性不整脈、伝導障害、循環不全へ進む流れは、分子レベルの異常がそのまま臨床像へ出てきたものと考えると理解しやすくなります。
神経症状と心症状が別々に起こるのではなく、どちらも同じNa⁺チャネル障害の別の顔です。

ℹ️ Note
Na⁺チャネルは本来「瞬間的に開いてすぐ閉じる」スイッチです。アコニチン系はこのスイッチを半開きのまま固定するため、細胞は興奮し続け、やがて次の信号を作れなくなります。刺激が強すぎて沈黙に転じるのが、脱分極ブロックの本質です。
LD50・致死量・時間経過のデータ
アコニチンの毒性は、定量データで見ると切迫感がはっきりします。
実験動物でのLD50は、マウス点滴静注で0.166 mg/kg、マウス腹腔内で0.328 mg/kg、ラット経口で5.97 mg/kgと報告されています。
投与経路によって差が大きく、静注と経口では数値が約36倍離れます。
これは経口のほうが安全という意味ではなく、吸収や初回通過、種差などで毒性の見え方が変わるためです(出典例: PubChem(Aconitine)、関連論文検索:
ヒトの推定致死量は2〜6 mgとされる報告があり、これは0.002〜0.006 gに相当します。
臨床的な時間経過は速く、誤食では10〜20分で症状が出る例が多く、致死例は発症後6時間以内に集中することが報告されています。
一方で、24時間以上生存した場合は回復に向かう例も多いとされています(出典: 上記文献検索参照)。
この時間軸を頭に置くと、トリカブトがなぜ古くから恐れられてきたかも見えてきます。
危険なのは「珍しい強毒」だからではなく、ごく少量で、短時間のうちに、心臓と神経の両方を崩すからです。
毒の正体を分子で言い換えると、アコニチン、メサコニチン、ヒパコニチンがNa⁺チャネルの正常なオン・オフを壊し、細胞を戻れない脱分極へ追い込み、その結果として不整脈や麻痺が表面化する、という一点に集約されます。
附子とは何か――毒草が生薬になる境界
生薬と漢方薬の違い
ここでいったん、言葉の階層をほどいておきます。
薬学教育では、植物、そこから切り出した原料、さらにそれらを組み合わせた処方という順に並べた「生薬と方剤の階層」の図で学ぶことが多く、私自身もこの図で頭の中が整理されました。
読者が混同しやすいのは、トリカブトという植物と、附子という生薬と、附子を含む漢方薬が、ひとまとめに「漢方の薬草」のように語られがちな点です。
整理すると、生薬は単味の天然由来原料です。
附子、甘草、桂皮のように、一つひとつが部位・加工法・規格を持った原料として扱われます。
これに対して漢方薬は、複数の生薬を一定の考え方で組み合わせた処方、あるいはその製剤です。
葛根湯真武湯八味地黄丸は漢方薬であり、附子はその中に入る構成要素の一つです。
つまり、附子それ自体が「漢方薬」なのではなく、漢方処方を組み立てる材料の側にあります。

図にすると、関係は次のようになります。
| 階層 | 位置づけ | このテーマでの例 |
|---|---|---|
| 植物 | 自然界にある生物そのもの | 生のトリカブト |
| 生薬 | 植物の特定部位を加工・規格化した単味原料 | 附子、加工ブシ末 |
| 漢方薬 | 複数生薬を組み合わせた処方・製剤 | 真武湯八味地黄丸など |
この区別を入れておくと、「トリカブトが漢方薬になる」という言い方に少し補正が必要だとわかります。
正確には、トリカブトの塊根が加工されて附子という生薬になり、その附子が処方の一部として漢方薬に組み込まれる、という流れです。
植物から医薬へ向かう途中に、生薬という中間層があるわけです。
附子=塊根の加工生薬
附子(ブシ)は、トリカブト属植物の塊根を加工した生薬です。
ここでの核心は、附子が野山に生えている植物名ではなく、採取した根をそのまま置いた原料名でもなく、加工という工程を経て医薬品原料として扱われる名前だという点にあります。
前のセクションで見たように、トリカブトの毒性はアコニチン系アルカロイドに支えられています。
附子は、その強い毒性を持つ塊根に修治を施し、成分組成を変えたうえで生薬として扱うものです。
薬になる境界は、植物名が変わることではなく、部位の限定、加工、規格化がそろうことにあります。
毒草がそのまま薬棚に入るのではなく、医薬品として扱える形に切り替わったときに、初めて「附子」という名前で議論できます。

この違いを並べると、輪郭がはっきりします。
| 項目 | 生のトリカブト | 修治前の附子原料 | 加工附子(ブシ・加工ブシ末) | 処方中の附子 |
|---|---|---|---|---|
| 定義 | トリカブト属植物そのもの | 生薬化の前段階にある塊根原料 | 塊根を加工した生薬 | 複数生薬から成る漢方処方の一構成要素 |
| 位置づけ | 有毒植物 | 生薬原料 | 単味生薬 | 漢方薬の配合成分 |
| 成分の見え方 | アコニチン系アルカロイドが前面に出る | 加工前の毒性をなお保持する | 加工で成分組成が変化する | 他生薬との組み合わせの中で機能する |
| 安全性の担保 | なし | 製造前段階 | 修治・規格・品質管理 | 処方設計・製剤化・規格管理 |
この表で見落とせないのは、附子が単独で完結する概念ではないことです。
加工附子は生薬として独立していますが、実際の医療では真武湯麻黄附子細辛湯牛車腎気丸のような処方の中で位置づけられることが多い。
生薬学で原料として学ぶ段階と、臨床で方剤の一部として見る段階は、同じ「附子」でも見ている層が違います。
ℹ️ Note
附子を理解するときは、「植物名としてのトリカブト」「加工された単味原料としての附子」「処方に入った附子」の三段階に分けると混線しません。毒草と生薬と漢方薬は、同じ箱に入る言葉ではありません。
中国のFuziと日本の附子
中国医学でいうFuziは、国際的には Aconiti Lateralis Radix Praeparata と表記され、日本でいう附子とおおむね対応する概念です。
どちらもトリカブトの塊根を加工した生薬という点では重なっています。
ただし、名称が近いからといって、中身がそのまま同一とは言い切れません。
原料植物の扱い、加工法、流通上の規格に地域差があるからです。

薬学を学んでいると、この「近いが同じではない」という関係に何度も出会います。
Fuziと日本の附子もその典型で、一般的な教科書では対応語として並べられることが多いですが、現場では規格書を参照しないと同列には扱えません。
日本漢方の附子は日本薬局方や製剤規格の枠組みで整理され、中国のFuziは中医学の炮製体系や中国側の標準の中で運用されます。
塊根を加工して減毒し、医療に用いるという大きな骨格は共通していても、加工の細部や評価のものさしは一枚岩ではありません。
読者向けに要点だけをそろえるなら、次の理解で十分です。
生のトリカブトは植物であり、Fuzi/附子はその塊根を加工した生薬であり、さらに日本の漢方薬では附子が処方の一部として組み込まれます。
たとえば八味地黄丸や真武湯における附子は、中国語名をそのまま輸入した単独薬ではなく、日本の漢方処方体系の中で配合された生薬です。
この対応関係を意識すると、「Fuziは危険な毒根」「附子は漢方だから別物」といった二分法は崩れます。
実際には、同じトリカブト由来の塊根が、植物のままか、加工生薬か、処方中の構成要素かで意味を変えているだけです。
毒草が生薬になる境界とは、神秘的な変身ではなく、部位の選択、加工による減毒、そして規格化された医療材料への移行にあります。
減毒の核心は修治にある
修治の目的と代表的手法
附子への転換点は、採った根をそのまま使わないことです。
毒から薬への変化は名称の言い換えではなく、修治という加工工程によって成分の中身を動かすことで起こります。
ここで行われるのは、単なる乾燥や保存ではありません。
加熱、加圧加熱、塩類浸漬といった処理を通じて、アコニチン、メサコニチン、ヒパコニチンのようなアコニチン系アルカロイドを、より低毒性の側へ寄せていく操作です。
この話を用量の問題だけで理解すると、核心を外します。
私は前臨床段階で、原料加工の有無だけで安全域の見え方が大きく変わる事例を何度も見てきました。
同じ「何mg入っているか」を比べるだけでは説明できず、加工前後でそもそも危険性の輪郭が別物になっているのです。
附子の修治もそれと同じで、量を減らして帳尻を合わせる発想ではなく、原料そのものの危険性を作り替える安全性設計として理解したほうが実態に近いです。
化学的には、ポイントはアコニチン系成分が持つエステル結合です。
ここが加熱や加圧加熱などの条件下で加水分解を受けると、分子の性質が変わります。
すると脂溶性や、生体膜を通って標的に届く振る舞い、Na⁺チャネルへの結びつき方のダイナミクスも変わってきます。
反応式を細かく追わなくても、毒性の強い側の分子が、そのままではない別の組成へ移るという理解で十分です。

概念図として描くなら、こうなります。
脂溶性が高く、標的に強く食い込むアコニチン系があり、修治によって加水分解が進むと、より低毒性のアコニン類が増えていく。
一本の矢印で単純変換されるというより、複数の関連成分が時間と処理条件の中で少しずつ組成を変え、毒性の重心が移っていくイメージです。
附子が薬として成立する背景には、この組成シフトを見越した加工技術があります。
アコニチン→アコニンへのシフト
修治で注目されるのは、アコニチン系アルカロイドが加水分解を受け、低毒性のアコニン類へ比重が移ることです。
ここで起きているのは、毒成分が「消える」というより、強毒性の分子群が別の性質を持つ分子群へ変わるという化学変化です。
だから附子の減毒は、根性論的な“よく煮れば安心”ではなく、分子構造の変化に支えられています。
修治で注目されるのは、アコニチン系アルカロイドが加水分解を受け、低毒性のアコニン類へ比重が移ることです。
ここで起きているのは、毒成分が「消える」というより、強毒性の分子群が別の性質を持つ分子群へ変わるという化学変化です。
長時間加熱によって有毒アルカロイドがアコニンに変わり、毒性が約200分の1になると報告されることがありますが、これは特定条件下の実験に基づく目安にすぎません。
温度・時間・圧力・原料の前処理などの条件で結果は大きく変わり、家庭で同様の処理を試みることは危険です。
YMYL配慮と注意喚起
このテーマで踏み外してはいけないのは、修治を家庭で再現できる“下ごしらえ”のように読ませないことです。
加工の原理は説明できますが、具体的な温度、時間、圧力、浸漬条件のような手順は、そのまま危険情報になります。
附子の安全性は、加工という言葉だけで担保されるのではなく、規格化された原料、製造工程、成分管理がそろって初めて成立します。
⚠️ Warning
修治は料理の延長ではありません。毒草を食べられる形に近づける民間知ではなく、危険なアルカロイド組成を制御するための医薬品側の加工技術です。
この点はYMYL領域ではとくに明確にしておく必要があります。
トリカブト中毒は発症までの時間が短く、初動の遅れが致命的になりえます。
したがって、修治の話を「自分でも何とかできる」に接続してしまう書き方は避けるべきです。
ここで伝えたいのは再現法ではなく、毒から薬への転換が、経験則まかせではなく化学と品質管理に支えられているという構造です。
附子が医療の文脈で扱われるのは、生のトリカブトが安全になったからではありません。
危険な原料に対して、修治で成分を変え、規格で縛り、処方設計の中に位置づけるからです。
毒が薬になるのは神秘ではなく、加工技術の精度が境界線を引いているからだと言えます。
伝統薬から規格薬へ――日本薬局方と現代の安全管理
日本薬局方の位置づけ
日本薬局方の位置づけ
現代医療で附子が使われる前提には、経験則だけではなく国家規格としての日本薬局方があります。
日本薬局方は、医薬品の性状、品質、試験法、保存条件などを定める規格基準書で、生薬についても総則と各条の体系の中で「何を医療用原料として扱うのか」を切り分けています。
ここで線引きされるのは名称だけではありません。
外観や由来の確認、純度の見方、試験で確かめる対象、保存中に品質を崩さないための条件まで含めて、医薬品として流通させるための土台が整えられています。
このため、附子の安全性を語るときに「昔から使われてきた」という歴史だけを前面に出すと、現代医療の実像からずれます。
医療で扱われるのは、伝統的知識を出発点にしながらも、規格に適合する原料として評価されたものです。
個別成分の許容範囲や試験の細部は版の改訂で更新されうるため、最新の閾値や詳細条件は一次資料で確認すべき領域ですが、構造としては一貫しています。
附子は「伝統薬だから使う」のではなく、「規格薬として扱える状態にしているから使える」のです。

加工ブシ末と減毒処理の規格化
この規格化が具体的に見えるのが、加工ブシ末のような医療用原料です。
前のセクションで触れた修治は、ここでようやく「工程管理された減毒処理」として医薬品の文脈に入ります。
つまり、塊根を加工したという事実だけでは足りず、一定条件下で処理され、処理後の品質が評価され、規格に適合したものだけが原料として扱われるという流れが必要です(出典例: 日本薬局方/厚生労働省の解説)。
ここで大切なのは、減毒を神秘化しないこと。
加工によってアコニチン系アルカロイドの組成が低毒性側へ移ること自体は薬学的に説明できますが、医療現場で意味を持つのは「変わるはず」ではなく「変わったことをどう確認するか」です。
医薬品原料としての加工ブシ末は、その確認を前提にしています。
ℹ️ Note
附子の安全性は、毒を“弱めたら終わり”では成立しません。減毒処理を規格の言葉に置き換え、試験で合否を決められる状態にしたところで、はじめて医療用原料になります。
この点は、実験室で化学変化を追う視点と、医薬品供給の視点で見え方が変わります。
研究者は成分変換のメカニズムに目が向きますが、製剤や原料の実務では、メカニズムだけでは足りません。
ロット間で同じ品質を再現できるか、保存中に逸脱しないか、製造工程の中で管理点が設定されているかまで含めて初めて安全性が立ち上がります。
加工ブシ末は、伝統的な附子利用を現代医療へ接続するための橋であり、その橋脚は減毒そのものより減毒の規格化にあります。
品質管理と流通管理
附子が現代医療で成立する条件は、一言でいえば伝統知だけでなく、規格化、ロット管理、製造管理が一体になっていることです。
原料植物が同じでも、医療用に流通するものは、製造段階で管理されたロットとして扱われ、規格試験を通過し、製剤化の工程でも管理されます。
ここにGMPの発想が重なります。
どの原料を、どの工程で、どの条件のもとに扱い、どのロットが市場に出たのかを追える状態にしておくことが、医薬品としての信頼性を支えます。
私が規格文書を読んでいていつも感じるのは、安全性は「危険成分がゼロであること」よりも、「危険を含む原料を、どこまで把握し、どこまで一定に保てるか」で決まるということです。
附子はこの考え方がそのまま当てはまる生薬です。
もともと強い毒性をもつ植物由来原料だからこそ、曖昧な民間的運用ではなく、測定、判定、記録、出荷判定という地道な管理の積み重ねが要ります。
安全性の中心は、経験談の蓄積というより、測定可能な品質項目として管理されていることにあります。
そのため、現代の附子を「昔の毒草の名残」と見るだけでは不十分です。
実態は、伝統的に知られてきた薬効の知識を起点にしながら、国家規格で枠をつくり、製造者が品質評価を行い、ロット単位で流通を管理することで、医療で扱える原料へ変換したものです。
個別の成分上限値や最新の規格細目は改訂に伴って確認が必要になる領域ですが、読者が押さえるべき骨格は明快です。
附子の安全性は、伝統知に規格化を重ね、さらに品質管理と流通管理で固定したときにだけ成立する。
この順番を外すと、生薬と毒草の境界はたちまち曖昧になります。
附子を含む漢方処方の代表例
八味地黄丸・牛車腎気丸
附子がどのように漢方処方の中で働くかを見るとき、まず名前が挙がるのが八味地黄丸と牛車腎気丸です。
どちらも、単に「体を温める生薬が入っている処方」と見るだけでは足りません。
漢方では、冷え、下肢のだるさ、排尿の不調、痛みの背景にある機能低下をひとまとまりの病態として捉え、その中で附子は冷えを伴う停滞を動かす役割を担います。
とくに「腎陽虚」と表現される領域では、温める力が落ち、巡りも鈍くなり、水分代謝や疼痛の訴えが重なりやすくなります。
八味地黄丸はその中心的な設計として理解されることが多く、牛車腎気丸はそこに下肢症状や水滞のニュアンスを強めた発展形として位置づけられます。
学術レビュー(例えばPubMed上の総説検索)でも、加工附子の薬理と臨床応用は、寒証寄りの疼痛や循環低下、水分代謝の乱れを含む文脈で整理されています。
この2処方で注目したいのは、附子が単独で前に出るのではなく、地黄剤の骨格の中で配置されていることです。
漢方処方は、いわゆる君臣佐使の考え方に沿って、主役の効き目だけでなく、補助、生体反応の調整、偏りの緩和まで含めて組み上げられます。
附子は温める方向に力を持つ一方、それだけでは処方として粗くなりかねません。
複数生薬との配合、製剤ごとの用量設計、製造段階での規格化が重なって、効果の焦点と安全域が整えられています。
読者が見るべきなのは「附子が入っているか」だけでなく、どの処方の中で、どんな役割を割り当てられているかです。

真武湯
真武湯も、附子の位置づけを理解するうえで欠かせない代表処方です。
こちらは、冷えに加えて水分代謝の乱れや全身の力の落ち込みが前景に出るときに語られることが多く、めまい感、ふらつき、むくみ、下痢傾向、倦怠感などがひとつの像としてまとまります。
附子はその中で、落ち込んだ温める力を支える軸として入り、単に温熱刺激を足すのではなく、処方全体の「沈んだ状態を持ち上げる」働きに組み込まれています。
附子配合処方のレビューを通覧すると、真武湯のような方剤は、冷えと浮腫と倦怠が重なる場面で繰り返し現れます。
これは偶然ではなく、附子が古典的に「寒」と「痛」だけの生薬として扱われてきたわけではないことを示しています。
実際には、冷えによって水の動きが滞り、結果として体が重く、だるく、痛みも出るという連なりの中に置かれてきました。
真武湯はその典型で、附子の役割を「温める」一語に縮めてしまうと、処方の半分を見落とします。
麻黄附子細辛湯
麻黄附子細辛湯は、附子の使われ方にもう一つの輪郭を与えてくれる処方です。
名前の通り、麻黄附子細辛という少数精鋭の構成で、寒邪を受けたときの反応が弱く、ぞくぞくするのに強く発散できない、という像に当てはめて理解されることが多い処方です。
ここでの附子は、慢性的な腎陽虚の文脈だけでなく、冷えを背景にした反応性の低下に対して、内側から火力を補う位置に置かれます。
痛みでいえば、冷えてこわばる、神経痛様の訴えを伴う、といった場面との相性が語られてきました。

この処方は、附子が他生薬とどう組むかを考える教材のような存在でもあります。
麻黄は表を開く方向、細辛は温めながら通す方向、附子は内側の陽気を支える方向へ働き、三者が別々に並んでいるのではなく、寒さで閉じた状態をほどくひとつの設計になっています。
君臣佐使という言い方を使うなら、附子は決して「毒の強い生薬を少し足している」だけではなく、処方の軸を補強する役に回っています。
しかもその働きは、単味利用ではなく、配合量と組み合わせの中で立ち上がります。
消費者の目線で見ると、同じ名前の処方でも製剤ごとに生薬構成や規格の表記の見え方が異なることがあります。
そのため、附子の有無や位置づけは、製品説明書や承認書に基づく情報で読むのが筋です。
ここを自己流で増量したり、附子を含む複数処方を安易に重ねたりすると、処方設計そのものを崩してしまいます。
附子は単独成分の強さだけで理解するより、規格化された処方の中で、冷えや疼痛を伴う病態へどう組み込まれているかで読むほうが、薬効の位置づけも安全性の境界も見失いません。
なぜ減毒しても効くのか

多成分系としての薬理
ここで読者がいちばん引っかかるのは、「毒を減らしたなら、効き目まで薄れてしまうのではないか」という点だと思います。
附子の理解で外せないのは、修治の狙いが有毒成分をゼロにすることではなく、毒性を下げながら、薬としての作用プロファイルを組み替えることにある、という点です。
加工後の附子は、単に“弱くなったトリカブト”ではありません。
成分が入れ替わり、比率が変わり、別のふるまいを示す変化後の多成分系として扱うほうが実態に近いです。
薬理学では、単一成分の薬なら「この分子がこの受容体に作用する」と整理できます。
ところが附子はそう単純ではありません。
もともとのアコニチン系アルカロイドが加熱や加圧加熱で加水分解を受けることで、毒性の強い側の成分が減り、低毒性側の成分が前面に出てきます。
そこへ、附子にもともと含まれる他の成分群や、処方に組み合わされる茯苓白朮芍薬地黄などの生薬が重なります。
読者が見ているのは「1つの毒を抜いた残り」ではなく、組成が変わったうえで、さらに配合で意味づけされた薬系なのです。
私は製薬企業の安全性研究で、多成分製剤の評価がどれほど難しいかを何度も見てきました。
単一化合物なら標準品の純度と濃度を揃えれば比較の軸が立ちますが、生薬や多成分系はロットごとの化学指紋が少しずつ動きます。
標準化を詰めても、バイオアッセイでは細胞の反応幅が想像以上に揺れます。
効いた・効かないを一本線で割り切れないのは、実験が粗いからではなく、対象そのものが複数成分のネットワークだからです。
附子で「減毒したのに、なぜまだ効くのか」という問いが難しいのは、まさにこの点にあります。
効き目は1成分の残量だけでは決まらず、変化後の全体設計で決まるからです。
ℹ️ Note
附子の薬効を理解するときは、「毒性成分が残っているから効く」「毒を抜いたのに効くのは不思議だ」という二択で考えないほうが正確です。実際には、修治によって成分の顔ぶれと比率が変わり、薬理の輪郭そのものが再設計されます。
低毒性側アルカロイドの寄与
その再設計の中心候補としてよく挙がるのが、加工後に増えるアコニン類のような低毒性側アルカロイドです。
前段で見たように、加熱後には毒性の強いアコニチン系が減り、低毒性側へ化学変換が進みます。
ここで大事なのは、「低毒性だから無関係」ではないことです。
毒性が下がることと、生体作用が消えることは同義ではありません。
むしろ修治は、強すぎるNa⁺チャネル作動性を弱めつつ、別の作用の寄与が見えやすい配合状態へ持っていく工程として理解したほうが筋が通ります。
近年の総説を読んでいると、加工附子の作用は、低毒性側アルカロイドだけで完結するというより、複数成分の相乗と拮抗のつり合いで立ち上がっている、という整理が妥当です。
痛み、冷え、循環、代謝、収まりません。
附子単味でも多成分ですが、漢方処方に入るとその傾向はさらに強まります。
たとえば真武湯で見える“冷えと水滞と倦怠”のまとまりは、附子だけを抜き出しても再現しきれません。
附子の低毒性側成分が土台をつくり、他生薬が方向づけを与える、と考えると処方全体の挙動が読みやすくなります。
安全性の視点から見ても、この「低毒性側の寄与」は都合のよい物語ではありません。
毒性成分が減ることで急峻なリスクを抑えつつ、残った成分群が薬理に関与するなら、修治は単なる無害化ではなく機能の選別です。
食品安全の文脈で語られる「長時間加熱で毒性が約200分の1になる」という目安は、その変化の大きさを示しています。
ただし、この数字は特定条件下の報告に基づく目安であり、具体的な温度・時間などの手順は製造管理下で評価されるべきもので、家庭での再現や試行を推奨するものではありません。
未解明領域と研究課題
とはいえ、「なぜ減毒しても効くのか」は、まだ教科書的に一行で片づく話ではありません。
未解明の部分は確実に残っています。
とくに難しいのが、成分間相互作用と体内動態です。
加工後に生じる複数の低毒性成分が、吸収・分布・代謝の各段階でどう振る舞うのか、さらに処方中の他生薬がその流れをどう変えるのかは、まだ粗い地図しかありません。
細胞実験で反応が見えても、体内で同じ比率のまま作用するとは限らず、逆に微量成分が全体の効き目の鍵を握ることもあります。
この分野で研究を難しくしているのは、評価系そのものの設計です。
ロット再現性を高めるには化学分析を細かく刻む必要がありますが、化学的に揃えたからといって、生物活性が同じ顔を見せるとは限りません。
逆に、バイオアッセイで似た反応が出ても、どの成分の組み合わせが効いていたのかを切り分けるのは骨が折れます。
私が安全性試験にいた頃も、多成分系の試験は「測れているもの」と「本当に知りたいもの」のあいだにずれが生まれやすい領域でした。
附子研究で結論が慎重になるのは、このずれが無視できないからです。

現時点で言えるのは、加工附子はゼロ化された無成分の残骸ではなく、変化後の成分群として薬理を持つということ、そして毒性低下と薬効保持の両立こそが修治の設計思想だということです。
そのうえで、どの成分が主役で、どの相互作用が処方の輪郭を作っているのかは、まだ解き切れていません。
この未解明部分があるからこそ、附子は「昔の経験知で説明できる薬」でも「単成分化学で全部読める薬」でもなく、その中間にある、いまなお研究対象として面白い生薬のまま残っているのです。
毒と薬の境界から見える医学史
用量vs加工という二軸
パラケルススの「用量が毒を決める」という命題は、毒性学を学ぶ者にとって出発点です。
実際、同じ物質でも量が変われば作用の顔つきは変わります。
ただ、附子の歴史を追うと、それだけでは足りないことが見えてきます。
薬を成立させるのは用量だけではなく、加工と規格です。
トリカブトはそのままでは毒草であり、附子はそこから切り出された塊根を修治し、生薬として扱える形にしたものです。
ここで起きているのは、単なる「量の調整」ではありません。
成分組成そのものを変え、危険なピークを鈍らせ、医療で扱うための輪郭を作る工程です。
パラケルススの言葉を現代的に言い換えるなら、「用量が毒を決め、加工が薬の入口を作る」と表現したほうが、附子にはよく当てはまります。
私は研究現場で、同じ名前の原料でも、規格が立っていない試料は議論の土台にならない場面を何度も見てきました。
濃度だけ揃えても、前処理や品質のばらつきが残れば、データは医学の言葉になりません。
そう考えると、伝統医療が附子に施してきた修治は、経験の蓄積であると同時に、薬学的には再現可能性を獲得するための知恵でもありました。
毒と薬の境界は、量の境目という一本線ではなく、加工というもう一つの軸を持つ面として理解したほうが実態に近いのです。
規格化がもたらした医療の安定
この二軸の考え方は、近代医学に入ると「規格」という形で制度化されます。
日本薬局方が担ってきた役割は、そこにあります。
原料の同定、品質の確認、成分のばらつきの管理がそろって、はじめて生薬は医療の中で安定した位置を持てます。
附子が象徴的なのは、毒草の時点では自然物でしかなかったものが、加工と規格を経て、ようやく医薬の言語に翻訳された点です。
伝統知と現代薬学は、しばしば対立的に語られます。
しかし附子を見ると、両者はむしろ接続しています。
経験的に積み上げられた「どう扱えば危険なまま終わらないか」という知恵が先にあり、現代薬学はその知恵を成分変化、毒性低減、品質管理の言葉で読み直してきました。
修治は迷信の名残ではなく、規格科学へ橋を渡すための前段だった、と捉えると医学史の流れがきれいにつながります。

研究や製造の現場にいると、規格書は地味な紙に見えて、実際には安全性のインフラそのものだと痛感します。
試験法、受け入れ基準、ロット管理のどれが欠けても、薬は「効くらしいもの」に後退します。
附子が今も生薬として残っているのは、毒を消し去ったからではなく、危険を評価可能な形に変え、一定の品質で扱えるようにしたからです。
そこに、伝統知が近代医療へ生き残る条件が凝縮されています。
ℹ️ Note
医学史の観点で見ると、附子は「毒が薬になった例」というより、「毒を薬として扱うための加工・規格・制度が育った例」と読むほうが、本質を取りこぼしません。
クラスター記事への導線
この視点は一つの生薬解説で終わるものではなく、関連トピックを横断することで深まります。
将来的に当サイトで作成すると有用な関連記事候補として、以下の内部ページタイトルを提案します(サイト内記事が整備され次第、本稿からリンクを設置してください)。
- 毒物図鑑: 「トリカブト(Aconitum)概説」——分類・分布・毒性の図鑑エントリ
- 生薬規格: 「附子の製造・規格と試験法」——修治工程と規格化の実務的解説
- 臨床と処方: 「附子配合処方の臨床エビデンス概観」——代表処方と臨床データの総覧
これらの候補は、読者が本記事の次に読みたい情報へ自然につながる導線です。サイト内記事が用意でき次第、本文中の該当箇所から内部リンクを張ることを推奨します。

薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
毒から薬へ|毒性のある物質が医薬品になる条件
毒はなぜ薬になりうるのか。この問いに答える鍵は、毒=悪、薬=善という単純な線引きではなく、用量・投与経路・標的選択性・規制という4つの条件にあります。非臨床安全性研究で用量反応曲線を組むとき、初期毒性兆候をどこで拾い、どの投与量をNOAELやLOAELとして切るかを詰める作業そのものが、
ボツリヌス毒素からボトックスへ|最強の毒が美容医療を変えた
ボツリヌス毒素は「最強の毒」とだけ語ると、本質を見失います。毒性学の実務でまず見るのは、何mgかではなく、どこに、どれだけ、どの経路で入るかという三つで、全身に回る中毒と、医師が局所へごく微量を打つ医療は、同じ物質でも意味がまるで変わります。 ボツリヌス毒素は毒と薬という二面性を持つ分子です。
ジギタリスの物語|毒から薬、そして再評価
花壇では優美に見えるジギタリスは、ひとたび体内に入れば心臓に触れる毒でもあります。その危うい植物が、18世紀の観察医学から現代の薬理学へどう橋を架け、心不全治療の景色をどう変えたのかを追うのが本稿です。
抗毒素と血清療法|北里柴三郎が開いた道
北里柴三郎を語るとき、主役は人物名だけでは足りません。焦点に置くべきなのは毒素そのものと、それを狙い撃ちで中和する抗毒素、そしてその抗体を投与して即効性を引き出す血清療法という発想です。