毒から薬へ|毒性のある物質が医薬品になる条件
毒から薬へ|毒性のある物質が医薬品になる条件
毒はなぜ薬になりうるのか。この問いに答える鍵は、毒=悪、薬=善という単純な線引きではなく、用量・投与経路・標的選択性・規制という4つの条件にあります。非臨床安全性研究で用量反応曲線を組むとき、初期毒性兆候をどこで拾い、どの投与量をNOAELやLOAELとして切るかを詰める作業そのものが、
毒はなぜ薬になりうるのか。
この問いに答える鍵は、毒=悪、薬=善という単純な線引きではなく、用量・投与経路・標的選択性・規制という4つの条件にあります。
非臨床安全性研究で用量反応曲線を組むとき、初期毒性兆候をどこで拾い、どの投与量をNOAELやLOAELとして切るかを詰める作業そのものが、「用量が毒を決める」を現場の言葉に置き換えたものだと実感します。
本記事は、毒性学に関心のある読者はもちろん、医薬の歴史をひとつの筋で理解したい人に向けて、パラケルススの原理、1910年に登場したサルバルサンこと606号、そして1989年と2010年のFDA承認で医療の地位を固めたボツリヌス毒素を、近代毒性学の流れの中で一気に見通せるように構成しました。
同じ「猛毒」でも、全身投与される有機ヒ素薬が薬になる条件と、局所微量投与される神経毒タンパク質が薬になる条件は同じではありません。
毒と薬の境界は曖昧なのではなく、科学と制度によって厳密に引き直されてきた――その輪郭を、この三本柱からたどります。
毒と薬はなぜ入れ替わるのか
毒性学と薬理学はどこで交わるか
同じ物質が、ある場面では毒として振る舞い、別の場面では薬として働く。
この一見すると矛盾した現象は、毒性学ではむしろ基本原理として扱われます。
毒性学が見ているのは「その物質が危険か安全か」という固定ラベルではなく、どの量が、どの経路で、どれくらいの時間、どの臓器に届いたときに、どんな反応を起こすかです。
吸収・分布・代謝・排泄まで含めて反応全体を追うので、同じ化学物質でも条件が変われば評価は入れ替わります。
ここで薬理学と毒性学は一本の線でつながります。
薬理学は、ある物質が標的に作用して望ましい効果をどこで示すかを見る学問です。
毒性学は、その延長線上で望ましくない作用がどこから現れるかを見る学問です。
つまり両者は対立概念ではなく、同じ反応曲線の別の領域を読んでいるにすぎません。
治療効果と有害作用を切り離して考えるのではなく、ひとつの連続した現象として捉えるところに接点があります。
製薬の安全性研究にいたとき、私はこの境界が案外日常的な薬にもそのまま当てはまることを何度も見てきました。
たとえばNSAIDsのような鎮痛薬は、痛みや炎症を抑えるという意味では典型的な治療薬ですが、量や投与期間が積み重なると胃粘膜保護に関わるプロスタグランジン産生まで抑えてしまい、胃粘膜障害や潰瘍という形で代償を払わせます。
毒から薬になる物質だけが特別なのではなく、ふつうの薬もまた、用量の線を越えれば有害作用の側へ移るのです。
この発想は、16世紀のパラケルススが示した「用量が毒を決める」という原理にさかのぼれます。
近代以降、この考え方は感覚的な格言ではなく、実験と定量の体系へ変わりました。
さらに19世紀にはオルフィラが毒物学を学問として整え、20世紀以降は安全性試験や医薬品開発の中で、用量反応関係を数値として詰める方法が確立していきます。
いま毒性学が安全性評価の中核にあるのは、この原理が歴史的な比喩ではなく、現場の判断基準として機能しているからです。
用量反応関係の基本
用量反応関係をひとことで言えば、「入った量に応じて反応の強さや頻度がどう変わるか」を見る考え方です。
低い用量では目立った変化が起こらず、ある範囲に入ると反応が現れ、さらに増やすと反応が強まっていく。
この全体像は、なだらかに立ち上がって途中で急になり、やがて頭打ちになるシグモイド曲線としてイメージするとつかみやすくなります。
この曲線を読むうえで要になるのが閾値です。
一定の条件では、そこまでは有害影響が観察されないという領域があり、その上で初めて毒性の兆候が見えてきます。
非臨床試験で使うNOAELとLOAELは、この境目を実務で切り分けるための言葉です。
前者は有害影響が観察されなかった最大投与量、後者は有害影響が観察された最小投与量を指します。
実際に用量設定を詰める作業では、この境界がきれいな一本線として現れることは少なく、肝酵素の上昇、体重変化、病理所見のそろい方を見ながら、どこから「有害」と判定するかを丁寧に詰めます。
ただし、ここで「閾値があるなら、その下は絶対安全だ」と短絡しないことも同じくらい欠かせません。
生体反応には幅があります。
代謝酵素の活性、年齢、併用薬、臓器機能、局所への届き方の違いで、同じ投与量でも反応の出方はそろいません。
曲線は一人ひとりで少しずつ位置がずれ、その集まりとして集団のデータが形になります。
だから医薬品開発では、単に平均値を見るだけでなく、安全係数をかけたり、曝露量を比較したりして、余裕を持った設計を行います。
薬理学との接点もここにあります。
薬の有効性もまた、用量反応曲線で評価されるからです。
量が足りなければ効かず、増やすと効果が立ち上がり、あるところで飽和する。
この有効性の曲線と、有害作用の曲線の位置関係が、臨床で言う治療域を形づくります。
効く量と害が出る量のあいだに幅がある薬は扱いやすく、両者が接近している薬は緻密な管理が要ります。
つまり「薬理作用」と「毒性」は別世界の話ではなく、標的に届いた量に対する生体応答を、望ましいか望ましくないかで読み分けているだけです。
ℹ️ Note
毒と薬を分ける境界は、物質名の横に貼られたイメージではなく、用量反応曲線のどこを使うかで決まります。同じ物質でも、全身に広く届くのか、局所に少量だけ届くのかで、その曲線上の立ち位置は変わります。
比較の地図を描く

この原理を歴史の中で見ると、対照的な二つの例がよく効いてきます。
ひとつは1910年に発表された有機ヒ素製剤サルバルサンです。
エールリッヒと秦佐八郎がたどり着いたこの606号は、毒性を抱えた物質を無理に無害化したというより、病原体に選択的に効かせるという発想で薬へ引き寄せた例でした。
全身投与される薬である以上、毒性との綱引きは避けられません。
それでも、標的選択性を意識した化学療法という考え方を前に進めた点で、毒と薬の境界を科学で描き直した歴史的な一歩でした。
もうひとつはボツリヌス毒素です。
こちらは神経伝達を担うアセチルコリン放出を遮断し、弛緩性麻痺を起こす神経毒タンパク質です。
ところが医療では、この作用そのものを局所で使います。
標的は神経筋接合部で、投与は微量かつ局所に限る。
全身を広く曝露させるのではなく、必要な場所だけに届かせる設計が鍵でした。
1989年に斜視や眼瞼痙攣で米国承認を受け、その後は適応が広がり、2010年には慢性片頭痛の予防でも承認されました。
ここで薬になった理由は、「毒なのに安全だった」からではありません。
強い作用を局所・微量・限定標的で使いこなせたからです。
この二つを並べると、毒が薬になる道筋はひとつではないことが見えてきます。
サルバルサンは全身投与の中で選択毒性を狙った例であり、ボツリヌス毒素は局所投与で全身曝露を抑えた例です。
片方は化学療法の発想、もう片方は投与設計の洗練が決め手でした。
そして両者を共通言語としてつないでいるのが、用量反応関係です。
比較の軸を整理すると、読み方がぶれません。
| 項目 | サルバルサン | ボツリヌス毒素 | 用量反応の原理 |
|---|---|---|---|
| 主な時代 | 20世紀初頭 | 20世紀後半から現代 | 16世紀に発想が示され、現代で定量化 |
| もとの性格 | 有機ヒ素化合物 | 神経毒タンパク質 | 個別物質ではなく評価の枠組み |
| 薬になった鍵 | 選択毒性と化学療法の発想 | 局所微量投与と標的限定 | 用量と反応の対応を定量的に読むこと |
| 読み解く視点 | 全身投与で利益と毒性をどう釣り合わせるか | 局所曝露で作用をどう閉じ込めるか | 有効性と有害性を同じ地図に置くこと |
ここで避けたいのは、「劇薬だから危険」「猛毒なのに薬になるのは不思議」といった二分法です。
そうした見方では、サルバルサンとボツリヌス毒素の違いも共通点も見えません。
科学的には、問うべきなのは強さの序列ではなく、どの標的に、どの量が、どの経路で届き、その結果として利益と不利益がどう並ぶかです。
毒性学は、その比較地図を描くための学問です。
薬理学は、その地図の中で治療効果の位置を定める学問です。
毒と薬が入れ替わるように見える場面も、この地図の上に置けば、むしろ筋道だった現象として読めるようになります。
パラケルススが示した用量が毒を決める原理

すべては毒発言の真意と誤解
パラケルスス(1493-1541年)は、「すべてのものは毒であり、毒でないものはない。
用量だけが毒であるか否かを決める」という趣旨の言葉で知られます。
近代毒性学の出発点として頻繁に引かれるのは、この一文が毒と薬を別々の箱に入れる見方を崩したからです。
物質そのものに固定的な善悪の札が付いているのではなく、どれだけ体内に入り、どこに届き、どの反応を引き起こすかで評価が変わる。
医薬と毒の境界を、性質ではなく条件で捉える発想がここにあります。
この言葉はしばしば「少量なら何でも安全」という意味に短縮されますが、そこまで単純ではありません。
パラケルススが示したのは、毒性を量の問題として考える視点です。
現代の毒性学では、そこに曝露期間、投与経路、標的臓器、吸収・分布・代謝・排泄まで加えて読みます。
つまり「用量が毒を決める」は、単なる格言ではなく、反応を定量的に読むための入口です。
私自身、安全性研究で用量設定を詰めていたとき、この言葉は歴史上の名言というより、毎日の判断基準そのものでした。
ある所見を薬効の延長とみるのか、有害影響の始まりとみるのかは、結局のところ用量反応の積み上げで決まります。
前述のNOAELやLOAELも、その境界を実験データの上に引き直したものです。
16世紀の哲学的な提起が、現代では試験計画や用量設定の言葉に置き換わって生きています。
用量反応曲線と治療域/治療指数
現代の枠組みに引き寄せると、パラケルススの原理は用量反応曲線として視覚化できます。
用量が上がるにつれて効果や有害反応の頻度・強さがどう変わるかを描いたもので、薬効も毒性もこの同じ地図の上に載ります。
低用量では反応が乏しく、ある領域で立ち上がり、さらに増量すると有害作用の曲線が近づいてくる。
この位置関係が、薬として使えるかどうかを左右します。
ここで混同しやすいのが、治療域と治療指数です。
治療域は、臨床で有効性を得つつ毒性域に踏み込まない濃度や用量の幅を指します。
いわば実地で守るべき運転レーンです。
これに対して治療指数(TI)は、古典的には LD50/ED50 で表される比で、理論上どれだけ安全マージンがあるかを見る指標です。
数値が大きければ扱える幅が広い方向を示しますが、TI がひとつ分かれば臨床安全性のすべてが見えるわけではありません。
毒性の質、作用機序、モニタリングの可否、治療目的によって実際のリスクは変わるからです。
このあたりは、非臨床から臨床初期への流れを見ると連続性がつかめます。
非臨床では反復投与試験などからNOAELを置き、そこからヒト等価用量や曝露比較を踏まえて安全域を組み立てます。
初回ヒト投与、つまりFIHの開始用量を決める場面でも、発想の芯は同じです。
動物でどこまで有害影響が出なかったかを起点に、人でどこから入るべきかを慎重に下ろしていく。
現場感覚としては、非臨床で引いた安全域の線が、臨床初期で別の単位系に翻訳されるだけで、思想そのものは切れていません。
パラケルススの原理は、ここで安全係数を伴う開発実務に姿を変えています。
💡 Tip
治療域は「どこで使うか」の幅、治療指数は「どれだけ離れているか」の目安です。同じ安全性の話でも、見ているものは一致しません。
投与経路が左右する安全性

同じ量でも、どの経路で入るかによって反応は変わります。
経口なら消化管から吸収され、肝臓での初回通過を受けます。
皮下や筋肉内では、組織からの吸収速度や局所滞留が効いてきます。
静脈内投与ではその過程を飛び越えて、物質が直接全身循環に入ります。
局所投与では、標的部位に濃度を集めながら全身曝露を抑える設計が可能になります。
毒性学で投与経路が必ず記載されるのは、体に入る量だけでなく、体に届く形が変わるからです。
この違いは、医薬と毒の境界を考えるときにとくに効いてきます。
たとえば同じ有害作用を持つ物質でも、経口で全身に広く回る場合と、局所に限って少量を投与する場合では、危険の質が別物になります。
製剤開発や安全性評価で経口、皮下、筋注、静注、局所を分けて考えるのは、形式的な分類ではありません。
吸収速度、最高濃度、局所濃度、標的到達性がそれぞれ変わるためです。
後段で触れるボツリヌス毒素は、この投与経路の発想が薬理と毒性の境界を書き換えた典型です。
神経伝達を遮断する強い作用そのものは変わらなくても、局所に微量を置き、全身曝露をできるだけ小さく抑えることで、毒性の地図上の位置が動きます。
ここでは「毒が弱くなった」のではなく、届かせ方を制御したことが薬への転換点でした。
パラケルススの用量原理は、現代では投与経路の設計と一体で読まれます。
オルフィラがもたらした体系化
パラケルススが残したのは、毒と薬を量の問題として見る哲学的な軸でした。
その軸を学問として組み立てた人物として位置づけられるのがオルフィラ(1787-1852)です。
役割分担でいえば、パラケルススは原理の提起者、オルフィラは毒物学の体系化を進めた創始者です。
実験的な検討、毒物の分類、法医学への応用を通じて、毒物学は経験談や警句の集積から、検証可能な学問へと移っていきました。
この流れがあったからこそ、毒性学は近代以降、物質の有害作用だけでなく、その発現機序、用量反応関係、吸収・分布・代謝・排泄まで含めた学問になりました。
パラケルススの一文だけでは、まだ「どのように測るか」は示されていません。
オルフィラ以後の毒物学は、その問いに実験で答える方向へ進みます。
毒を語る言葉が、印象や逸話ではなく、観察・測定・比較の言葉へ変わったわけです。
この橋渡しを押さえておくと、サルバルサンのような有機ヒ素化合物も、ボツリヌス毒素のような神経毒タンパク質も、同じ地図の上で読めるようになります。
片方は全身投与で選択毒性を追い、もう片方は局所投与で全身曝露を抑える。
手法は異なっても、背後にある共通言語は用量反応関係です。
パラケルススが開いた扉を、オルフィラが学問の形に整え、その先で近代薬理学と毒性学が接続した。
その流れの上に、現代の安全性評価も立っています。
ヒ素はどうして梅毒治療薬になったのか|サルバルサンの登場

前史:アトキシルの限界
ヒ素が梅毒治療に結びついた背景には、19世紀末から使われていたヒ素系薬剤アトキシルの存在があります。
アトキシルは当時、感染症に対して「化学物質で病原体をたたく」という発想を現実の治療へ押し出した薬剤のひとつでした。
ここに、のちに化学療法(ケモサラピー)と呼ばれる考え方の芽があります。
病気を体質や気分の乱れとしてではなく、特定の病原体を標的にして制御する対象として扱う視点です。
ただし、アトキシルは理想的な薬ではありませんでした。
効く可能性はあっても、副作用が重く、使いこなすには大きな代償を伴いました。
ヒ素化合物は病原体に作用しうる一方で、宿主側にも毒性を示します。
つまり、効力と有害性が近接しており、前節で見た治療域の問題がそのまま突きつけられていたわけです。
ヒ素を含むから危険だった、というより、どの形のヒ素化合物なら病原体により強く当たり、ヒトには相対的に軽く済むのかがまだ分かっていなかった段階だったと見るほうが正確です。
この時代の試行錯誤を振り返ると、毒物学と薬理学の境界がまだ粗く、同時に近代的な発想の核だけはすでにあったことが見えてきます。
危険な元素を避けるのではなく、化学構造を変えて標的への当たり方を調整する。
この感覚は、現代の創薬研究にいるとごく自然に思えますが、当時はまだ新しい挑戦でした。
606号の検証と1910年発表
この流れを決定的に変えたのが、パウル・エールリッヒと秦佐八郎の共同研究です。
エールリッヒは、化合物を系統的に合成・評価し、病原体に効いて宿主への害が抑えられる分子を探すという方法を進めていました。
経験や偶然に頼るのではなく、候補化合物を番号で管理しながら一つずつ検証していくやり方です。
その到達点として知られるのが606号です。
1909年に秦佐八郎がこの606番目の化合物の有効性を確認し、梅毒病原体に対して強い作用を示すことが見いだされました。
これがのちのサルバルサンです。
そして1910年4月19日、この成果がサルバルサンとして発表されます。
年号を明確に押さえると、1909年が有効性確認、1910年が公表と整理できます。
魔法の弾丸と選択毒性
エールリッヒを語るときに欠かせないのが、魔法の弾丸という比喩です。
狙った標的だけを撃ち抜き、それ以外には当たらない弾丸があれば、感染症治療はもっと合理的になる。
この発想を薬理学の言葉に置き換えたものが選択毒性です。
病原体には強く作用し、ヒトにはそれより弱く作用する。
その差を利用して治療を成立させる考え方です。
サルバルサンは、この選択毒性を近代医療の中で具体化した初期の代表例でした。
ヒ素は本来、毒として認識されていた元素です。
しかし、化合物の形を変えれば作用の向き先も変わる。
言い換えると、毒性は元素名だけでは決まらず、化学構造、標的への親和性、体内での振る舞いで姿を変えます。
サルバルサンはその事実を、感染症治療という切実な場面で証明しました。
この意味でサルバルサンは、のちの抗菌化学療法の基礎に置かれる存在です。
抗生物質時代の前夜に、化学物質で病原体を狙い撃つという路線を現実の医療へ持ち込んだからです。
毒を薄めて薬にしたというより、毒の向かう先を選ばせることで薬にした、と捉えると本質が見えます。
ℹ️ Note
サルバルサンの革新性は、ヒ素を無害化したことではなく、病原体と宿主のあいだにある感受性の差を治療へ変換した点にあります。
毒性と標準化の課題

もっとも、サルバルサンは理論の勝利そのままに、扱いやすい完成品として現れたわけではありませんでした。
実地では、溶解性、安定性、投与管理の難しさがつきまといます。
調製の段階で不安定になりやすく、投与手順にも注意が要る。
化学療法の出発点であると同時に、薬効があるだけでは医薬品にならないことも教えた薬でした。
ここには毒性管理の問題が重なります。
選択毒性があるとはいえ、毒性が消えたわけではありません。
病原体への作用と宿主への有害作用の差を、製剤設計と投与管理でどう現場に落とし込むかが問われました。
臨床で安全性を守るには、化合物そのものの性質だけでなく、どのように溶かし、どう投与し、どの条件で品質をそろえるかまで含めて考える必要があります。
私は製剤品質の話題に触れるたび、薬は分子式だけでできているわけではないと実感します。
ロットごとのばらつきが残れば、同じサルバルサンの名であっても臨床現場で受け取るリスクは揺れてしまいます。
投与手順の規格化も同じで、再現性のない運用はそのまま安全性の揺らぎになります。
現代ならGMPや標準操作手順で当然のように管理する領域ですが、サルバルサンの時代には、その必要性が臨床上の切迫した課題として立ち上がっていたのです。
1912年 ネオサルバルサンの改良点
そうした課題を受けて、1912年にはネオサルバルサンが登場します。
ここは名称と年次を分けて理解すると整理しやすく、1910年がサルバルサン、1912年が改良版のネオサルバルサンです。
両者を同じものとして扱うと、薬剤史の流れが見えにくくなります。
ネオサルバルサンの改良点は、要するに取り扱いの難しさを減らし、実地で使える形へ寄せたことにありました。
溶解性や調製の面で扱いやすくなり、投与時の運用負担を軽くする方向へ進んだのです。
これは単なる使い勝手の改善ではありません。
薬剤が現場で安定して再現されることは、そのまま安全性と有効性の再現につながります。
サルバルサンからネオサルバルサンへの流れを見ると、近代化学療法の成立には二つの段階があったことが分かります。
ひとつはエールリッヒと秦佐八郎が示した、選択毒性をもつ化合物の発見。
もうひとつは、その化合物を標準化し、毒性を管理しながら医療現場で運用可能な製剤へ仕上げる工程です。
前者だけでは歴史的発見にとどまり、後者があってはじめて治療の基盤になります。
サルバルサンは、抗菌化学療法史の出発点であると同時に、毒と薬の境界が分子設計と品質管理の両方で決まることを示した実例でもありました。
高毒性物質の局所投与が治療になる|ボツリヌス毒素から現代医療へ
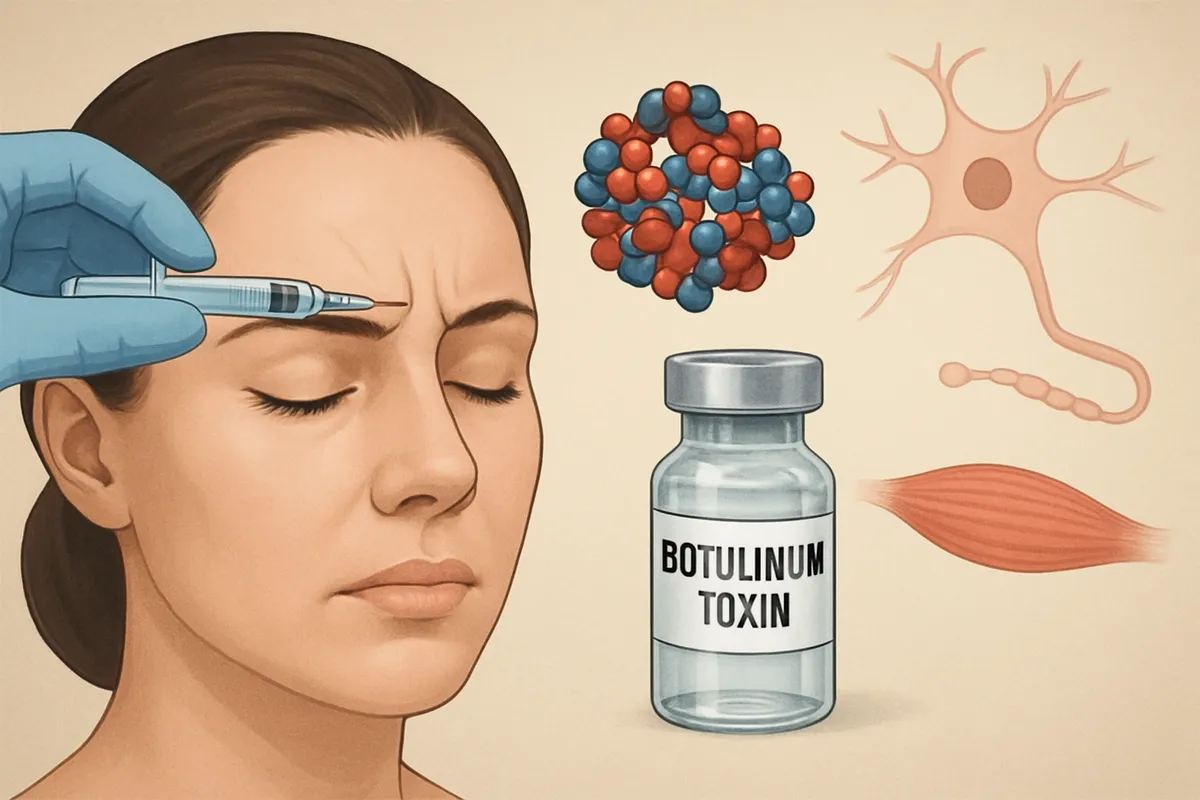
ボツリヌス毒素は、自然界でも屈指の強い毒ですが、医療ではその性質を逆手に取って使います。
筋肉の収縮を局所的に抑える作用を、厳密に量を管理したうえで注射することで、眼瞼けいれんや痙縮、片頭痛などの治療に応用できるのです。
ここでも重要なのは、毒を全身に浴びせるのではなく、狙った場所にごく少量だけ届けることでした。
高毒性物質が薬になる条件は、効く部位を限定できること、投与量を精密に制御できること、そして副作用を許容範囲に抑えられることです。
ボツリヌス毒素の臨床応用は、毒性そのものを消すのではなく、届け方を設計することで治療へ転化できることを示しています。
生物活性を局所投与で医療に生かす|ボツリヌス毒素から現代医療へ

分子機序:アセチルコリン放出阻害
ボツリヌス毒素が医療に転じた理由は、まず作用点が明確だったことにあります。
標的は神経筋接合部で、ここでは運動神経の末端からアセチルコリンが放出され、その信号を受けて筋肉が収縮します。
ボツリヌス毒素はこの放出過程を止めます。
結果として筋肉は一時的に力が入りにくくなり、可逆的な弛緩性麻痺が起こります。
分子レベルでは、毒素は神経終末の内部に取り込まれたあと、神経伝達物質を放出するために必要なSNARE複合体を切断します。
SNARE複合体は、小胞の膜と細胞膜をぴたりと接近させて融合させる、いわば放出装置の中核です。
この装置が壊れると、アセチルコリンを入れた小胞は膜と融合できず、神経から筋肉への命令が届かなくなります。
A型では主にSNAP-25が切断され、B・D・F・G型ではVAMP、C型ではSNAP-25とsyntaxinが標的になります。
ここで医療上の転換点になったのが、局所投与という発想でした。
毒素を全身に回すのではなく、症状の出ている筋や腺にごく微量だけ届ければ、作用を必要な場所に閉じ込められます。
私は安全性評価や製剤設計を考えるとき、局所投与の価値は「量を減らす」こと以上に、「体内のどこに濃度を立てるか」を制御できる点にあると感じます。
患部では必要な濃度を保ちつつ、血中に入った分は全身クリアランスで処理される。
この設計が成り立つと、猛毒であっても薬理作用だけを切り出せます。
1989年の初承認と臨床応用の始まり
医療応用の出発点は美容ではなく、眼科の切実なニーズでした。
異常に収縮する眼筋や眼周囲の筋を、外科手術だけに頼らず調整したい。
その課題に対して、ボツリヌス毒素の局所微量投与は理にかなっていました。
狙った筋だけの神経伝達を抑えれば、過剰収縮を和らげられるからです。
この流れの中で、1989年にFDAが斜視と眼瞼痙攣で初承認を与えます。
ここで評価されたのは、毒性の強さそのものではなく、標的が明確で、投与部位が限定され、効果が局所に現れ、全身毒性を避ける設計が成立していたことです。
毒性学の言葉で言えば、危険な物質を無害化したのではなく、曝露の地図を書き換えたことが承認の基盤になりました。
ここで評価されたのは、単純な毒性の強弱ではなく、標的が明確で、投与部位が限定され、効果が局所に現れ、全身曝露を最小化する設計が成立していたことです(出典: FDA承認記録(1989): その後の臨床応用は、眼科から神経内科、リハビリテーション、疼痛領域へと広がっていきます。
痙性斜頸のような局所ジストニア、脳卒中後の上肢痙縮、腋窩多汗症など、過剰な神経出力や分泌が問題になる病態では、ボツリヌス毒素の「局所で神経伝達を弱める」という性質がそのまま治療原理になります。
医療史として見ると、これは毒を薄めて使ったというより、病態の回路に合わせて毒の作用点を狭く切り取った例です。
2010年 慢性片頭痛と適応拡大
ボツリヌス毒素の医療的な意味がもう一段深まったのは、筋肉をゆるめる薬という理解を超えて、疼痛の制御にも役割を持つと認識されたときです。
象徴的なのが2010年の慢性片頭痛予防での承認。
これによってボツリヌス毒素は、眼科や運動異常の治療薬にとどまらず、頭痛診療でも位置づけを持つようになりました。
象徴的なのが2010年の慢性片頭痛予防での承認です(出典: FDA承認記録(2010): 慢性片頭痛での効果は、単純な筋弛緩だけでは説明しきれません。
末梢神経終末での神経伝達や、痛みに関わるシグナル放出の調整が関与すると考えると理解しやすくなります。
つまり、ボツリヌス毒素の本質は「筋肉を止める毒」ではなく、神経末端の放出機構に介入する分子だということです。
この見方に立つと、適応拡大が一つの筋道でつながります。
承認後は、痙性斜頸、上肢痙縮、多汗症などへと適応拡大が進みました。
いずれも共通するのは、症状の中心に局所的な神経活動の過剰があることです。
美容領域で知られることの多い薬ですが、実際の医療的意義は、眼科では異常眼球運動や眼輪筋のけいれんを抑え、神経内科ではジストニアや痙縮を軽減し、疼痛領域では慢性片頭痛の発作頻度低減に寄与するという、幅広い臨床価値の上に成り立っています。
毒素型A〜Gと製剤・単位の違い

ボツリヌス毒素には、主要なものとしてA型からG型までの7型があります。
すべてが同じ働きをするわけではなく、どのSNAREタンパク質を切断するかが型ごとに異なります。
その違いが、作用の性質や持続、臨床応用のしやすさに結びつきます。
医療で主に用いられてきたのはA型で、一部ではB型も使われます。
ここで注意したいのは、「同じA型ならどの製剤も同じ」とは言えないことです。
医療用製剤は、毒素そのものの精製法、複合タンパク質の扱い、力価の定義などに差があります。
そのため投与単位は製剤ごとに標準化されていても、相互互換ではありません。
この点は薬理学的にも臨床的にも見落とせず、単位の数字だけを見て横並びに換算する発想は成り立ちません。
私はこの違いを、単なるメーカー都合ではなく、バイオ医薬品に近い性格の表れとして捉えています。
小分子薬なら有効成分量で比較しやすい場面がありますが、タンパク質毒素製剤では、生物活性をどう測り、どう規格化したかが製品の顔つきそのものを決めます。
だからこそ「A型」という大きなくくりと、「実際に投与する製剤」は分けて理解したほうが、臨床の現実に近づきます。
安全管理:適正使用と標準化
そのため現代医療では、標準化された製剤、規格化された単位、解剖学に基づく投与手技、適応ごとの使用指針が組み合わされています。
これは前のセクションで触れた製剤標準化の発想が、毒素医薬でより厳密に実装された形でもあります。
どの筋に、どれだけ、どの深さで、どの間隔で投与するかが再現されてこそ、局所効果と安全域が両立します。
高毒性物質を薬として成立させる条件は、作用機序の理解だけでなく、適正使用を支える運用の精度にあります。
そのため現代医療では、標準化された製剤、規格化された単位、解剖学に基づく投与手技、適応ごとの使用指針が組み合わされて運用されています。
そのため現代医療では、標準化された製剤、規格化された単位、解剖学に基づく投与手技、適応ごとの使用指針が組み合わされています。
これは前のセクションで触れた製剤標準化の発想が、毒素医薬でより厳密に実装された形でもあります。
どの筋に、どれだけ、どの深さで、どの間隔で投与するかが再現されてこそ、局所効果と安全域が両立します。
⚠️ Warning
ボツリヌス毒素の医療的価値は、「危険な毒を安全にした」ことより、「毒の作用を局所に限定し、標準化された手技で再現できるようにした」点にあります。本記事は毒物の製造手順や非医療目的の使用方法について解説するものではありません。
この標準化があるからこそ、ボツリヌス毒素は眼科・神経内科・疼痛診療で長く使われる治療選択肢になりました。
毒の強さそのものは変わっていません。
変わったのは、どこに届け、どこで止め、どう再現するかという医療側の設計です。
毒と薬の境界が、用量だけでなく投与経路と品質管理でも引き直されることを、これほど鮮やかに示す例は多くありません。
毒が薬になる条件

条件1:用量と治療域
毒が薬になる第一条件は、どこから効き始め、どこから害が前面に出るかを、用量で切り分けられることです。
ここで土台になるのが治療域と安全域の考え方です。
治療域は、有効性が現れる範囲と有害性が目立ち始める範囲のあいだにある操作可能な領域を指します。
古典的には治療指数(TI)がその輪郭を示しますが、実務では数字ひとつで安全性を言い切ることはありません。
動物での LD50 と ED50 から求めた TI は便利な目安ではあっても、臨床で扱うのはもっと揺らぎを含んだ現実だからです。
その揺らぎを含めて捉える言葉が、安全域です。
安全域は固定された一本の線ではなく、確率論的な幅として理解したほうが実態に近いです。
年齢、肝機能や腎機能、疾患背景、併用薬、さらには同じ薬でも投与タイミングや曝露量のばらつきで、実効的な幅は動きます。
狭い治療域の薬では、この幅のわずかな移動が有効域から毒性域への越境につながります。
逆に言えば、毒を薬として成立させるには、「安全な量がある」だけでは足りず、その幅を再現よく維持できることが必要になります。
私は安全性試験の実務にいたとき、非臨床から臨床へ橋を架ける作業は、まさにこの幅をどう読むかに尽きると感じていました。
反復投与毒性試験などから NOAEL や LOAEL を見極め、そこからヒト等価用量に換算し、安全係数をかけて初期用量を置く。
その後、ヒト初回投与では一足飛びに「効く量」へ行かず、用量反応探索で最小有効用量と最大耐用量の距離を確かめていきます。
帳尻合わせの計算ではなく、どの用量なら利益が立ち上がり、どの用量から不利益が先に走るかを一段ずつ描き直す工程です。
サルバルサンをこの枠組みで見ると、鍵はヒ素化合物を無害化したことではなく、病原体に対する効果が立ち上がる用量と、宿主に対する毒性が前面化する用量のあいだに、なんとか臨床操作できる幅を見いだした点にあります。
ボツリヌス毒素では事情が少し異なり、全身で見れば危険な分子でも、局所微量投与によって実効上の治療域を成立させています。
つまり用量は、単独ではなく投与経路や標的選択性と組み合わさって初めて意味を持ちます。
条件2:投与経路と局所化
同じ物質でも、どこから入れるかで毒性の地図は大きく変わります。
経口、静脈内、筋肉内、局所注射、外用では、吸収速度も全身曝露も到達組織も違います。
毒が薬になる第二条件は、病変部位に作用を届けつつ、不要な全身曝露をできるだけ減らすことです。
言い換えれば、薬効を目的地に集中させ、副作用を起こす回り道を短くする設計です。
ボツリヌス毒素はこの条件を最も鮮明に示します。
神経毒としての本質は変わっていませんが、局所に微量投与し、標的となる神経終末の近くで作用を発現させることで、全身への広がりを抑えています。
前のセクションで触れたように、これは毒を弱くしたのではなく、曝露を局所に閉じ込めたのです。
だからこそ、同じ分子が食中毒や乳児ボツリヌス症では脅威であり、医療現場では治療手段にもなります。
サルバルサンはボツリヌス毒素ほど局所化に依存する薬ではありませんが、それでも投与経路の設計は本質的でした。
全身治療が必要な感染症では、病原体に届くだけの曝露を確保しながら、宿主の毒性をどこまで許容するかという問題が避けられません。
ここでは局所化そのものより、全身曝露を制御可能な形で与えることが条件になります。
毒を薬に変える道筋は一つではなく、局所に閉じ込める方法もあれば、全身で使う代わりに曝露を管理する方法もあります。
臨床開発では、この投与経路の違いが初期用量設定にもそのまま反映されます。
非臨床で得られた NOAEL をそのまま並べるのではなく、どの経路で投与したデータなのか、局所曝露と全身曝露のどちらが薬効に効いているのかを見極める必要があります。
AUC や Cmax を見ながら橋渡しをしていく作業は地味ですが、ここが曖昧だと、動物で安全に見えた条件がヒトでは別物になります。
用量だけでなく、用量がどの経路で身体に入ったかまで含めて読むのが毒性学の作法です。
条件3:標的選択性
第三条件は、誰に効いて、誰にはなるべく効かないかという標的選択性です。
毒が薬になるとき、理想は病原体や病態の回路には強く作用し、正常組織への影響は抑えられていることです。
エールリッヒが化学療法で追いかけた発想も、現代の分子標的薬も、この点では同じ地平に立っています。
サルバルサンでは、梅毒の病原体に対して宿主より強い障害を与えるという選択毒性が出発点でした。
もちろん、当時の薬は現代基準の高選択的分子標的薬のように洗練されていたわけではありません。
それでも「毒であること」と「薬であること」を分けたのは、標的が無差別ではなかった点です。
病原体を叩く利益が、宿主側の毒性を上回る場面があったから、臨床的な意味を持ちました。
ボツリヌス毒素では選択性の形が異なります。
これは病原体を狙う薬ではなく、特定の神経終末の放出機構に介入する分子です。
医療で主に用いられる型では、SNARE 複合体を構成するタンパク質の一部を切断し、神経伝達物質の放出を抑えます。
A型やE型は SNAP-25、B・D・F・G型は VAMP、C型は SNAP-25 と syntaxin に作用します。
ここで効いているのは、単に「神経を止める」ことではなく、特定の細胞機構に分子的に触るという選択性です。
局所投与と組み合わさることで、その選択性が治療として立ち上がります。
毒性学の原理として見ると、標的選択性は「効くか効かないか」の二択ではありません。
標的への親和性、標的組織への到達性、標的以外への作用の出方、その全部を重ねて読んでいく必要があります。
だから、同じ用量でも標的に集まる薬は薬になりやすく、標的外に散る薬は毒性が先に出ます。
毒と薬の境界線は、分子の強さだけでなく、作用がどれだけ狙った場所に偏っているかで引き直されます。
条件4:製剤化・規制・標準化
毒が薬になるには、作用機序や用量の理屈だけでは足りません。
第四条件として欠かせないのが、同じものを同じ品質で再現できることです。
ここで初めて、製剤化、規制、標準化の話が前面に出てきます。
どれほど面白い分子でも、ロットごとに活性がぶれる、分解しやすい、投与単位が再現できないという状態では医療に乗りません。
サルバルサンの時代にも、取扱いの難しさや毒性管理は大きな課題でした。
現代の基準で見れば、製剤学と品質保証の仕組みはまだ発展途上です。
一方、ボツリヌス毒素のような生物活性の高い製剤では、この条件が薬としての成立そのものを左右します。
型が同じでも製剤が違えば、精製法、規格化の方法、力価の定義が異なります。
そのため単位は製剤ごとに閉じており、数字だけを横に並べても意味が一致しません。
ここでは製剤化そのものが安全性の一部です。
この再現性を支えるのが、非臨床の信頼性を担保する GLP と、製造の一貫性を担保する GMP です。
試験計画、SOP、QA、記録保存、ロット管理、バリデーションといった仕組みは、一見すると地味ですが、毒を医薬品として扱うための骨格です。
どのロットでも同じ活性が出ること、混入や劣化が管理されること、出荷判定が文書化されることがあって、はじめて臨床での用量設定が意味を持ちます。
規制科学の実務では、この標準化と用量反応評価が一体で動きます。
PMDAやICHの枠組みで行われる用量-反応評価は、単に承認資料を整える作業ではありません。
非臨床データから初回ヒト投与量を定め、探索試験で反応曲線を描き、最小有効用量と忍容限界の距離を詰めていく。
その過程全体が、リスク最小化の設計図になっています。
私の感覚では、毒性学は「危ないものを見つける学問」というより、危険を測り、境界を管理可能な形に変換する学問です。
毒が薬になる瞬間は、しばしば実験室よりも、標準化された運用の中で完成します。
💡 Tip
毒が薬になる条件は、強い作用を弱めることではありません。用量、投与経路、標的、品質管理の4点をそろえて、利益が毒性を上回る範囲を再現可能にすることです。
比較表:サルバルサン/ボツリヌス/用量反応

個別事例を一般化して眺めると、サルバルサンもボツリヌス毒素も、そしてパラケルスス以来の用量反応の原理も、同じ地図の上に置けます。
違うのは「どの条件が主役になるか」です。
サルバルサンでは選択毒性と全身曝露の管理、ボツリヌス毒素では局所化と製剤標準化、原理としての毒性学では用量反応の定量化が中心軸になります。
| 観点 | サルバルサン | ボツリヌス毒素 | 用量反応の原理 |
|---|---|---|---|
| 主な時代 | 20世紀初頭 | 20世紀後半から現代 | 16世紀以降に理論化され、現代で定量化 |
| 毒の種類 | 有機ヒ素化合物 | 神経毒タンパク質 | 個別毒物ではなく評価原理 |
| 薬になった鍵 | 病原体に対する選択毒性 | 局所微量投与と神経終末への限定作用 | 用量と反応を同じ軸で読むこと |
| 用量の考え方 | 有効性と全身毒性の釣り合いを探る | 微量でも作用するため単位管理が核心になる | 治療域と安全域を定量化する |
| 投与経路の意味 | 全身治療として曝露制御が必要 | 局所化で全身曝露を最小化する | 経路差で毒性の地図が変わる |
| 標的選択性 | 宿主より病原体に強く効かせる | SNARE を介した特定神経機構への介入 | 標的への偏りが毒性と薬効を分ける |
| 製剤化・標準化 | 取扱いと毒性管理が課題だった | 製剤ごとの力価・単位の標準化が不可欠 | 規制下での再現性が臨床判断を支える |
| 安全域の捉え方 | 狭い幅の中で利益を成立させる | 局所投与で実効的な幅を確保する | 個体差・併用薬・疾患背景で幅が動く |
この比較から見えてくるのは、毒が薬になる条件は単一ではなく、4つの条件の組み合わせで決まるということです。
ある毒は標的選択性で薬になり、別の毒は局所化で薬になり、どちらの場合も最終的には製剤化と規制の網を通って、再現可能な医療技術へ変わります。
ここを押さえると、個別の逸話がばらばらの歴史ではなく、同じ原理の異なる実装例として読めるようになります。
近代毒性学は何を変えたのか

オルフィラの功績と用語整理
パラケルススが「用量が毒を決める」という原理を言葉にしたあと、毒を観察と実験で体系化する学問へ押し進めた人物がオルフィラです。
1787年生まれ、1852年没のこの法医学者は、毒を単なる恐怖や逸話の対象ではなく、症状、臓器変化、化学分析、死後所見を結びつけて読む対象に変えました。
ここで毒の知識は、経験則から実験毒物学へと姿を変えます。
中毒死の解明、裁判での立証、解剖所見との対応づけが進み、毒をめぐる議論に再現性と証拠の軸が入りました。
この流れのなかで、いま日本語で混同されがちな用語も整理しておくと見通しが立ちます。
毒性学は、物質が生体にどのような有害作用を示すかを、用量、曝露経路、標的臓器、作用機序、時間軸まで含めて扱う学問です。
現代のtoxicologyに最も近い中心語はこれです。
毒物学は歴史的にはtoxicologyの訳語として広く使われてきた言葉で、毒物そのものの性質、鑑別、分析、法医学的応用に重心が置かれる場面で今も通じます。
中毒学は臨床の現場により近く、急性中毒や慢性中毒の診断、治療、解毒、全身管理を扱うclinical toxicologyの文脈で使うと位置づけが明瞭です。
実務感覚で言えば、毒性学は「なぜ害が出るのか」を読み解く学問、毒物学は「何が入っていたのか」を突き止める学問、中毒学は「いま起きている障害にどう対応するか」を扱う学問です。
もちろん境界は重なります。
製薬の安全性評価に携わると、非臨床の毒性学、分析科学としての毒物学、臨床現場の中毒学が一本の線につながっていることを日常的に感じます。
オルフィラの仕事が残したのは、まさにその接続の原型でした。
毒をめぐる知識が、法医学、薬理学、臨床医学のあいだを行き来できるようになったのです。
20世紀の規制と標準化
20世紀に入ると、毒の研究は「知る」段階から「管理する」段階へ進みます。
医薬品として使う以上、同じ化合物が毎回同じ挙動を示し、同じ試験法で評価され、同じ品質で供給されなければなりません。
この要請が、試験法の整備、規格化、ロット管理、記録保存、品質保証の仕組みを押し上げました。
毒性学はここで、実験室の学問であると同時に規制科学の基盤になります。
非臨床ではGLPが試験成績の信頼性を支え、製造ではGMPがロットごとの再現性を支えます。
これによって、安全性データは「その研究者がそう見た」という話ではなく、「どの施設で、どの計画で、どの記録体系のもとに得られたか」が読めるデータへ変わりました。
さらに国際的な開発ではICHの整備によって、安全性評価、用量設定、開発段階ごとの必要試験が共通言語化されます。
ここで前のセクションまでに見てきた用量反応の原理は、承認審査に耐える形式へ翻訳されました。
その翻訳を象徴するのが、NOAEL と LOAEL のような概念です。
どの用量までは有害影響が観察されなかったのか、どの用量から有害影響が現れたのかを切り分け、その情報を初回ヒト投与量や反復投与試験の設計に接続する。
製薬企業の安全性研究では、この線引きが机上の理屈では終わりません。
動物試験で得た NOAEL をそのまま人へ持ち込むのではなく、ヒト等価用量への換算、安全係数の適用、曝露指標の確認を重ねて、ようやく開始用量の議論になります。
私自身、この計算過程を初めて業務として追ったとき、毒性学は「危険な量を避ける」学問というより、まだ起きていない危険を先回りして数値に置き換える仕事なのだと実感しました。
この標準化の意義は、毒を消し去ることにありません。
ヒ素化合物でも、細胞毒でも、神経活性の強い物質でも、開発の現場では「どこまでが利益で、どこからが害か」を試験系の中で可視化し、その境界を越えない設計を積み重ねます。
20世紀の近代毒性学が変えたのは、毒を善悪の言葉で扱う習慣ではなく、毒性を測定可能で比較可能な対象に変えたことです。
2026年の学会動向と教育
この学問がいまも更新され続けていることは、日本毒性学会の活動を見るとよくわかります。
毒性学は古典的な毒物の話だけで閉じた領域ではなく、創薬安全性、化学物質評価、環境曝露、オミクス、新規モダリティ、計算毒性学まで含む広い学際領域として動いています。
2026年7月1日から3日に第53回学術年会が予定されていること自体、研究基盤と教育基盤が継続的に回っている証拠です。
2026年2月には基礎教育講習会の案内も出ており、研究者養成だけでなく、分野横断で安全性リテラシーを底上げする流れが続いています。
学会年会に参加すると、この分野の教育文化には独特の厚みがあると感じます。
シンポジウムや一般演題だけでなく、基礎教育講習のような場がきちんと用意されていて、薬理、病理、分析、規制、臨床をまたぐ人たちが同じ言葉をそろえていく。
私もそうした教育講習に触れたとき、毒性学は専門家だけの閉じた技能ではなく、異分野の人が共通の安全性言語を身につけるためのインフラなのだと腑に落ちました。
ある領域では自明の概念でも、別の領域では意味づけが違う。
そこを丁寧に接続する場があるから、毒性所見、曝露、病理変化、臨床症状、規制判断が一本につながります。
2025年から2026年にかけての学会動向を見ても、毒性学の現在地は「古い毒の知識の集積」ではありません。
新しいモダリティが出るたびに、従来の試験系で足りるのか、バイオマーカーはどう読むのか、ヒト予測性をどう高めるのかが問い直されます。
だからこそ日本毒性学会のような場は、歴史を語る記事の中でも現在形で触れる意味があります。
毒が薬になる条件は過去に完成した知恵ではなく、いまも更新中の技術体系です。
制御という近代の回答
近代毒性学が出した答えは、毒をこの世からなくすことではありませんでした。
実際の医療や創薬で起きているのは、毒を制御可能な対象として扱うという発想の定着です。
用量を決め、経路を選び、標的を絞り、品質をそろえ、試験系を標準化し、ヒトへの移行を段階的に管理する。
こうしてはじめて、毒性は排除すべき混沌ではなく、設計に組み込むべき条件になります。
この転換は、医薬品開発の根幹そのものです。
毒性学の役割は「危ないからやめる」と告げることだけではなく、「どの条件なら許容できるか」を具体化することにあります。
治療域、NOAEL、LOAEL、FIH 用量設定、GLP、GMP、ICH といった言葉は、どれもこの制御思想の別の顔です。
私には、近代毒性学とは毒を弱めた学問というより、毒を境界管理の対象へ変えた学問に見えます。
ℹ️ Note
近代以降の毒性学が築いたのは、「毒か薬か」を二者択一で裁く仕組みではありません。利益と有害性が交わる境界を測り、その境界内で再現可能な医療を成立させる仕組みです。
この視点に立つと、サルバルサンもボツリヌス毒素も例外ではなくなります。
危険な物質が偶然薬になったのではなく、危険を測り、狙いを定め、規格化し、臨床で再現できる形へ落とし込んだから薬になった。
近代毒性学が変えたのは、毒そのものというより、人間が毒と向き合う方法だったのです。
まとめ|毒が薬に変わるとき、人類は何を学んだのか
毒が薬に変わる場面で人類が学んだのは、毒を消す技術ではなく、毒を制御する技術でした。
用量を定め、投与経路を選び、標的選択性を見極め、標準化で再現性を担保する。
この発想は、パラケルススから近代毒性学、そして現代の医薬品開発まで一本につながっています。
私自身、学びを定着させたいときほど、学会資料や公的文書のような一次情報に戻る癖が役に立つと感じています。
歴史の逸話が、開発や審査の言葉へつながる瞬間が見えるからです。
この記事を入口に、パラケルススボツリヌス毒素抗毒素史の個別テーマや、PMDA日本毒性学会の公開資料まで視野を広げると、「毒と薬は紙一重」という言葉が比喩ではなく技術史そのものだったことが、よりはっきり見えてきます。
薬学部で毒性学を専攻し、製薬企業の安全性研究部門で毒性試験に従事。「毒と薬は紙一重」をモットーに、毒物の作用機序から医薬品への転換まで、分子レベルの科学をわかりやすく解説します。
関連記事
ボツリヌス毒素からボトックスへ|最強の毒が美容医療を変えた
ボツリヌス毒素は「最強の毒」とだけ語ると、本質を見失います。毒性学の実務でまず見るのは、何mgかではなく、どこに、どれだけ、どの経路で入るかという三つで、全身に回る中毒と、医師が局所へごく微量を打つ医療は、同じ物質でも意味がまるで変わります。 ボツリヌス毒素は毒と薬という二面性を持つ分子です。
トリカブトと漢方の附子|毒が薬になるまで
山菜と見分けを誤れば命に関わるトリカブトは、塊根を加工し、規格の中で管理すると、生薬附子(ブシ)として医療の現場に入ってきます。この記事は、毒草としての植物が、どうやって処方に組み込まれる医薬の素材へ変わるのかを知りたい人に向けて、その道筋を一本の線でたどるものです。
ジギタリスの物語|毒から薬、そして再評価
花壇では優美に見えるジギタリスは、ひとたび体内に入れば心臓に触れる毒でもあります。その危うい植物が、18世紀の観察医学から現代の薬理学へどう橋を架け、心不全治療の景色をどう変えたのかを追うのが本稿です。
抗毒素と血清療法|北里柴三郎が開いた道
北里柴三郎を語るとき、主役は人物名だけでは足りません。焦点に置くべきなのは毒素そのものと、それを狙い撃ちで中和する抗毒素、そしてその抗体を投与して即効性を引き出す血清療法という発想です。